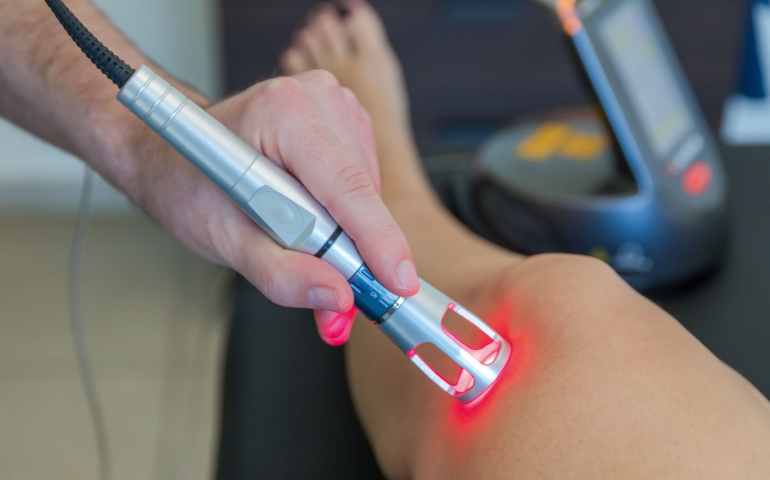
Klasyfikacja laseroterapii
Historia laseroterapii sięga lat 60. XX wieku. Pierwszy laser rubinowy zademonstrowano w 1960 roku, a już w 1967 roku Endre Mester, węgierski lekarz i naukowiec, zauważył, że zastosowanie światła lasera na skórze myszy powoduje przyspieszenie gojenia się ran. To odkrycie było początkiem badań nad terapeutycznym zastosowaniem lasera. W kolejnych latach badania nad laseroterapią skupiały się na zastosowaniu lasera w leczeniu różnych schorzeń, takich jak choroby skóry, choroby oczu, schorzenia mięśniowo-szkieletowe czy bóle głowy.
Laseroterapia to pojęcie bardzo szerokie, obejmujące nie tylko dziedzinę fizjoterapii, ale również zastosowania w chirurgii, stomatologii i medycynie estetycznej. W tym artykule ograniczymy się do zastosowań w fizjoterapii z uwzględnieniem niektórych terapii dolegliwości skórnych, gdyż z istoty rzeczy promienie lasera działają na tkanki skóry. Promienie laserowe, czyli wiązki spójnego światła monochromatycznego, w fizjoterapii spełniają na ogół funkcję wspomagania procesów leczniczych narządu ruchu, stymulując procesy fizjologiczne zachodzące w organizmie. Laseroterapia pomaga w łagodzeniu bólu, redukcji stanów zapalnych, w przyspieszaniu procesów regeneracyjnych tkanek oraz poprawie krążenia. Najczęściej zabiegi laseroterapii są stosowane przy leczeniu urazów sportowych, chorób stawów, bólów mięśniowych oraz obrzęków pourazowych.
Laseroterapia może być przeprowadzana w różnych trybach pracy, w zależności od celu leczenia. W trybie ciągłym promienie laserowe są emitowane w postaci ciągłej fali elektromagnetycznej, natomiast w trybie pulsacyjnym promienie są emitowane w krótkich impulsach. Tryb pulsacyjny może być bardziej skuteczny w przypadku leczenia niektórych schorzeń.
Laseroterapia jest zazwyczaj bezpieczna i nieinwazyjna, a jej skutki uboczne są rzadkie. Niemniej jednak, jak dla każdej formy terapii, istnieją pewne ograniczenia i przeciwwskazania, w tym ciąża, choroby nowotworowe, nadwrażliwość na światło, zaburzenia krwotoczne czy zaawansowana miażdżyca.Przystępując do przeglądu aparatów stosowanych w laseroterapii, aby uporządkować prezentację, trzeba przyjąć jakiś system klasyfikacji.
Ze względu na właściwości fizykotechniczne jako kryteria klasyfikacji można brać pod uwagę dwa podstawowe parametry laserów:
- moc wyjściowa lasera, mierzona w watach (W), która obejmuje bardzo szeroki zakres od pojedynczych miliwatów (mW) do setek watów;
- długość fali promieniowania lasera, od której zależy głębokość penetracji fotonów w tkankach. Fotony o krótszej fali mają większą energię. W laseroterapii stosuje się światło w zakresie podczerwieni (długość fali ponad 800 nm, głównie 810 nm, 904 nm i 1064 nm) i światło czerwone (długość fali 600 ÷ 700 nm). Fotony w tych zakresach długości fali są dobrze absorbowane przez chromofory zawarte w tkankach, takie jak hemoglobina i mioglobina.
Klasyfikacja ze względu na moc wydaje się być prosta, ale w rzeczywistości można się spotkać z różnymi podziałami w zależności od kryteriów związanych z przeznaczeniem danej klasyfikacji. Ze względu na konieczność przestrzegania warunków bezpieczeństwa pracy z laserem najczęściej przyjmuje się klasyfikację amerykańskiej Agencji d/s Żywności i Leków (FDA), która obejmuje cztery klasy:
- I: Lasery o mocy wyjściowej poniżej 0,5 mW, które są bezpieczne dla oczu i skóry.
- II: Lasery o mocy wyjściowej poniżej 1 mW, które są również bezpieczne dla oczu i skóry.
- IIIa: Lasery o mocy wyjściowej poniżej 5 mW, które są bezpieczne dla oczu, ale mogą powodować uszkodzenia skóry w przypadku długotrwałego naświetlania.
- IIIb: Lasery o mocy wyjściowej pomiędzy 5 a 500 mW, które mogą powodować uszkodzenia oczu i skóry. W przypadku tych laserów konieczne jest stosowanie specjalistycznej ochrony oczu.
- IV: Lasery o mocy wyjściowej powyżej 500 mW, które mogą powodować poważne uszkodzenia oczu i skóry. Stosowanie tych laserów wymaga specjalnej ostrożności i zabezpieczeń, takich jak osłony oczu i ograniczenie czasu naświetlania.
Laseroterapia zazwyczaj wykorzystuje lasery IIIa i IIIb, ponieważ są one wystarczająco mocne, aby ich promieniowanie przenikało przez skórę i wpływało na tkanki, a zarazem wystarczająco bezpieczne dla pacjenta przy zachowaniu określonych środków ostrożności. Laseroterapia w zakresie mocy określonej dla klas IIIa i IIIb jest nazywana niskoenergetyczną. Lasery należące do klasy IV służą do laseroterapii nazywanej wyskoenergetyczną. Jednak klasa IV jest zbyt szeroka dla rozróżnienia wielu aparatów ze względu na moc, bo mieszczą się w niej zarówno lasery o mocy ok. 1 W jak też lasery o mocy kilkudziesięciu, czy kilkuset watów, o całkowicie różnych zastosowaniach. Ponadto, dla określenia skutków napromieniowania światłem lasera liczy się nie tyle moc źródła światła, co energia absorbowana przez tkanki, czyli iloczyn mocy i czasu trwania impulsu naświetlającego.
W istocie, liczy się dawka absorbowanej energii, czyli wartość energii na jednostkę napromieniowanej powierzchni (J/cm²). Ze względu na kryterium dawki energii absorbowanej przez ciało, która zależy nie tylko od mocy, ale też od czasu naświetlania i powierzchni naświetlanego obszaru, rozróżnia się następujące trzy kategorie:
- laseroterapia niskoenergetyczna (LLLT – Low Level Laser Therapy), w której stosuje się lasery o niskiej mocy, co skutkuje dawkami energii poniżej 10 J/cm²
- laseroterapia średnioenergetyczna (MLLT - Medium Level Light Treatment), w której stosuje się lasery średniej mocy, co skutkuje dawkami energii do 100 J/cm²
- laseroterapia wysokoenergetyczna (HLLT – High Level Laser Therapy), w której stosuje się lasery dużej mocy, co skutkuje dużymi dawkami energii, powyżej 100 J/cm²
Zatem w zestawie parametrów fizykotechnicznych, poza mocą i długością fali pojawia się czas i powierzchnia naświetlania, a to wiąże się z parametrami impulsów światła i kształtem wiązki promieniowania. Sprawy się komplikują i nadmiernie oddalamy się od pojęć praktycznych dla fizjoterapeuty. Wydaje się, że najbardziej odpowiednim kryterium klasyfikacji aparatów do laseroterapii jest ich przeznaczenie do określonych rodzajów laseroterapii. Można wyszczególnić kilka najczęściej stosowanych rodzajów laseroterapii, różniących się specyficznymi cechami i rodzajem zastosowań:
- laseroterapia niskoenergetyczna (LLLT)
- laseroterapia wysokoenergetyczna (HILT)
- laseroterapia frakcyjna (FLT)
- laseroterapia fotodynamiczna (PDT)
Ograniczymy się do prezentacji tych czterech form terapii, chociaż rozróżnia się poza tym laseroterapię akupunkturową, LED-ową (w istocie LED to nie laser – nie daje wiązki światła spójnego) i parę innych.
Laseroterapia niskoenergetyczna (LLLT)
Lasery niskoenergetyczne generują moc rzędu od 1 mW do 500 mW, gęstość mocy waha się w zakresie od 10 mW/cm² do 10 W/cm², a gęstość energii od 100 mJ do 100 J/cm². Mogą pracować w trybie ciągłym lub impulsowym z częstotliwością impulsów do 5000 Hz. Emitują fale o długości od 300 do 10 600 nm, czyli od nadfioletu do zakresu średniej podczerwieni. Najczęściej stosuje się lasery rubinowe (694 nm), argonowy (488 i 514 nm), helowo-wneonowe (633 nm), Ga Al As (805 lub 650 nm), Ga As (904 nm), CO2 (10 600 nm). Wydawałoby się, że im dłuższa fala, tym płycej wnika promieniowanie (mniejsza energia fotonów), czyli w zależności od barwy emitowanego światła (od nadfioletu do podczerwieni) zmienia się rodzaj tkanki, przez którą światło jest bardziej pochłaniane.
Jednak jest to problem bardziej skomplikowany. Rzeczywiście, na gruncie fizyki wiemy, że fotony o większej energii (mniejszej długości fali) mają większe prawdopodobieństwo wnikać głębiej w naświetlany materiał niż fotony o mniejszej energii. Fotony to kwanty energii elektromagnetycznej, które mogą oddziaływać z materią na różne sposoby w zależności od ich energii. Na przykład wysokoenergetyczne fotony promieniowania rentgenowskiego lub promieniowania gamma penetrują bardzo głęboko (przenikają ciało człowieka) i mogą jonizować atomy, czyli wpływać na strukturę penetrowanej materii. Fotony o niższej energii (większej długości fali), takie jak promieniowanie od nadfioletu do podczerwieni stosowane w laseroterapii, nie mają wystarczającej energii, by jonizować atomy i cząsteczki (nie są groźne jak promienie rentgenowskie), ale oddziałują z materią przez odbicie, załamanie, rozpraszanie i absorpcję. W zabiegach laseroterapii ok.połowa promieniowania ulega odbiciu, a pozostałe fotony ulegają absorpcji, czyli pochłanianiu przez atomy i cząsteczki tkanek. Krótkie fale laserowe (np. 514 nm) są absorbowane przez melaninę, zatem są skuteczne w leczeniu niektórych zmian skórnych, ale mają niewielką penetrację w głąb tkanki. Długie fale lasera (np. 1064 nm) są mniej absorbowane przez melaninę i mają większą penetrację w głąb tkanki, zatem są skuteczne nie tylko w leczeniu niektórych zmian skórnych, takich jak naczyniaki, ale też w leczeniu zmian w układzie mięśniowo-szkieletowym.
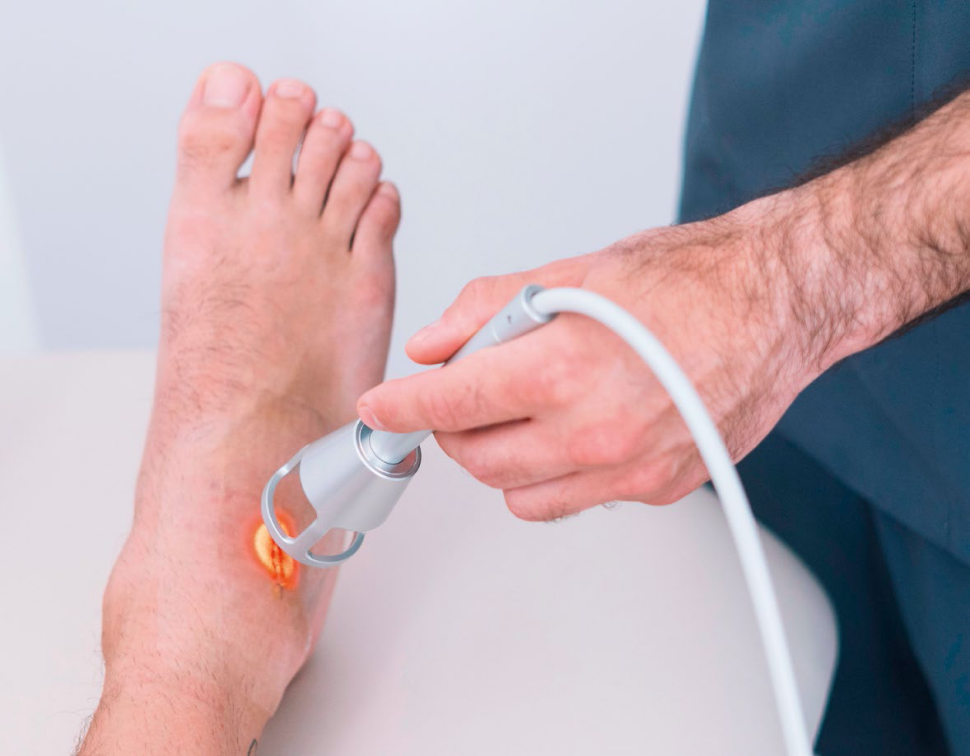
Lasery niskoenergetyczne nazywane są też zimnymi, ponieważ nie wywołują efektu termicznego. Ich działanie polega na wchłanianiu przez tkanki światła o odpowiedniej długości fali, co prowadzi do stymulacji enzymów mitochondrialnych, zwiększonej produkcji ATP, poprawy cyrkulacji krwi i innych procesów metabolicznych. Procesy biostymulacji dają określone efekty terapeutyczne, pomagają w leczeniu różnych schorzeń, w tym bólu, obrzęku, zapalenia, uszkodzeń mięśni i tkanek łącznych, a także chorób autoimmunologicznych. Efekty terapeutyczne zależą od wielu czynników, takich jak dawka światła, długość fali, czas ekspozycji, rodzaj tkanki i stan chorobowy pacjenta. LLLT jest uważana za bezpieczną metodę leczenia, należy jednak pamiętać o wcześniej wymienionych kategoriach pacjentów wykluczonych dla stosowania laseroterapii. W bogatym piśmiennictwie naukowym na temat terapii LLLT polecamy pozycje1÷5, które szczególnie przyczyniły się do lepszego zrozumienia tej terapii i jej skuteczności w leczeniu różnych chorób i urazów. Oferta rynkowa aparatów do laseroterapii LLLT jest bardzo bogata.
Oto kilka przykładów:
Handy Cure - ręczny aparat do laseroterapii o niskiej mocy, wykorzystujący diody laserowe o różnej długości fali, umożliwiający aplikację promieniowania laserowego bezpośrednio na skórę.
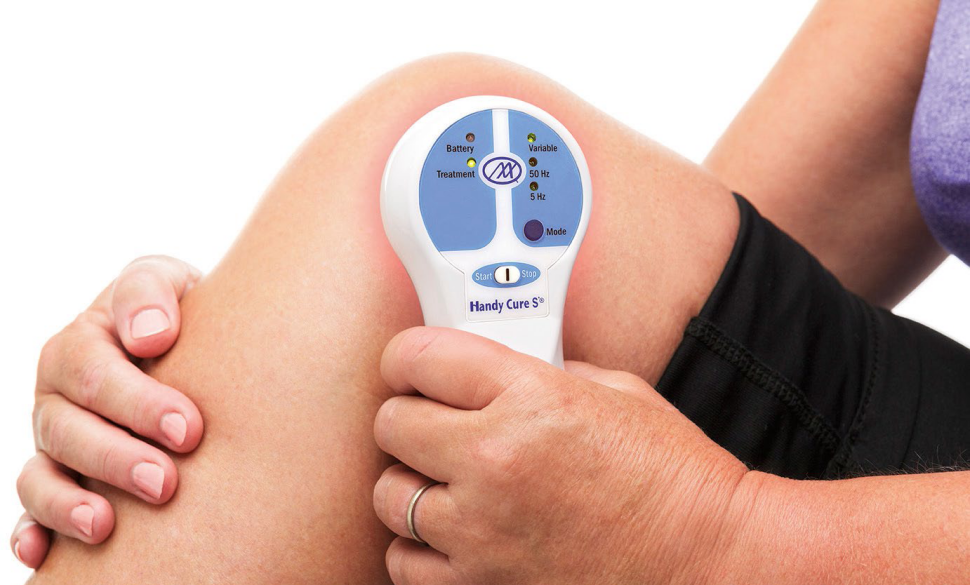
LaserTRX - aparat z sondami laserowymi, umieszczanymi bezpośrednio na powierzchni ciała, umożliwiający precyzyjną aplikację promieniowania laserowego o niskiej mocy na wybrane obszary ciała.
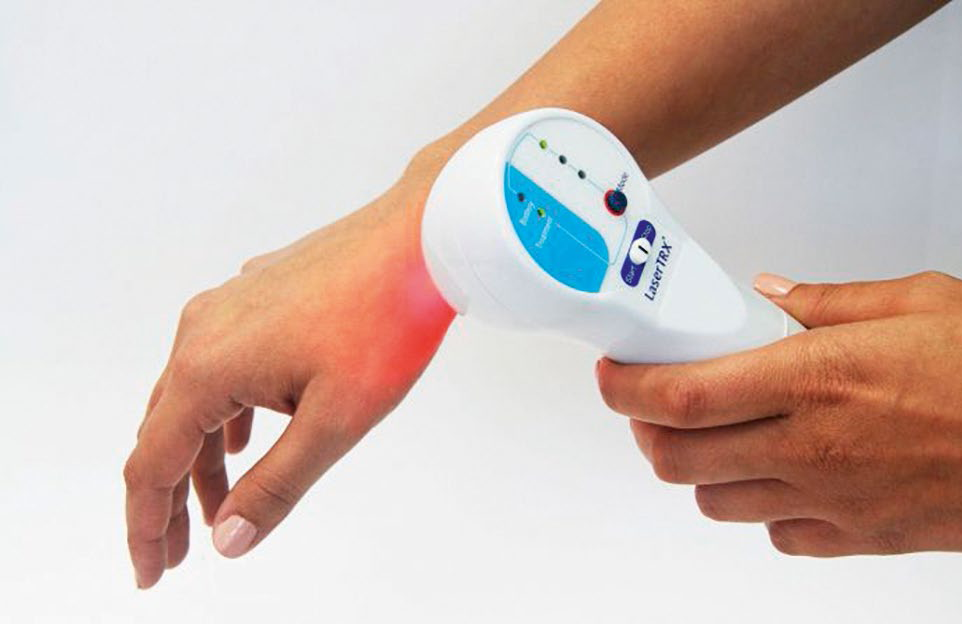
TeraQuant Pro - stacjonarny aparat do laseroterapii o niskiej mocy, wykorzystujący diody laserowe i światłowody, umożliwiający przeprowadzenie terapii na większej powierzchni ciała.
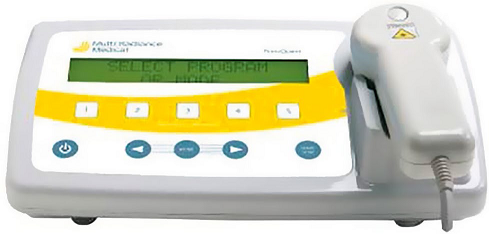
Lumix Superpulsed – aparat do laseroterapii o niskiej mocy, wykorzystujący technologię Superpulsed, która pozwala na precyzyjne i skuteczne aplikowanie promieniowania laserowego na wybrane obszary skóry.
PowerLaser Pro 500 - ręczny aparat do laseroterapii o niskiej mocy, wykorzystujący diody laserowe o różnej długości fali, umożliwiający precyzyjną aplikację promieniowania laserowego na wybrane obszary skóry.

Laseroterapia wysokoenergetyczna
Lasery dużej mocy stosuje się w medycynie nie tylko w fizykoterapii, ale też w leczeniu chorób nowotworowych i w chirurgii tkanek miękkich. Lasery stosowane w chirurgii mogą osiągać moc do kilkuset watów. Lasery dużej mocy stosowane w fizjoterapii, tj. w laseroterapii wysokoenergetycznej (HILT - High Intensity Laser Therapy) mają zwykle moc od kilku do kilkudziesięciu watów (na ogół w zakresie 5 - 30 watów). To jedna z najnowocześniejszych metod terapii laserowej. Polega na stosowaniu krótkich, powtarzalnych impulsów światła laserowego, aby wysokie dawki energii oddawanej do tkanek stymulowały procesy biologiczne.
Wpływa to na poprawę krążenia krwi, stymulację produkcji kolagenu, redukcję stanów zapalnych i przyspieszenie gojenia się tkanek. Metoda jest stosowana w leczeniu wielu schorzeń ortopedycznych, neurologicznych i reumatologicznych, takich jak bóle kręgosłupa, dyskopatia, zapalenie stawów, bóle mięśni i więzadeł, rwa kulszowa, neuralgia trójdzielna, łokieć tenisisty, zapalenie stawów skroniowo-żuchwowych i inne. Wskazania do stosowania laseroterapii HILT obejmują również przypadki przewlekłych i uporczywych bólów, które nie ustępują po innych metodach leczenia, a także urazy sportowe, zaburzenia ukrwienia i obrzęki tkanek miękkich. W laseroterapii HILT zazwyczaj stosuje się lasery na podczerwień o długości fali 810 nm, 904 nm, 980 nm lub 1 064 nm. Wiązka promieni podczerwonych o dużej mocy powoduje skuteczne wprowadzenie energii fotonów do głębokich tkanek przy jednoczesnym podgrzaniu tkanek do temperatury 40 - 45°C, co sprzyja przyspieszeniu procesów metabolicznych i regeneracyjnych6,7.
Oferta rynkowa aparatów do laseroterapii wysokoenergetycznej jest bardzo bogata. Oto kilka przykładowych aparatów:
MLS Laser - stacjonarny aparat do laseroterapii wysokoenergetycznej, wykorzystujący technologię Multiwave Locked System, która umożliwia aplikację równoczesnego promieniowania dwóch fal laserowych o różnej długości fali, generowanej zarówno w trybie ciągłym jak i impulsowym.
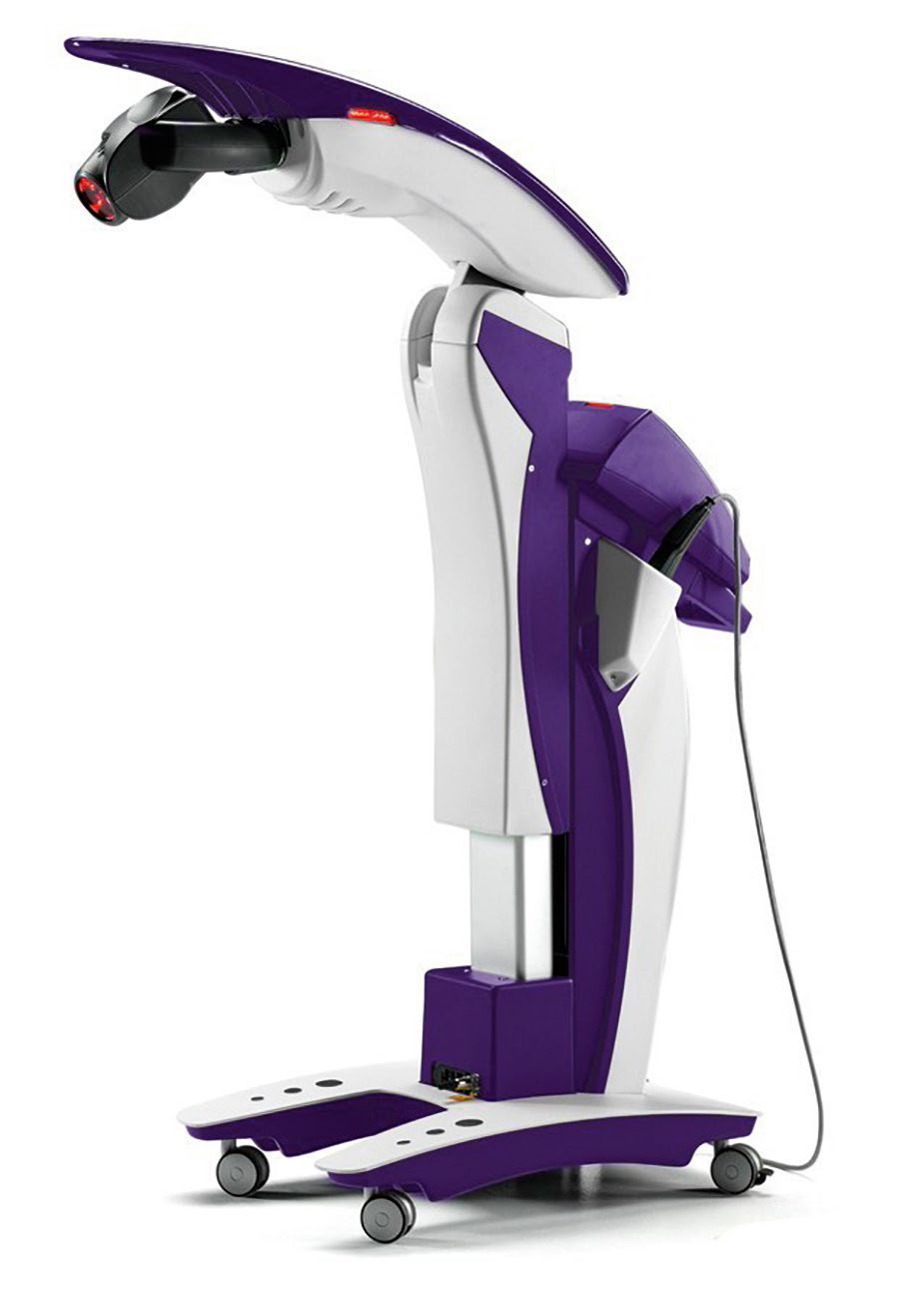
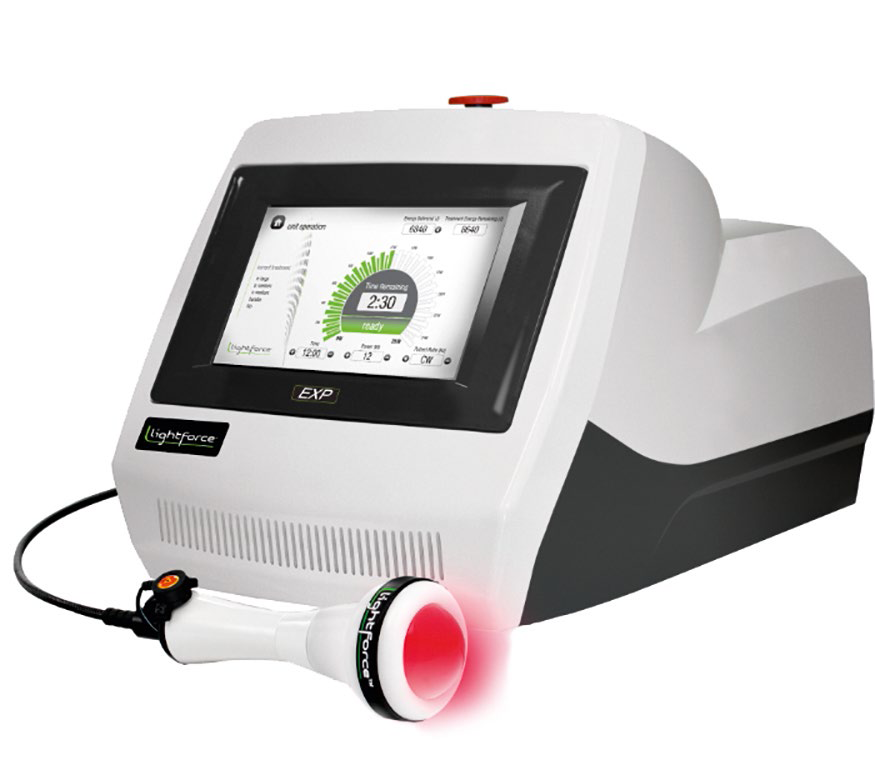
LightForce EXP - ręczny aparat do laseroterapii wysokoenergetycznej, umożliwiający precyzyjną aplikację promieniowania laserowego o dużej mocy na wybrane obszary ciała.
K-Laser Cube 4 - stacjonarny aparat do laseroterapii wysokoenergetycznej, wykorzystujący technologię Klaser, która umożliwia aplikację promieniowania laserowego o dużej mocy i wysokiej skuteczności. K-Laser Cube to wysokiej klasy najmocniejsze lasery wysokoenergetyczne na rynku, cenione na całym świecie. Model K-Laser Cube 4 oferuje moc do 15 Watt w pracy ciągłej oraz do 20 Watt w unikatowym trybie ISP. Cztery długości fal: 660 nm, 800 nm, 905 nm i 970 nm pozwalają zoptymalizować zabieg w zależności od jednostki chorobowej. Ponadto K-Laser Cube oferuje trzy tryby pracy: ciągły, impulsowy oraz tryb ISP (Intense Super Pulse – praca impulsowa w tym samym zakresie częstotliwości z automatyczną regulacją szerokości impulsu do osiągnięcia znacznie wyższej żądanej mocy średniej.
K-Laser Cube posiada również unikalną możliwość dopasowywania parametrów zabiegu laseroterapii wysokoenergetycznej do cech pacjenta. Oprócz analizy grubości tkanki tłuszczowej, morfologii ciała i rodzajów tkanek, bierze również pod uwagę inny kluczowy czynnik dla naszej skóry: melaninę. Dzięki swoim innowacyjnym parametrom, laser rozpoznaje sześć fototypów skóry, biorąc pod uwagę wszystkie ustawione wcześniej parametry.
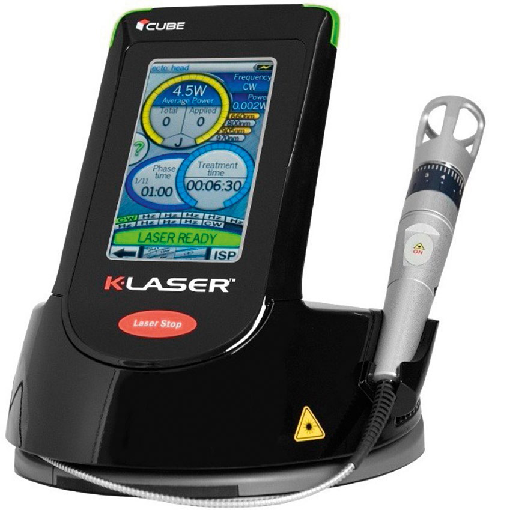
Dzięki wbudowanemu akumulatorowi, niewielkich rozmiarach i wadze (ok. 1,3 kg) laser wysokoenergetyczny K-Laser Cube 4 jest aparatem przenośnym. Transport aparatu ułatwia również zintegrowany uchwyt. Fizjoterapeuta może wybrać miejsce przeprowadzenia zabiegu, dlatego K-Laser Cube 4 jest idealnym narzędziem w dziedzinie medycyny sportowej, fizjoterapii i rehabilitacji.
BTL-6000 High Intensity Laser - stacjonarny aparat do laseroterapii wysokoenergetycznej, umożliwiający precyzyjną aplikację promieniowania laserowego o dużej mocy na wybrane obszary ciała.

Inne rodzaje laseroterapii
Wymieniliśmy jeszcze dwa rodzaje laseroterapii, nie wchodzących bezpośrednio w zakres fizjoterapii, ale dotyczących dziedzin bliskich zainteresowaniom fizjoterapeuty.
Laseroterapia frakcyjna
Laseroterapia frakcyjna FLT (Fractional Laser Therapy) jest metodą stosowaną w medycynie estetycznej oraz dermatologii do poprawy wyglądu skóry oraz leczenia różnych chorób skórnych. Polega na aplikacji wiązki lasera w sposób frakcyjny, czyli zostawianie niewielkich, pionowych kanałów w skórze. Zatem działaniu lasera poddaje się tylko ułamek (frakcję) powierzchni leczonej skóry, powodując mikroskopijne strefy uszkodzeń, między którymi znajdują się obszary nienaruszonej skóry. Jest to metoda frakcyjnej fototermolizy, w której uszkodzenie termiczne inicjuje kaskadę procesów prowadzących do przyspieszenia gojenia obszarów nieleczonych przez nabłonkowanie.
Dzięki temu skóra staje się jędrniejsza, bardziej elastyczna, a zmarszczki i blizny są mniej widoczne.
Laseroterapia frakcyjna FLT może być stosowana do leczenia wielu schorzeń skórnych, takich jak blizny potrądzikowe, zmarszczki, przebarwienia, nierówności skóry oraz rozstępy. Zabieg może być nieco bolesny, ale zazwyczaj nie wymaga znieczulenia ogólnego. Po zabiegu może wystąpić lekkie zaczerwienienie, obrzęk i łuszczenie się skóry, ale są to objawy tymczasowe i zazwyczaj ustępują w ciągu kilku dni.
Zatem laseroterapia frakcyjna FLT jest skuteczną metodą leczenia wielu schorzeń skórnych, a jej korzyści wynikają z minimalnej inwazyjności, skróconego czasu gojenia i zmniejszonego ryzyka powikłań. Istnieje bogate piśmiennictwo naukowe dotyczące laseroterapii frakcyjnej. Kilka ważnych artykułów polecamy w bibliografii8÷15.
Na rynku jest wiele aparatów do laseroterapii frakcyjnej. Oto kilka z nich:
Fraxel - to jedna z najpopularniejszych marek aparatów do laseroterapii frakcyjnej FLT. Fraxel działa na promieniowanie o długości fali 1 550 nm lub 1 927 nm, co pozwala na precyzyjne naświetlenie wybranych obszarów skóry.
Palomar Lux 1540 - działa na promieniowanie o długości fali 1 540 nm, co pozwala na precyzyjne naświetlenie obszarów skóry, które wymagają leczenia.
Lumenis AcuPulse - oferuje wiele różnych programów leczenia. Działa na promieniowanie o długości fali 2 940 nm lub 10 600 nm, co pozwala na precyzyjne naświetlenie wybranych obszarów skóry.
Alma Pixel - oferuje wiele różnych trybów pracy, w zależności od potrzeb pacjenta. Działa na promieniowanie o długości fali 2 940 nm lub 10 600 nm, co pozwala na precyzyjne naświetlenie obszarów skóry, które wymagają leczenia.
Syneron-Candela CO2RE - wykorzystuje promieniowanie o długości fali 10 600 nm, co pozwala na precyzyjne naświetlenie wybranych obszarów skóry. Oferuje wiele różnych programów leczenia, w zależności od specyfiki zabiegu.
Laseroterapia fotodynamiczna
Laseroterapia fotodynamiczna (PDT -Photodynamic Therapy) wykorzystuje fotosensybilizatory i unikalną cechę laserów, jaką jest selektywność, tj. pochłanianie promieni lasera przez wybrane chromofory, np. hemoglobinę we krwi, z ominięciem pozostałych struktur. Jeśli wprowadzimy do skóry jakiś barwnik (chromofor) i naświetlimy odpowiednią wiązką światła laserowego, to możemy poddawać terapii wybrane fragmenty skóry.
Zatem mechanizm działania PDT opiera się na wprowadzeniu do organizmu fotosensybilizatora (doustnie lub w postaci aplikacji na skórę), który jest selektywnie absorbowany przez patologiczne tkanki. Następnie na te tkanki jest skierowane promieniowanie lasera, co powoduje aktywację fotosensybilizatora i wyzwolenie reakcji fotodynamicznej. W wyniku tych reakcji dochodzi do tworzenia reaktywnych form tlenu, co prowadzi do uszkodzenia błon komórkowych i degradacji patologicznych tkanek.
Laseroterapia fotodynamiczna znajduje zastosowanie w leczeniu nowotworów skóry, a także w leczeniu chorób skóry, takich jak trądzik różowaty czy łuszczyca. W przypadku nowotworów skóry, metoda ta pozwala na wybiórcze niszczenie patologicznych komórek, minimalizując szkody dla zdrowych tkanek.
Jednym z najważniejszych aspektów przy zastosowaniu PDT jest odpowiedni dobór fotosensybilizatora oraz długości fali lasera, które powinny być dopasowane do rodzaju i lokalizacji choroby. Ponadto, PDT jest zazwyczaj przeprowadzana w kilku sesjach, aby osiągnąć najlepsze efekty. W leczeniu chorób skóry, takich jak trądzik, łuszczyca i brodawki najczęściej stosuje się aparaty z laserem diodowym o długości fali 630 – 690 nm. Nazwa laser diodowy w tym przypadku jest określeniem marketingowym, gdyż źródłem światła jest dioda LED, która nie jest laserem. Przykładami takich aparatów są: Omnilux Revive i Aktilite CL 128. Z bogatego piśmiennictwa naukowego na temat terapii PDT do najważniejszych artykułów można zaliczyć pozycje16÷25 w Bibliografii.
- Chung H, Dai T, Sharma SK, et al. The nuts and bolts of low-level laser (light) therapy. Ann Biomed Eng. 2012;40(2):516-533. doi:10.1007/s10439-011-0454-7
- Huang YY, Chen AC, Carroll JD, Hamblin MR. Biphasic dose response in low level light therapy. Dose Response. 2009;7(4):358-383. doi:10.2203/dose-response.09-027.Hamblin
- Avci P, Gupta A, Sadasivam M, et al. Low-level laser (light) therapy (LLLT) in skin: stimulating, healing, restoring. Semin Cutan Med Surg. 2013;32(1):41-52.
- Schindl A, Schindl M, Pernerstorfer-Schön H, Schindl L. Low-intensity laser therapy: a review. J Investig Med. 2000;48(5):312-326.
- Ferraresi C, Kaippert B, Avci P, et al. Low-level laser (light) therapy increases mitochondrial membrane potential and ATP synthesis in C2C12 myotubes with a peak response at 3-6 h. Photochem Photobiol. 2015;91(2):411-416. doi:10.1111/php.12410
- Toma RL, Tucci HT, Antônio EL, et al. Effects of high-intensity laser therapy on pain, muscle strength, and functional capacity in patients with knee osteoarthritis: a randomized controlled trial. Lasers Med Sci. 2017;32(3):795-803. doi:10.1007/s10103-017-2181-0
- Vale RG, de Oliveira RD, Pernambuco CS, et al. Can high-intensity laser therapy enhance functional performance in the elderly? A randomized controlled trial. Lasers Med Sci. 2013;28(3):973-982. doi:10.1007/s10103-012-1124-6
- Hantash BM, Bedi VP, Kapadia B, et al. In vivo histological evaluation of a novel ablative fractional resurfacing device. Lasers Surg Med. 2007;39(2):96-107. doi:10.1002/lsm.20438
- Hantash BM, Ubeid AA, Chang H, Kafi R, Renton B. Biphasic response of fractional laser-treated skin to solar simulated radiation. Lasers Surg Med. 2009;41(2):114-118. doi:10.1002/lsm.20750
- Laubach HJ, Tannous Z, Anderson RR, Manstein D. Skin responses to fractional photothermolysis. Lasers Surg Med. 2006;38(2):142-149. doi:10.1002/lsm.20223
- Lee WR, Shen SC, Al-Suwayeh SA, Yang HH, Yuan CY, Fang JY. Fractional photothermolysis for the treatment of acne scars: a report of 27 Asian patients. J Cosmet Laser Ther. 2010;12(5):226-231. doi:10.3109/14764171003729536
- Paasch U, Haedersdal M. Laser systems for ablative fractional resurfacing. Expert Rev Med Devices. 2011;8(1):67-83. doi:10.1586/erd.10.50
- Raulin C, Greve B, Grema H. IPL technology: a review. Lasers Surg Med. 2003;32(2):78-87. doi:10.1002/lsm.10118
- Tierney EP, Hanke CW. Review of the literature: fractional photothermolysis for the treatment of acne scarring. Dermatol Surg. 2009;35(9):1445-1461. doi:10.1111/j.1524-4725.2009.01257.x
- Weiss ET, Chapas AM, Brightman LA, et al. Successful treatment of atrophic postoperative and traumatic scarring with carbon dioxide ablative fractional resurfacing: quantitative volumetric scar improvement. Arch Dermatol. 2010;146(2):133-140. doi:10.1001/archdermatol.2009.331
- Dougherty TJ, Gomer CJ, Henderson BW, et al. Photodynamic therapy. J Natl Cancer Inst. 1998;90(12):889-905. doi:10.1093/jnci/90.12.889
- Castano AP, Mroz P, Hamblin MR. Photodynamic therapy and anti-tumour immunity. Nat Rev Cancer. 2006;6(7):535-545. doi:10.1038/nrc1894
- Hopper C. Photodynamic therapy: a clinical reality in the treatment of cancer. Lancet Oncol. 2000;1:212-219. doi: 10.1016/S1470-2045(00)00110-8
- Allison RR, Moghissi K. Photodynamic therapy (PDT): PDT mechanisms. Clin Endosc. 2013;46(1):24- 29. doi:10.5946/ce.2013.46.1.24
- Kim MM, Parmeswaran Diagaradjane AP, Pogue BW, Hasan T. Emerging technologies in cancer imaging and point-of-care diagnostics. Technol Cancer Res Treat. 2006;5(4):347-356. doi:10.1177/153303460600500405
- Nowis D, Makowski M, Stokłosa T, Legat M, Issat T, Gołąb J. Direct tumor damage mechanisms of photodynamic therapy. Acta Biochim Pol. 2005;52(2):339-352.
- Agostinis P, Berg K, Cengel KA, et al. Photodynamic therapy of cancer: an update. CA Cancer J Clin. 2011;61(4):250-281. doi:10.3322/caac.20114
- Lovell JF, Liu TWB, Chen J, Zheng G. Activatable photosensitizers for imaging and therapy. Chem Rev. 2010;110(5):2839-2857. doi:10.1021/cr900300p
- Chen B, Pogue BW, Hoopes PJ, Hasan T. Combining vascular and cellular targeting regimens enhances the efficacy of photodynamic therapy. Int J Radiat Oncol Biol Phys. 2005;61(4):1216-1226. doi:10.1016/j.ijrobp.2004.12.019
- O’Connor AE, Gallagher WM, Byrne AT. Porphyrin and nonporphyrin photosensitizers in oncology: preclinical and clinical advances in photodynamic therapy. Photochem Photobiol. 2009;85(5):1053- 1074. doi:10.1111/j.1751-1097.2009.00597