Znaczenia stanu zapalnego nie można zredukować tylko do reakcji na infekcje patogenne, powinien on być postrzegany raczej jako odpowiedź organizmu na ostre i przewlekłe uszkodzenie tkanki. Z tej perspektywy jest on nieodzowną częścią procesów naprawczych, a więc jest zaangażowany praktycznie we wszystkie fazy procesów gojenia i regeneracji20. Dlatego należy ponownie przemyśleć klasyczne postrzeganie zapalenia jako negatywnego zjawiska, uwzględniając jego rolę w kontekście procesów gojenia i regeneracji tkanek. Szczególnie w początkowej fazie procesów regeneracji po uszkodzeniach i urazach tkanek stan zapalny jest wyzwalaczem, który inicjuje regulowany proces powrotu do zdrowia i sprawności, a następnie kontynuuje jego przebieg.
Procesy zapalne podlegają złożonej reakcji, która w dużej mierze zależy od stanu układu odpornościowego, dlatego we wszystkich procesach gojenia i regeneracji należy brać pod uwagę aspekty immunomodulacyjne. Stany zapalne w kontekście procesów regeneracyjnych zwykle ustępują samoistnie. Samoograniczenie jest niezbędnym warunkiem pozytywnego wpływu stanu zapalnego wywołanego uszkodzeniem10. Poniżej zaprezentowano, jaki jest jego udział w regeneracji różnych tkanek układu mięśniowo-szkieletowego, zwłaszcza w odniesieniu do mięśni szkieletowych i ścięgien, omówiono także wpływ na więzadła, kości i chrząstkę.
Gojenie się mięśni
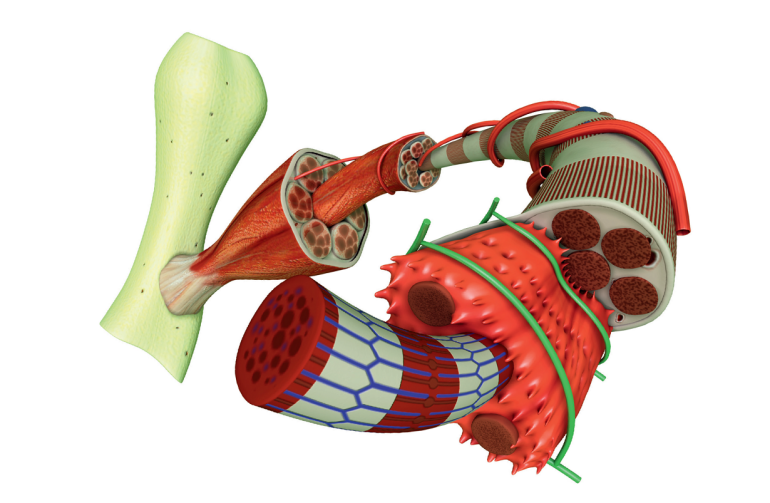
Gojenie się mięśni jest złożonym zjawiskiem wymagającym nie tylko wielu procesów komórkowych obejmujących tworzenie się i naprawę włókien mięśniowych, wzrost nowych naczyń krwionośnych (neoangiogenezę) i odbudowę macierzy zewnątrzkomórkowej (ECM), która jest ważna dla funkcjonowania mięśni, lecz także ponownego unerwienia zregenerowanych włókien mięśniowych. Wspomniane procesy komórkowe są złożone i muszą być ze sobą skoordynowane. Układ odpornościowy z różnymi komórkami odpornościowymi (tabela) ma kluczowe znaczenie w regulacji tych procesów i wywiera znaczny wpływ na odbudowę strukturalną i funkcjonalną mięśni. Uszkodzenie mięśni prowadzi do powstania szczątków komórkowych i uwolnienia czynników wewnątrzkomórkowych, które w połączeniu z degranulacją lokalnych komórek tucznych prowadzą do aktywacji układu odpornościowego.
Aktywowane miejscowo komórki odpornościowe uwalniają cytokiny prozapalne, takie jak czynnik martwicy nowotworu alfa (TNF-α), interferon gamma (IFNg), interleukina-6 (IL-6) i interleukina-1 (IL-1)27. W rezultacie, począwszy od leukocytów, które są stałe w mięśniach, i imigrujących leukocytów6,9 w ciągu pierwszych 24 godzin po uszkodzeniu mięśnia dochodzi do wstępnej fazy procesu zapalnego, który, zainicjowany przez neutrofile i uwalniane przez nie cytokiny, prowadzi do migracji i aktywacji makrofagów, usuwających uszkodzoną tkankę.
Ponadto w ciągu pierwszych 48 godzin w mięśniu aktywowane są komórki satelitarne, co doprowadza do początkowego nasilenia proliferacji. W tym okresie cytokina prozapalna IFNg jest odpowiedzialna za podtrzymanie proliferacji i hamowanie różnicowania się komórek satelitarnych21. W początkowej fazie zapalnej cytokiny prozapalne odpowiedzialne są za różnicowanie się w kierunku makrofagów o wysokiej aktywności fagocytarnej (makrofagi M1), które „oczyszczają” uszkodzony obszar, przygotowując w ten sposób środowisko do tworzenia i naprawy włókien mięśniowych. Ponadto makrofagi M1 w interakcji z innymi lokalnymi komórkami tworzą cytokiny, takie jak IL-6, które są odpowiedzialne za początkową aktywację komórek satelitarnych i dokonują ekspresji indukowanej syntazy tlenku azotu (iNOS), która powoduje apoptozę uszkodzonych komórek poprzez tworzenie tlenku azotu, a tym samym przyczynia się do usuwania uszkodzonego materiału