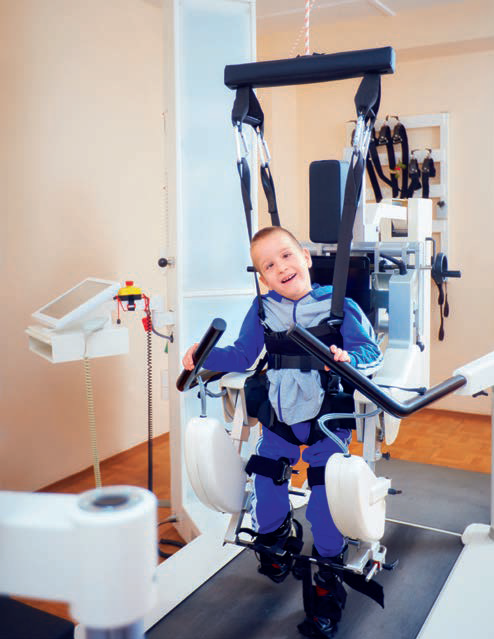
Chód jest jedną z najpotrzebniejszych czynności życia codziennego. Pozwala nam na przemieszczanie się w konkretnym celu. Jest ważnym aspektem funkcjonowania społecznego. Mobilizuje organizm, zapewniając warunki pracy mięśniom oraz układowi krążeniowemu i oddechowemu.
Utrata zdolności chodu w wyniku choroby wiąże się z ciężką niepełnosprawnością i zależnością od osób trzecich. Dlatego jednym z głównych celów rehabilitacji jest przywrócenie funkcji chodu. Mogą służyć temu różne pomoce techniczne, takie jak roboty wspomagające rehabilitację chodu i egzoszkielety.
Jednak chód ma jeszcze szersze znaczenie w fizjoterapii. Stanowi on podstawę kilku metod terapeutycznych, które wykorzystują wzorce chodu w celach diagnostycznych i opierają na nim postępowanie usprawniające.
Opisujemy dwie metody silnie związane w zupełnie inny sposób z chodem – PNF i kinezjologię stosowaną. Przyjrzymy się także możliwościom zastosowania robotów i egzoszkieletu w rehabilitacji pacjentów neurologicznych.
Czym jest metoda PNF?
Metoda PNF w kontekście torowania chodu Metoda PNF, czyli proprioceptywnego torowania nerwowo-mięśniowego (proprioceptive neuromuscular facilitation) powstała w 1946 roku w Kalifornii dzięki staraniom Hermana Kabata i Maggie Knott1.
Jest to metoda oparta na dogłębnej wiedzy z zakresu neurofizjologii, a w szczególności neurofizjologii układu ruchowego. W wielu aspektach odnosi się ona do wzorców rozwojowych układu nerwowego w odniesieniu do funkcji ruchu, starając się odnaleźć właściwy poziom wyjściowy, na którym należy rozpocząć pracę z pacjentem.
Bazując na prawidłowym rozwoju, prawidłowych wzorcach ruchowych i fizjologii układu nerwowego, stara się zmobilizować potencjał pacjenta, u którego działanie układu nerwowego zostało zaburzone.
W związku z tym oferta terapeutyczna PNF skierowana jest do pacjentów neurologicznych z różnego rodzaju schorzeniami i na różnym poziomie funkcjonowania: pacjentów poudarowych, z urazami czaszkowo-mózgowymi, uszkodzeniami rdzenia kręgowego, chorobami neurodegeneracyjnymi itd.
Pomimo że metoda PNF w dużej mierze odwołuje się do naturalnych wzorców zdrowego układu nerwowego, nie jest oparta jedynie na odruchach. Wymaga aktywnego uczestnictwa pacjenta, w związku z tym nie nadaje się dla pacjentów znajdujących się w śpiączce, w stanie wegetatywnym czy też z bardzo ograniczonymi możliwościami poznawczymi i komunikacyjnymi.
Tym niemniej elementy metody PNF stosowane są u pacjentów nawet w bardzo ciężkim stanie, także na oddziałach intensywnej opieki medycznej. Jednak takiego postępowania nie należy nazywać metodą PNF, a jedynie wykorzystaniem pewnych jej zasad i wzorców, czyniących rehabilitację bardziej funkcjonalną.
Metoda PNF znalazła zastosowanie także w innych obszarach rehabilitacji pacjentów. Już po ukończeniu kursu podstawowego można uczestniczyć w zajęciach na temat stosowania PNF w ortopedii, pediatrii, leczeniu skolioz czy: PNF i terapia manualna.
Są to dodatkowe specjalizacje, niejako niezależne od głównego nurtu kształcenia, przenoszące pewne aspekty metody na inne płaszczyzny, wydawałoby się pozaneurologiczne. Jednak to oddalenie się od neurologii jest pozorne.
We wszystkich dysfunkcjach – czy to ortopedycznych, czy pediatrycznych – cały czas mamy do czynienia ze sterowaniem ruchem ciała przez ośrodkowy układ nerwowy. Niezmienione zostają także zasady prowadzenia terapii, stosowane techniki, filozofia pracy oraz wzorce ruchowe oparte na chodzie. Elementy te omówimy pokrótce poniżej, szczególną uwagę zwracając na znaczenie chodu w koncepcji PNF.
Zasady prowadzenia terapii PNF
Koncepcja PNF wykorzystuje kilka kluczowych zasad terapeutycznych, których suma po części definiuje tę metodę i odróżnia ją od innych. Są to:
- Stosowanie adekwatnego oporu: opór ma za zadanie ułatwienie wykonania ruchu. Stanowi informację dla układu nerwowego, w jaki sposób, z jaką siłą i w jakim kierunku powinien zostać poprowadzony ruch. Opór wymusza także pożądany rodzaj skurczu i uczy kontroli ruchu. Może także wzmacniać mięśnie.
- Irradiacja i wzmocnienie: polega na wykorzystaniu wiedzy o synergistach ruchu angażowanych w różnych pozycjach wyjściowych i różnych warunkach. Dzięki irradiacji można zaangażować inne grupy mięśniowe celem wzmocnienia konkretnej grupy wykonującej określony ruch. Z kolei dzięki irradiacji można oddziaływać pośrednio na te mięśnie, które nie reagują lub słabo reagują na stymulację bezpośrednią.
- Zastosowanie bodźców czuciowych: aplikowanie bodźców czuciowych w określony sposób pozwala bardziej precyzyjnie torować określony ruch i funkcję.
- Komendy słowne i informacja wzrokowa: PNF korzysta z wielu kanałów dopływu informacji, aby wzmocnić oddziaływanie. Komendy wydawane są tonem, który toruje skurcz lub rozluźnienie. Ważny jest także rytm, który może być nadawany głosem. Informacja wzrokowa może stanowić pomoc w wykonaniu zadania, a jej usunięcie jest elementem progresji stopnia trudności.
- Trakcja i aproksymacja: są to metody oddziaływania na receptory, pozwalające we właściwy sposób torować funkcjonowanie układu nerwowego.
- Rozciągnięcie: wstępne rozciągnięcie aktywizuje taśmę mięśniową i ułatwia wykonanie ruchu w określonym wzorcu.
- Kolejność ruchu: z reguły jest on inicjowany od komponenty dystalnej – po ustabilizowaniu segmentu ciała, na którym ruch się odbywa. Istnieje jednak możliwość wyizolowania poszczególnych aspektów wzorca ruchowego i zmiany typowej kolejności ruchu.
- Wzorce ruchowe: są to funkcjonalne ruchy czynnościowe zachodzące w diagonalnych, oparte na wzorcu chodu. Zagadnieniu temu poświęcimy więcej miejsca w dalszej części artykułu.
Techniki w metodzie PNF
Głównymi technikami wykorzystywanymi w metodzie PNF są:
- Rytmiczne zapoczątkowanie ruchu: polega na specyficznej sekwencji ćwiczenia i opanowywania przez pacjenta danego ruchu. Początkowo ruch jest wykonywany biernie przez terapeutę, następnie prowadzony (wykonywany w sposób wspomagany), w kolejnej fazie jest przeprowadzany przeciwko oporowi, aby na końcu pacjent wykonał go czynnie – samodzielnie. Każda faza stanowi inny etap uczenia się pacjenta, daje możliwości innego rodzaju korekcji i ćwiczy kontrolę układu nerwowego nad wykonywanym ruchem, uwzględniając inne aspekty i wyzwania, jakim musi sprostać pacjent.
- Zwrotność agonistów: praca mięśniowa wykonywana jest od zakresu, w którym pacjent jest najsilniejszy i/lub który najlepiej kontroluje. Następnie wykonuje ruch koncentryczny przeciwko adekwatnie zaadaptowanemu oporowi, docierając do ustalonej pozycji końcowej. Stamtąd w sposób ekscentryczny sprowadzany jest ponownie do pozycji początkowej.
- Zwrotność antagonistów: technika ta bardzo dobrze odwzorowuje wymagania dnia codziennego, kiedy wykonywany jest ruch "w tę i z powrotem", np. podczas sięgania po coś, a dobra kontrola ruchu konieczna jest w obydwu kierunkach. Terapeuta ćwiczy z pacjentem ruch (zazwyczaj zaczynając od tego, który jest łatwiejszy dla pacjenta), a następnie w określonym obszarze – po podaniu komendy słownej, bez wprowadzania przerwy – wykonywany jest ruch przeciwko oporowi, w przeciwną stronę.
- Zwrotność stabilizacyjna: jest techniką pozwalającą wypracować stabilną pozycję pacjenta. Terapeuta aplikuje trójwymiarowy opór o wzrastającej stopniowo sile w określonych obszarach ciała (najczęściej po diagonalnej). Pacjent adaptuje się do oporu, tak aby nie zachodził przy nim widoczny ruch.
- Powtarzane rozciągnięcie: terapeuta rozpoczyna określony wzorzec ruchu od szybkiego rozciągnięcia napiętej taśmy mięśniowej. Następnie na przebiegu ruchu może aplikować kolejne rozciągnięcia, poprzedzając tę czynność komendą słowną – w ten sposób dochodzi do wzmocnienia skurczu wykonywanego przez pacjenta.
- Napnij – rozluźnij: pacjent wykonuje ruch do granicy ruchomości. Następnie wykonywany jest kilkusekundowy izometryczny skurcz agonistów, w wyniku którego dochodzi od odruchowego rozkurczu antagonistów. Pozwala to na bierne pogłębienie ruchu po odpowiednio długiej fazie rozkurczu. Technika służy głównie zwiększaniu zakresu ruchomości.
- Trzymaj – rozluźnij: jest to skurcz izometryczny przeciwko oporowi, mający na celu poprawę ruchomości lub łagodzenie objawów bólowych.
- Odtwarzanie: terapeuta wprowadza pacjenta w pozycję końcową, po czym aplikuje opór do skurczu izometrycznego wszystkich istotnych komponent uzyskanej pozycji. Po rozluźnieniu się pacjenta jest on biernie wyprowadzany o pewien zakres z pozycji końcowej. Jego zadaniem jest jak najbardziej precyzyjny i kontrolowany powrót do poprzedniej pozycji końcowej. Z każdym powtórzeniem zakres jest zwiększany. Na zakończenie pacjent samodzielnie odtwarza pozycję końcową, przebywając cały zakres ruchu. Ćwiczenie stanowi końcowy etap uczenia motorycznego, w którym pacjent musi opanować kontrolę nad ruchem oraz precyzyjnym położeniem w przestrzeni.
Znaczenie chodu w PNF
Jak już wspomnieliśmy chód ma szczególne znaczenie w koncepcji PNF. Swobodne przemieszczanie się jest istotnym, a czasami podstawowym celem wielu terapii, głównie u pacjentów neurologicznych, którzy w wyniku incydentu naczyniowego lub wypadku stracili tę zdolność, a także u pacjentów, których postępująca choroba neurologiczna stopniowo pozbawia możliwości chodzenia.
Wówczas celem terapii jest jak najdłuższe podtrzymanie tej zdolności. Wiele czynności przygotowuje pacjenta do chodzenia, zanim stanie on na nogi. Trening rozpoczyna się często w pozycji leżącej, w której ćwiczone są wzorce chodu.
Istotne jest, aby pacjent nie przebywał tylko w pozycji leżenia na plecach. Dlatego dużo miejsca poświęca się ćwiczeniom w leżeniu przodem w podporze na przedramionach czy też w leżeniu bokiem.
Do chodu przygotowywany jest też tułów. Jego odpowiednia praca: skracanie i rozciąganie oraz komponenta rotacyjna są niezwykle istotne dla możliwie poprawnej mechaniki chodu.
Niezwykle istotne jest również przygotowanie kończyn, do czego wykorzystywane są wzorce PNF, oparte głównie na funkcjonalnym chodzie. Z tego względu chód jest tak istotny w tej koncepcji.
Właściwie wszystkie pozostałe elementy pracy z pacjentem niejako nakładane są na wzorce chodu. Ćwiczenia zazwyczaj wykonuje się, rozpoczynając od pozycji niskich: w leżeniu, podporze, klęku, pozycji czworaczej itd.
Następnie przechodzi się do pozycji wyższych, np. ćwiczeń w siadzie, a w kolejnym etapie przechodzi się do stania i chodzenia. Chód ćwiczony jest nie tylko do przodu, lecz także w bok oraz do tyłu.
Duże znaczenie ma nauka odpowiedniego zabezpieczania się przed upadkiem oraz bezpiecznego sposobu upadania. Ważne jest także przećwiczenie różnych sytuacji, jakie czekają na pacjenta podczas chodu, np. omijanie przeszkód, pokonywanie schodów, niesienie torby, zatrzymanie się w celu otwarcia drzwi itd.
Trening chodu nie opiera się tylko na wyćwiczeniu siły mięśni i wytrzymałości, lecz musi być w pełni dostosowany do warunków, w jakich pacjent funkcjonuje. PNF wypracował narzędzia i metodologię pozwalającą w maksymalny sposób usprawnić wiele funkcji pacjentów, nawet po ciężkich urazach i chorobach. Jedną z najistotniejszych z tych funkcji jest chodzenie.
Wspomaganie rehabilitacji chodu po udarze
Rehabilitacja chodu z wykorzystaniem robota w podostrej fazie po udarze
W 2007 roku zostało opublikowane wieloośrodkowe badanie, przeprowadzone przez niemieckich uczonych, nad skutecznością zastosowania robotów we wspomaganiu rehabilitacji chodu u pacjentów w fazie podostrej po przebyciu udaru2.
Badanie prowadzono w 4 ośrodkach rehabilitacji poudarowej przez 21 miesięcy, było poprzedzone randomizacją oraz częściowo zaślepione (single-blind). Wymienione kryteria pozwalają uznać wyniki przytaczanego badania za wysoce wiarygodne.
Początkowo do badania włączono 170 osób po udarze przebytym w okresie ostatnich 6 miesięcy. Pacjenci wykazywali całkowitą niemożność chodzenia, wymagali pomocy jednego lub dwóch terapeutów oraz ortez i innego rodzaju zaopatrzenia w celu wspomaganego przemieszczania się. Możliwe było samodzielne siedzenie bez podparcia.
Pacjenci rozumieli instrukcje werbalne oraz byli wydolni i stabilni pod względem funkcji układu krążeniowego. Zostali oni przydzieleni do dwóch grup: A – badawczej (n = 77) i B – kontrolnej (n = 78).
Niezwykle istotne jest, aby chodzenie nie odbywało się dla samego chodzenia. Pacjent powinien mieć cel i motywację do jego osiągnięcia.
Grupa kontrolna (B) przez kolejnych 20 dni otrzymywała codziennie 45 minut terapii prowadzonej przez terapeutę – jej celem była głównie poprawa funkcji chodu. Grupa badawcza (A) otrzymywała terapię podzieloną, realizowaną również przez 20 codziennych sesji.
Pierwsze 20 minut poświęcone było na rehabilitację chodu za pomocą robota, natomiast pozostałe 25 minut – na pracę z terapeutą. Pacjent umieszczany był w robocie dzięki pomocy terapeutów. Następnie był odciążany (ćwiczenia przy 10–20% masy ciała) oraz stabilizowany uprzężą (szelkami).
Główną częścią urządzenia były dwie niezależne płyty pozwalające na symulowanie fazy podporu i przenoszenia. Długość kroku ustalono na 48 cm, natomiast kadencja była dobierana indywidualnie do komfortu pacjenta. Prędkość poruszania się za pomocą robota wynosiła od 1,4 do 1,8 km/h.
Analizie jakościowej i ilościowej poddawano wiele wskaźników funkcjonowania pacjentów, w tym:
- funkcjonalne przemieszczanie się na odległość 15 m, analizowane na podstawie nagrań wideo przez niezależnych ekspertów,
- wyniki na skali Barthel, dostarczającej informacji o stopniu niezależności w wykonywaniu czynności życia codziennego,
- prędkość chodu,
- wydolność podczas chodu,
- różne aspekty mobilności – od transferu w obrębie łóżka do całkowitej sprawności (za pomocą Indeksu Mobilności Rivermead (IMR)
- siłę kończyny oraz mobilność poszczególnych stawów (za pomocą Motricity Index).
Wyniki analizowane bezpośrednio po zakończeniu badania wykazały, że zdecydowanie więcej osób, w rehabilitacji których wykorzystano pomoc robota, było w stanie chodzić samodzielnie (grupa A = 53,2% vs. grupa B = 2,8%).
Podobna przewaga utrzymywała się także podczas kolejnego pomiaru kontrolnego przeprowadzonego po 6 miesiącach (grupa A = 70,1% vs. 35,9%). Uzyskane różnice były wysoce istotne statystycznie (p < 0,0001) na korzyść grupy z wykorzystaniem robota.
Również na skali Barthel wynik 75 punktów lub więcej (ze 100 możliwych do uzyskania) osiągnęło istotnie więcej pacjentów z grupy z użyciem robota (grupa A = 51,1%) niż z grupy kontrolnej (grupa B = 26,9%).
Po 6 miesiącach różnica statystyczna pomiędzy obydwoma grupami w liczbie osób, które osiągnęły wynik w skali Barthel równy lub wyższy niż 75, nie była istotna statystycznie (grupa A = 58,4% vs. grupa B = 46,2%).
Wszystkie pozostałe drugorzędowe wyniki poprawiły się w obydwu grupach, jednak w grupie wykorzystującej pomoc robota poprawa była istotnie wyższa. Szczególnie zauważalna była ona w odniesieniu do wydolności chodu. Poprawa utrzymała się również po 6 miesiącach od zakończenia badania.
Chociaż autorzy badania nie wykonali statystycznej analizy wyników bezpośrednio po terapii i 6 miesięcy później, przegląd przytoczonych w artykule wartości średnich wskazuje na interesującą tendencję: średnie wyniki bezpośrednio po zakończeniu terapii i 6 miesięcy później w grupie kontrolnej nieznacznie różnią się od siebie (z tendencją wzrostową), natomiast średnie wyniki w grupie badawczej zdają się nadal wzrastać w większym stopniu niż w grupie kontrolnej.
Wskazywałoby to nie tylko na trwałość efektu w grupie badawczej, lecz wypracowanie korzyści, która pozwalała na dalszy postęp w dłuższej perspektywie czasowej.
Należy jednak jasno stwierdzić, że jest to jedynie obserwacja oparta na przytoczonych średnich bez analizy statystycznej, w związku z czym postawiona hipoteza może być całkowicie błędna. Na podstawie analizy wyników można stwierdzić, że wykorzystanie robota jako rozwiązania wspomagającego klasyczną terapię chodu u pacjentów poudarowych w fazie podostrej jest skuteczne i przyczynia się do lepszego funkcjonowania pacjentów w życiu codziennym, w tym do poprawy samodzielnej zdolności przemieszczania się, a uzyskane wyniki są trwałe.
Kolejne badanie dotyczące wykorzystania robota w rehabilitacji chodu u osób w fazie podostrej po przebytym udarze zostało opublikowane przez Tonga w 2006 roku3. Badanie to było prowadzone w Hongkongu przez okres ponad roku. Do badania klasyfikowano pacjentów, u których epizod udaru niedokrwiennego lub krwotocznego miał miejsce w okresie nie dłuższym niż ostatnie 6 tygodni.
Kryteriami włączającymi były:
- brak zaburzeń poznawczych, które uniemożliwiłyby wykonywanie instrukcji,
- możliwość przebywania w pozycji stojącej przez co najmniej 1 minutę (samodzielnie lub z pomocą),
- istotne ubytki funkcji chodu oraz stabilność krążeniowo-oddechowa.
Różnego rodzaju powikłania oraz znaczące dla przebiegu badania choroby towarzyszące lub czynniki medyczne (np. wszczepiony rozrusznik serca) powodowały wykluczenie potencjalnego kandydata z uczestnictwa w badaniu.
Docelowo dopuszczono 50 pacjentów, z czego w analizie uwzględniono wyniki uzyskane od 46. Pacjenci zostali przydzieleni do trzech grup (grupa A, n = 16; grupa B, n = 15, grupa C, n = 15). Alokacja została przeprowadzona z uwzględnieniem randomizacji, jednak nie zastosowano zaślepienia, co zostało uzasadnione brakiem praktyczności takiego postępowania w opracowanym planie badawczym.
Grupa A stanowiła grupę kontrolną. Realizowano w niej konwencjonalną fizjoterapię opartą na koncepcji PNF oraz Bobath. Celem była poprawa postury oraz poprawa zdolności ruchowych, w tym głównie chodu.
Wykonywano ćwiczenia mające na celu stabilizację ciała, normalizację napięcia mięśniowego oraz poprawę funkcjonalną. Podczas każdej z 20 sesji, rozłożonych na okres 4 tygodni, realizowano po 30 minut treningu tułowia i kończyny górnej z terapeutą, 20 minut chodu oraz 10 minut ćwiczeń kończyny dolnej.
Grupa B była grupą, w której rehabilitację chodu wspomagano użyciem robota (electromechanical gait trainer). Również pacjenci z tej grupy podczas sesji terapeutycznej przez 30 minut uczestniczyli w zajęciach z wykorzystaniem metody PNF i Bobath.
10-minutowy trening kończyny dolnej był również realizowany w analogiczny sposób. Różnica polegała na zastąpieniu tradycyjnej rehabilitacji chodu wykorzystaniem robota przez 20 minut w ciągu każdej sesji. Robot pozwalał na odciążenie pacjenta oraz symulował symetryczny chód (60% fazy podparcia i 40% fazy przenoszenia).
Istniała również możliwość dostosowania długości kroku (od 34 do 48 cm) oraz prędkości chodu (od 0,2 do 0,6 m/s). Fizjoterapeuta mógł interweniować w trakcie treningu, korygować pacjenta oraz dostarczać mu adekwatnej pomocy.
Grupa C realizowała ten sam program, który przeznaczono dla grupy B (wykorzystanie robota do wspomagania rehabilitacji chodu), jednak dodatkowo stosowano elektrostymulację mięśni kończyny niedowładnej.
Jedna para elektrod została zamocowana nad mięśniem czworogłowym uda, który był poddawany stymulacji w fazie podporu w celu ułatwienia przyjmowania obciążenia. Druga para elektrod została umieszczona w okolicy nerwu strzałkowego wspólnego – celem stymulacji zgięcia grzbietowego stopy w fazie przenoszenia.
W celu sprawdzenia skuteczności oddziaływania wykorzystano różne narzędzia pomiarowe, w tym m.in. ocenę równowagi za pomocą skali BBS, zdolność przemieszczania się za pomocą skali FAC, poziom samodzielności za pomocą skali FIM, poziom funkcjonowania w zakresie czynności życia codziennego za pomocą skali Barthel, prędkość chodu na odległość 5 metrów oraz cechy sprawności kończyny za pomocą Motricity Index.
Początkowo porównano między sobą wyniki grupy A z połączonymi wynikami grup B i C celem sprawdzenia efektu zastosowania dodatkowej interwencji w porównaniu do standardowej fizjoterapii poudarowej.
Stwierdzono, że grupy, w których stosowano interwencje za pomocą robota, osiągały statystycznie istotnie wyższe wyniki w zakresie prędkości chodu, zdolności przemieszczania się (FAC) oraz sprawności kończyny (Motricity Index).
Nie stwierdzono natomiast różnicy w zakresie równowagi (BBS), funkcjonowania w czynnościach życia codziennego (skala Barthel) oraz poziomie samodzielności (FIM). Następnie porównano między sobą grupy B i C celem sprawdzenia skuteczności elektrostymulacji jako środka wspomagającego wykorzystanie robota w rehabilitacji chodu.
W tym przypadku nie stwierdzono istotnej różnicy między grupami w żadnej z przebadanych kategorii. Na podstawie przeprowadzonego badania można wysnuć wniosek, że zastosowanie robota jako uzupełnienia standardowej terapii chodu u pacjentów poudarowych w fazie podostrej jest skuteczne w odniesieniu do kategorii bezpośrednio związanych z samym chodem i zapewnia istotnie lepsze rezultaty niż rehabilitacja ograniczona do interwencji terapeuty.
Badanie nie wykazało przełożenia poprawy parametrów chodu na pozostałe aspekty funkcjonowania. Być może sytuacja ta związana była z dość wczesnym okresem przeprowadzenia badania, a deficyty pacjentów nie pozwoliły im zrobić bardziej funkcjonalnego użytku z poprawy funkcji chodu.
Dodatkowe zastosowanie elektrostymulacji w sposób opisany w badaniu oraz w opisanych warunkach nie wiązało się z lepszymi wynikami ocenianych parametrów.
Rehabilitacja chodu z wykorzystaniem robota w przewlekłej fazie po udarze
Szczególnie interesującym zagadnieniem jest możliwość poprawy funkcjonowania osób po przebytym stosunkowo dawno udarze mózgu. Powszechnie wiadomo bowiem, że największe możliwości odtworzenia funkcji oraz najbardziej wydajne procesy neuroplastyczności zachodzą w okresie wczesnej rehabilitacji.
Chociaż najnowsze odkrycia udowadniają, że czynienie postępów przez pacjentów nie jest ograniczone przez ramy czasowe – jeżeli zostanie im zapewnione odpowiednie wsparcie rehabilitacyjne – to powszechnie największe nadzieje wiąże się z wczesną fazą rehabilitacji poudarowej.
Ważne jest więc odniesienie się do konkretnych badań wykazujących zasadność i skuteczność rehabilitacji w fazie przewlekłej. Istotne jest również zagadnienie wspomagania rehabilitacji rozwiązaniami technicznymi.
Wiadomo bowiem, że robot mogący wyręczyć wysoko wykwalifikowaną kadrę medyczną jest w końcowym rozliczeniu bardziej ekonomiczny, a personel może zostać oddelegowany do pacjentów, którzy wymagają czynności, których rozwiązania techniczne nie są w stanie zastąpić.
Wolny chód w dużej mierze uniemożliwia korzystanie z niego w sytuacjach życia codziennego poza domem oraz jest niekorzystnym czynnikiem ograniczającym uczestnictwo w sytuacjach społecznych, w związku z czym doprowadza do znacznego ograniczenia jakości życia.
Obsługa robota wspomagającego rehabilitację chodu nie jest nadmiernie skomplikowana i wyczerpująca, co powoduje konieczność zaangażowania mniejszej liczby pracowników oraz personelu o innym stopniu kwalifikacji.
Badanie dotyczące zastosowania robota w rehabilitacji chodu w fazie przewlekłej po udarze mózgu zostało przeprowadzone przez zespół fińskich naukowców pod kierownictwem S.H. Peurali4.
W badaniu uczestniczyło 45 osób, które przebyły udar mózgu średnio 3 lata wcześniej. Autorzy zadbali o równą reprezentację liczbową osób z niedowładem lewostronnym i prawostronnym oraz po udarze niedokrwiennym i krwotocznym.
Większość pacjentów była w stanie poruszać się samodzielnie po płaskim terenie. Jedna osoba potrzebowała asysty dwóch pomocników, kilka osób potrzebowało pomocy jednego pomocnika; większość potrzebowała pomocy przy pokonywaniu schodów lub innych przeszkód w poruszaniu się.
Największym problemem była jednak bardzo mała prędkość chodzenia. Głównym celem badania było określenie możliwości poprawy prędkości chodu u pacjentów w fazie przewlekłej po udarze.
Aby ocenić taką możliwość, autorzy zdecydowali się na wykorzystanie kilku powszechnie znanych, standardowych narzędzi pomiarowych, m.in. wykonano 10-metrowy test chodu 10MWT (pomiar czasu konieczny na pokonanie tego dystansu), 6-minutowy test chodu 6MWT (całkowity dystans pokonywany w tym czasie) oraz zastosowano zmodyfikowaną skalę Ashwortha (MMAS). Przeprowadzono również badania równowagi i subiektywnego poziomu zmęczenia, jednak w dalszym opisie skupimy się głównie na wyznacznikach prędkości chodu.
Pacjenci zostali w randomizowany sposób przydzieleni do jednej z trzech grup:
- Grupa 1 otrzymywała klasyczny trening chodu, przeprowadzany przez fizjoterapeutę w wymiarze 20 minut dziennie przez 3 tygodnie (15 sesji).
- Grupa 2 poddawana była treningowi za pomocą robota wspomagającego rehabilitację chodu. Pacjent umieszczany był w urządzeniu z napędzanymi elektrycznie platformami na stopy oraz stabilizowany był za pomocą szelek. Istniała możliwość doboru parametrów chodu (w tym prędkości i kadencji kroków) jak również stopnia odciążenia. Starano się, aby odciążenie nie przekraczało 20% masy ciała i stopniowo zmniejszano je, wraz z obserwowaną progresją. Trening za pomocą robota realizowany był również w ciągu 15 sesji po 20 minut każda.
- Grupa 3 otrzymywała taki sam trening za pomocą robota, jaki realizowany był w grupie 2, jednak dodatkowo wykonywana była elektrostymulacja mięśni, wspomagająca chód zgodnie z indywidualnymi potrzebami pacjentów. Oprócz interwencji eksperymentalnych każdy pacjent poddawany był codziennej rehabilitacji poprawiającej ogólną sprawność, jednak nieingerującej w oceniane parametry chodu.
Zgodnie z uzyskanymi wynikami wszystkie trzy grupy znacząco poprawiły parametry prędkości chodu (10 MWT, p < 0,001; 6MWT, p < 0,01; MMAS, p < 0,001) oraz równowagi (p < 0,001). Długość przebytego dystansu podczas treningu chodu w czasie wszystkich sesji wynosiła łącznie średnio 6900 m w grupie 3, 6500 m w grupie 2 oraz 4800 m w grupie 1.
Istotna różnica w pokonanym dystansie dotyczyła jedynie grupy ćwiczącej z terapeutą oraz ćwiczącej za pomocą robota przy wykorzystaniu elektrostymulacji – na korzyść tej ostatniej. Na podstawie powyższego badania można wysnuć istotne wnioski.
Po pierwsze, pacjenci po przebytym dawno udarze stale wykazują potencjał poprawy zdolności motorycznych. Po drugie wyniki osiągane przy wykorzystaniu robota były tak samo dobre jak w przypadku pracy wykwalifikowanego personelu.
Po trzecie, dodatkowe zastosowanie elektrostymulacji pozwoliło pokonać pacjentom zdecydowanie większą odległość, co mogło przełożyć się na bardziej wydajny i/lub intensywny trening.
Rehabilitacja chodu po urazie rdzenia kręgowego
Wykorzystanie egzoszkieletu u pacjentów z urazem rdzenia kręgowego
Poziom niepełnosprawności w przypadku uszkodzenia rdzenia kręgowego jest głównie zdeterminowany wysokością urazu oraz stopniem naruszenia rdzenia (uszkodzenia całościowe i częściowe).
Szczególnie wysokie uszkodzenia, z całościowym przerwaniem ciągłości rdzenia, powodują olbrzymią niepełnosprawność oraz są przyczyną wtórnych do unieruchomienia problemów zdrowotnych. Dotyczą one ograniczonej wydolności krążeniowo-oddechowej, atrofii mięśniowej, bólu, ryzyka powstania odleżyn, a także występowania stanów depresyjnych lub w pełni rozwiniętej depresji.
Korzystanie z wózka inwalidzkiego jest rozwiązaniem częściowym, które uniemożliwia pełną pionizację pacjenta oraz daje możliwość ćwiczenia tylko określonych partii mięśniowych.
Wykorzystanie robota do treningu chodu jest dobrym rozwiązaniem, jednak tylko w pewnej części odpowiada na potrzeby pacjentów z uszkodzeniem rdzenia. Robot wspomagający rehabilitację chodu stosowany jest wówczas, gdy istnieje realna szansa na przywrócenie funkcji chodu (np. u pacjentów poudarowych) lub w sytuacji, w której choroba stopniowo pozbawia pacjenta możliwości chodzenia (np. w przypadku stwardnienia rozsianego). Nie sprawdza się on jednak jako trwałe rozwiązanie pomagające w chodzeniu.
Platformy, bieżnia i uprzęże mają za zadanie pomóc pacjentowi w odzyskaniu sprawności lub spowolnić proces jej utraty, natomiast nie przejmą funkcji chodu za pacjenta i nie umożliwią mu chociaż w częściowym stopniu chodzenia w warunkach poza ośrodkiem rehabilitacyjnym.
Aby odpowiedzieć na te specyficzne potrzeby pacjentów coraz częściej stosowane są ruchome ortezy sterowane przez pacjenta, nazywane egzoszkieletami. Pozwalają one na przemieszczanie się w ograniczonym zakresie, także w różnych warunkach otoczenia.
Bardziej zaawansowane modele pozwalają na generowanie kroku poprzez przemieszczanie ciężaru ciała przez pacjenta. W większości przypadków pacjenci spełniający kryteria posługiwania się egzoszkieletem mogą być w trakcie chodu samodzielni, tzn. nie potrzebują bezpośredniego wsparcia ze strony osób trzecich.
Autorzy w podsumowaniu stwierdzili, że cztery czynniki określały (prawie liniowo) prędkość poruszania się za pomocą egzoszkieletu. Były to: wiek, czas, który upłynął od uszkodzenia rdzenia kręgowego, poziom uszkodzenia i liczba sesji treningowych.
W 2015 roku zespół Dennisa R. Louie5 przeprowadził systematyczny przegląd piśmiennictwa dotyczącego zastosowania egzoszkieletu u osób z uszkodzeniem rdzenia kręgowego. Spośród 150 badań, wybranych po wstępnej selekcji, do końcowego przeglądu zakwalifikowano 15. Żadne badanie nie posiadało próby kontrolnej.
W omawianej grupie nie ma to jednak istotnego znaczenia, bowiem wyniki można określić jako zero-jedynkowe. Bardzo zróżnicowany był czas treningu i jego rodzaj. W niektórych przypadkach dążono jedynie do tego, aby pacjent zapoznał się z obsługą egzoszkieletu, w innych liczba sesji była dostosowana indywidualnie do potrzeb pacjenta, aby nauczył się on sprawnie chodzić w egzoszkielecie w różnych warunkach, na różnych powierzchniach i z możliwie dużą prędkością.
Jak wynika z powyższego opisu, badania zebrane w przeglądzie były bardzo zróżnicowane. Zastanawiające było, że starsi pacjenci byli w stanie osiągać większe prędkości niż młodsi. Najprawdopodobniej miało to związek z typem uszkodzenia (urazowy u młodszych osób) i poziomem urazu (wyższy u młodszych).
Rehabilitacja chodu z wykorzystaniem lokomatu w rehabilitacji pacjentów z częściowym uszkodzeniem rdzenia kręgowego
W 2013 roku grupa badawcza pod kierownictwem Any Esclarín-Ruz6 opublikowała artykuł podsumowujący wyniki wykorzystania robota służącego wspomaganiu rehabilitacji chodu typu lokomat u pacjentów z częściowym uszkodzeniem rdzenia kręgowego. Lokomat jest rodzajem sterowanej ortezy, umożliwiającej zautomatyzowany trening chodu na bieżni, z dostosowanym do potrzeb pacjenta stopniem odciążenia ciała.
W badaniu wzięło udział 88 osób, w równej liczbie z uszkodzeniami górnego i dolnego neuronu ruchowego. Następnie pacjenci w sposób losowy zostali przyporządkowani do jednego z dwóch warunków eksperymentalnych: konwencjonalnych ćwiczeń mobilności lub konwencjonalnych ćwiczeń mobilności oraz treningu wspomaganego robotem.
Każda sesja ćwiczeń konwencjonalnych trwała po 60 minut, podczas których realizowano program fizjoterapii obejmujący wzmacnianie obszarów powyżej poziomu uszkodzenia oraz mobilizację obszarów poniżej poziomu uszkodzenia.
Pracowano nad stabilizacją tułowia, ograniczeniem spastyczności, czynnościami samoobsługi oraz transferem. 30 minut każdej sesji poświęcono na tradycyjne formy rehabilitacji chodu z pomocą terapeuty. Program rehabilitacji obejmował 40 sesji w ciągu 8 tygodni.
Program usprawniania grupy eksperymentalnej był tożsamy w pierwszej części, która obejmowała 20 minut treningu ogólnego dla osób z urazem rdzenia kręgowego. Pozostałe 30 minut poświęcono na reedukację chodu za pomocą robota.
Do oceny wyników badacze posłużyli się kryteriami głównymi oraz drugorzędnymi.
- Główne
- osiągnięcia w chodzie na odległość 10 metrów (10MWT), czyli pomiar prędkości chodu,
- dystans przebyty w ciągu 6-minutowego testu chodu (6MWT).
- Drugi z wymienionych testów bada nie tylko przebyty dystans, lecz także wydolność pacjenta. Celem jest bowiem dobranie takiej prędkości oraz strategii poruszania się, aby pacjent był w stanie ukończyć test.
- Drugorzędne
- indeks chodu po urazie rdzenia kręgowego (WISCI II),
- skalę niezależności funkcjonalnej (FIM-L),
- ocenę siły kończyn dolnych (ASIA),
- skalę motoryczną kończyn dolnych (LEMS),
- subiektywne wrażenie zmiany, oceniane przez pacjenta (PGIC).
Wartości wymienionych powyżej skal nie będziemy poddawać interpretacji. Wszystkie grupy poprawiły swoje wyniki względem wartości wyjściowych. Dystans pokonywany w 6MWT był statystycznie większy w grupie ćwiczącej za pomocą lokomatu niż w grupie poddanej tylko terapii tradycyjnej.
W przypadku osób z uszkodzeniem górnego neuronu ruchowego wynosił on średnio 187,48 m vs. 119,41 m, natomiast przy uszkodzeniu dolnego neuronu ruchowego średnie odległości wynosiły odpowiednio 157,54 m vs. 145,62 m. Szczególnie dużą różnicę zaobserwowano w przypadku górnego neuronu ruchowego.
Istotne różnice zaobserwowano także w prędkości chodu, określanej w teście 10MWT. W tym przypadku najwyższą średnią odnotowano w grupie po uszkodzeniu górnego neuronu ruchowego, ćwiczącej z lokomatem (0,54 m/s), natomiast najniższą – w grupie po uszkodzeniu górnego neuronu ruchowego, ćwiczącej jedynie z terapeutą (0,39 m/s).
Z zaprezentowanych wyników można wywnioskować, że zastosowanie robota typu lokomat do usprawniania chodu pacjentów z częściowym uszkodzeniem rdzenia kręgowego jest skuteczniejsze niż sama rehabilitacja prowadzona siłami terapeuty.
Szczególnie istotna różnica na rzecz wykorzystania robota dotyczyła pacjentów z uszkodzeniem górnego neuronu ruchowego. Zastosowanie robota w omawianych przypadkach jest istotną wartością dodaną dla pacjentów po urazach rdzenia.
Rehabilitacja chodu w stwardnieniu rozsianym
Trening chodu z wykorzystaniem robota
Grupa włoskich naukowców pod kierownictwem Sofii Straudi7 przeprowadziła dwuośrodkowe, randomizowane badanie porównawcze z wykorzystaniem robota do usprawniania funkcji chodu. Do badania zakwalifikowano 40 osób w wielu powyżej 18 lat, z rozpoznanym stwardnieniem rozsianym o charakterze postępującym, którzy wykazywali poważne zaburzenia chodu.
Warunkiem uczestnictwa był:
- wystarczający poziom zdolności poznawczych,
- brak innych chorób neurologicznych,
- stabilny stan pacjenta,
- brak "mechanicznej niesprawności" (urazów, złamań itp.) w obszarze narządu ruchu, które uniemożliwiłyby uczestnictwo w badaniu.
Pacjenci zostali w sposób losowy przydzieleni do dwóch grup: porównawczej i eksperymentalnej. W grupie porównawczej przeprowadzano terapię ogólnousprawniającą trwającą 30 minut (podczas każdej sesji) oraz standardową terapię chodu, koordynacji i równowagi, dostosowaną do potrzeb pacjenta, trwającą również 30 minut.
W grupie eksperymentalnej również poświęcono 30 minut na trening ogólny, natomiast przez pozostałe 30 minut pacjent ćwiczył chód przy pomocy robota. Składał się on z bieżni oraz sterowanych ortez. Pacjent był stabilizowany za pomocą szelek.
Stopień odciążenia i prędkość chodu były dobierane do indywidualnych możliwości pacjenta i modyfikowane w trakcie przebiegu rehabilitacji. Wszyscy pacjenci z obydwu grup otrzymali 12 sesji w ciągu 6 tygodni.
W celu oceny postępu terapeutycznego zastosowano wiele wskaźników głównych i drugorzędnych.
Do najważniejszych wskaźników głównych należały:
- 10-metrowy test chodu mierzący prędkość,
- 6-minutowy test chodu sprawdzający wytrzymałość,
- test równowagi Berga,
- test "wstań i idź",
- pomiar jakości życia.
Porównań dokonywano w połowie programu rehabilitacji, bezpośrednio po jego zakończeniu oraz po 3 miesiącach. Uzyskano następujące wyniki: istotną poprawę w zakresie wytrzymałości (6-minutowy test chodu) odnotowano jedynie w grupie korzystającej z robota.
Wyniki uległy poprawie między pomiarem wyjściowym a połową programu oraz pomiędzy pomiarem wyjściowym a pomiarem bezpośrednio po zakończeniu badania. W grupie korzystającej z robota doszło także do poprawy równowagi, również w takim samym schemacie czasowym.
U osób, które ze względu na chorobę lub uraz utraciły funkcję chodu, egzoszkielet jest ważną pomocą nie tylko w odniesieniu do chodu, lecz również umożliwia zapobieganie negatywnym skutkom immobilizacji i trudnościom w pionizacji.
W grupie z robotem odnotowano także poprawę jakości życia w zakresie podskali funkcjonowania fizycznego. W grupie kontrolnej nie uległy istotnej statystycznie poprawie żadne z wymienionych powyżej parametrów. Ani w grupie kontrolnej, ani badawczej nie uległa poprawie prędkość chodu mierzona 10-metrowym testem chodu ani zmienne mierzone testem "wstań i idź".
Stwardnienie rozsiane jest chorobą o złej prognozie, a rezerwy, z których może czerpać pacjent, są ograniczone. Próby ich mobilizacji i utrzymania jak największej sprawności oraz możliwie zadowalającej jakości życia nie są łatwe. Efekty pracy również nie są trwałe, a pacjenci wymagają stałej rehabilitacji.
Wnioski te potwierdziło także przytoczone powyżej badanie. Na jego podstawie można stwierdzić, że zastosowanie robota poprawia wytrzymałość pacjentów ze stwardnieniem rozsianym na obciążenia fizyczne.
Jest to aspekt niezwykle ważny, ponieważ ogólna, postępująca słabość jest jednym z kluczowych objawów, z jakim zmagają się pacjenci. Niestety uzyskany efekt nie utrzymał się do kolejnego pomiaru po 3 miesiącach.
Wysiłki o utrzymanie sprawności osób ze stwardnieniem rozsianym powinny być czynione na bieżąco, a zastosowanie robota zdaje się czasowo poprawiać istotne parametry wytrzymałości i jakości życia.
Niestety, zgodnie z przytoczonymi powyżej wynikami, terapia tradycyjna, z zaangażowaniem jedynie terapeuty, nie jest w stanie zapewnić nawet czasowej poprawy badanej grupie pacjentów.
Chód w kinezjologii stosowanej
Kinezjologia stosowana jest metodą terapeutyczną wywodzącą się z chiropraktyki, która jednak z biegiem czasu znacznie uniezależniła się od swojego pierwowzoru i wypracowała zupełnie nowe sposoby diagnostyki i terapii.
Podstawą kinezjologii stosowanej jest tzw. trójkąt zdrowia8. Na jego trzech wierzchołkach znajdują się kategorie, którymi zajmuje się kinezjologia stosowana: struktura, biochemia i psychika.
Jednocześnie zaczęła również przejmować pewne wzorce z innych metod leczenia, np. z osteopatii. Pomimo obcych wpływów, pozostała niezależna i nie straciła na swojej wyjątkowości.
Praca strukturalna obejmuje zagadnienia mechaniczne obecne również w osteopatii, tj. układ mięśniowo- szkieletowy (tzw. parietalny), narządy wewnętrzne (układ wisceralny) oraz układ czaszkowo-krzyżowy (cranio-sacralny).
Aspekty biochemiczne odnoszą się do diagnostyki niedoborów oraz obciążeń chemicznych uniemożliwiających pacjentowi adekwatną adaptację do środowiska. Za pomocą wyjątkowego sposobu rozpoznawania zaburzeń możliwe jest regulowanie biochemii organizmu.
Równie ważna jest kwestia psychiki, zwłaszcza zagadnienie traum i stresu oraz ich wpływu na zaburzenia psychosomatyczne pacjentów. Kinezjologia stosowana nie jest psychoterapią, jednak posługuje się licznymi, w tym także manualnymi "narzędziami" wygaszania reakcji stresowych i usuwania następstw traum.
Dopiero gdy wszystkie trzy aspekty znajdują się w równowadze, można mówić o zdrowiu w rozumieniu kinezjologii stosowanej. Zdrowie w tej koncepcji nie oznacza braku chorób (jak jest to często potocznie rozumiane przez pacjentów) oraz nie jest definiowane jako dobrostan psychofizyczny (co jest pojęciem abstrakcyjnym, trudnym do zmierzenia i zobiektywizowania), lecz oznacza zdolności daptacyjne organizmu do tolerancji obciążeń zewnętrznych i wewnętrznych.
Najprawdopodobniej cel, jaki stawia sobie kinezjologia, najlepiej określić jako próba przywrócenia gibkości, elastyczności, sprężystości (resilience) reagowania na bodźce wewnętrzne i zewnętrzne.
Najczęściej z kinezjologią stosowaną kojarzony jest tzw. test mięśniowy. Uważany jest on za podstawowe narzędzie diagnostyczne. Taka definicja niewiele wyjaśnia i może znacznie spłycać zrozumienie bardzo ważnego zagadnienia.
Kluczowe jest bowiem słowo "narzędzie". Mięsień nie jest niczym więcej niż narzędziem, wskaźnikiem pozwalającym odczytać stan układu nerwowego. Kinezjologia stosowana diagnozuje stan układu nerwowego, wykorzystując w tym celu mięśnie, pozwalające odczytać i zinterpretować ten stan.
Wiadomo bowiem, jak układ nerwowy powinien sterować mięśniami w przypadku różnych wyzwań, którym jest poddawany, tzn. znana jest reakcja fizjologiczna oraz patologiczna. Przykładowo wiadomo, kiedy mięsień powinien być normotoniczny.
Przejawy hipotonii i hipertonii (w tym nierzadko uogólnionej) są w większości przypadków przejawem zaburzeń funkcjonowania układu nerwowego. Z tego względu test mięśniowy nie bada siły mięśni, a nawet nie bada samych mięśni.
Muszą być więc spełnione określone warunki, aby mięsień był dobrym wskaźnikiem stanu układu nerwowego, a samo badanie układu nerwowego za pomocą mięśni musi być wykonane precyzyjnie – inaczej uzyskamy jedynie informacje o kompensacjach, których nie da się zinterpretować.
Warto przy tym zwrócić uwagę, że test mięśniowy nie jest jedynym narzędziem do rozmowy z układem nerwowym, jakie może wykorzystywać kinezjolog. Być może równie często stosowana jest "prowokacja bólowa".
Polega ona na ocenie progu bólu w różnych obszarach ciała, które normalnie (nieprowokowane) nie są bolesne. Po znalezieniu takiego uwrażliwionego obszaru terapeuta może zmienić ustawienie pacjenta (np. kończyny), pozycję (siedzącą, leżącą, stojącą), sposób oddychania itp., sprawdzając, w jaki sposób takie postępowanie wpłynie na próg bólu.
Jak wspomnieliśmy, obydwa narzędzia mogą być w wielu sytuacjach wykorzystywane wymiennie. Jedno z nich posługuje się "receptorami mięśni", drugie "receptorami bólu", w podobny celu: badania układu nerwowego.
Jak już wspomnieliśmy, kinezjologia stosowana bada i usprawnia możliwości adaptacyjne organizmu do warunków zewnętrznych i wewnętrznych. Zgodnie z koncepcją kinezjologii stosowanej chodzenie i oddychanie są najistotniejszymi, najbardziej podstawowymi wzorcami sterowanymi przez układ nerwowy. Są one także ściśle ze sobą powiązane.
Z tego powodu wzorzec chodu i wzorzec oddychania stanowią punkty odniesienia w kinezjologii stosowanej. Są one wykorzystywane zarówno w diagnozie, jak i w leczeniu. Bez nadmiernej przesady można powiedzieć, że kinezjologia stosowana opiera się w całości na wzorcach chodu i oddychania.
Zaburzony chód traumatyzuje ciało wraz z każdym krokiem, wysyła nieprawidłowe informacje do układu nerwowego, który stara się je zinterpretować i zapobiegać dalszej traumatyzacji, jednocześnie zapewniając nam możliwość poruszania się, ponieważ czynność ta była w ewolucji niezbędna do przeżycia, a także w obecnych warunkach niemożność samodzielnego chodzenia stanowi istotny czynnik upośledzenia funkcjonowania. Z tego powodu można powiedzieć, że kinezjologia stosowana jest metodą skoncentrowaną na wzorcu chodu.
Terapia kinezjologii stosowanej na podstawie wzorca chodu
W kinezjologii stosowany jest powszechnie znany wzorzec chodu: kończyna wykroczna znajduje się w zgięciu, a kończyna zakroczna w wyproście. W związku z tym po stronie kończyny wykrocznej aktywna jest taśma przednia, natomiast hamowana jest taśma tylna, i odwrotnie w przypadku kończyny zakrocznej.
Kończyny górne poruszają się przeciwstawnie względem kończyn dolnych i w związku z tym przeciwne taśmy mięśniowe są torowane i hamowane przez układ nerwowy.
Zadanie terapeuty polega na sprawdzeniu, czy układ nerwowy właściwie toruje i hamuje określone grupy mięśniowe we wzorcu chodu. Zarówno nieprawidłowe hamowanie (hipotonia), jak i nieprawidłowe pobudzanie (hipertonia) świadczą o zaburzeniu i zawsze powinny być sprawdzone obydwie komponenty.
Uogólniona hipertonia, czyli brak hamowania wszystkich grup mięśniowych, jest zjawiskiem bardziej złożonym i właściwie nigdy nie ma podłoża mechanicznego. Często jej przyczyną są zaburzenia biochemiczne i/ lub traumatyczne.
Uogólniona hipotonia również nie musi mieć charakteru mechanicznego. Zdarza się jednak, że hipotonią objęta jest znaczna część ciała. Taka sytuacja może mieć miejsce np. w przypadku niestabilności kręgosłupa szyjnego. Wówczas wszystkie mięśnie poniżej zaburzonego segmentu będą hipotoniczne.
Podobnie niestabilność innych istotnych dla stabilizacji obszarów ciała (np. miednicy) będzie powodowała hipotonię mięśni przyczepionych do miednicy. Hipotonia może dotyczyć także całej taśmy mięśniowej. Uszkodzenie jednego z jej segmentów pociąga za sobą wyłączenie całej taśmy. Z kolei dolegliwości pojawiać się będą w okolicy najsłabszego (najistotniejszego ogniwa).
Prześledźmy tę sytuację na przykładzie powierzchownej taśmy przedniej. Nie wchodząc w szczegóły, w jej skład wchodzą krótkie i długie prostowniki palców stóp, mięsień piszczelowy przedni, mięsień prosty uda, mięsień prosty brzucha, powięź wewnątrzpiersiowa, mięsień mostkowo-obojczykowo-sutkowy oraz powięź naczaszna.
Przykładowo uraz stopy może spowodować wyłączenie całej taśmy, co w szczególnym stopniu może oddziaływać na kluczowe obszary ciała. Takim elementem jest w wymienionej taśmie mięsień mostkowo-obojczykowo-sutkowy.
Jego hipotonia staje się przyczyną niestabilności obojczyka i problemów ze stawem barkowym. Ze względu na przyczep przy wyrostku sutkowatym kości skroniowej mogą pojawiać się dolegliwości bólowe głowy (zwykle związane z chodzeniem).
W pobliżu przyczepu głowowego znajduje się otwór szyjny, przez który przechodzi m.in. żyła szyjna wewnętrzna i nerw błędny. Powoduje to problemy z odpływem krwi żylnej z głowy oraz zaburzenia autonomiczne. Na zaburzenie kompensacyjnie reaguje całe ciało i powstający wzorzec jest zdecydowanie bardziej skomplikowany.
Jednak kinezjologia stosowana pozwala go rozpoznać i pod kontrolą układu nerwowego odnaleźć struktury, które rzeczywiście wymagają korekcji. Należy podkreślić, że przy mechanicznym zaburzeniu jakiegoś ogniwa uczestniczącego we wzorcu chodu układ nerwowy wyłącza je.
W rezultacie inne ogniwa muszą pracować mocniej i ulegają przeciążeniu. Są one również miejscem bólu, jednak nie są jego przyczyną. Rozluźnianie napiętych obszarów ciała, tak często wykonywane w innych podejściach terapeutycznych, prowadzi co najwyżej do krótkotrwałej ulgi.
Konieczne jest odnalezienie "niemych" zaburzeń pod postacią wyłączonych obszarów i ponowna ich integracja, aby inne struktury przestały być przeciążane. Wzorzec chodu jest doskonałym narzędziem poszukiwania wyłączonych i przeciążonych obszarów ciała.
Z drugiej strony każdy krok wykonywany za pomocą hipotonicznych lub hipertonicznych mięśni traumatyzuje organizm, a zadaniem kinezjologa jest odtworzenie możliwości adaptacyjnych organizmu we wzorcu chodu. Dlatego można powiedzieć, że kinezjologia stosowana jest w dużej mierze rehabilitacją i reedukacją poprawnego chodu.
Chód i oddychanie w kinezjologii stosowanej
Wspomnieliśmy już wcześniej, że chód i oddychanie są najważniejszymi wzorcami ruchowymi w kinezjologii stosowanej. Co ważne, są one również ze sobą powiązane. Prawidłowy chód toruje właściwe oddychanie.
Wzorzec chodu nie ogranicza się bowiem do naprzemiennych wzorców zgięciowych i wyprostnych. Są one oczywiście niezwykle istotne i także torują oddychanie, np. poprzez właściwą koordynację pracy mięśni czworobocznych grzbietu i prostego brzucha, jednak dla oddychania szczególnie ważna jest naprzemienna komponenta rotacyjna, pozwalająca na właściwą pracę przepon oraz mięśni skośnych wewnętrznych i zewnętrznych brzucha oraz mięśni międzyżebrowych wewnętrznych i zewnętrznych, mostkowo-obojczykowo-sutkowych, pochyłych itd.
Rotacja tułowia powinna współgrać z hamowaniem i torowaniem określonych grup mięśniowych podczas cyklu wdechu i wydechu. Jeżeli któraś z taśm nie pracuje w cyklu chodu, wzorzec oddechowy zostanie zaburzony.
Z drugiej strony zaburzenie oddychania, np. poprzez asymetryczną pracę przepony, wynikającą z urazu odcinka szyjnego, będzie zaburzała wzorzec chodu. Kinezjologia stosowana stara się zharmonizować te wzorce w celu zwiększenia zdolności adaptacyjnych organizmu.
W artykule poruszyliśmy tematykę znaczenia chodu w rehabilitacji, metod fizjoterapeutycznych wykorzystujących chód jako podstawę diagnozy i postępowania z pacjentem, a także wybrane najnowsze rozwiązania techniczne mające na celu przywracanie funkcji chodu oraz chodzenie pacjentom, którzy w wyniku choroby lub wypadku utracili taką możliwość.
Należy mieć nadzieję, że postęp wiedzy medycznej i techniki w coraz większym stopniu będzie ułatwiał życie osobom z ograniczeniami ruchowymi.
- PNF in Der Praxis: Eine Anleitung in Bildern; wydanie 8.; Springer 2019.
- Pohl M., Werner C., Holzgraefe M., Kroczek G., Mehrholz J., Wingendorf I., Hoölig G., Koch R., Hesse S., Repetitive locomotor training and physiotherapy improve walking and basic activities of daily living after stroke: a single-blind, randomized multicentre trial (DEutsche GAngtrainerStudie, DEGAS). Clin Rehabil. 2007 Jan;21(1):17-27.
- Tong R.K., Ng M.F., Li L.S., Effectiveness of gait training using an electromechanical gait trainer, with and without functional electric stimulation, in subacute stroke: a randomized controlled trial. Arch Phys Med Rehabil. 2006 Oct;87(10):1298-304.
- Peurala S.H., Tarkka I.M., Pitkänen K., Sivenius J., The effectiveness of body weight-supported gait training and floor walking in patients with chronic stroke. Arch Phys Med Rehabil. 2005 Aug;86(8):1557-64.
- Louie D.R., Eng J.J., Lam T., Spinal Cord Injury Research Evidence (SCIRE) Research Team. Gait speed using powered robotic exoskeletons after spinal cord injury: a systematic review and correlational study. J Neuroeng Rehabil. 2015 Oct 14;12:82.
- Esclarín-Ruz A., Alcobendas-Maestro M., Casado-Lopez R., Perez-Mateos G., Florido-Sanchez M.A., Gonzalez-Valdizan E., Martin J.L., A comparison of robotic walking therapy and conventional walking therapy in individuals with upper versus lower motor neuron lesions: a randomized controlled trial. Arch Phys Med Rehabil. 2014 Jun;95(6):1023-31.
- Straudi S., Fanciullacci C., Martinuzzi C., Pavarelli C., Rossi B., Chisari C., Basaglia N., The effects of robot-assisted gait training in progressive multiple sclerosis: A randomized controlled trial. Mult Scler. 2016 Mar; 22(3):373-84.
- Applied Kinesiology Synopsis, Triad of Health Publishing; 2nd Edition (1. January 1988)