Wprowadzenie
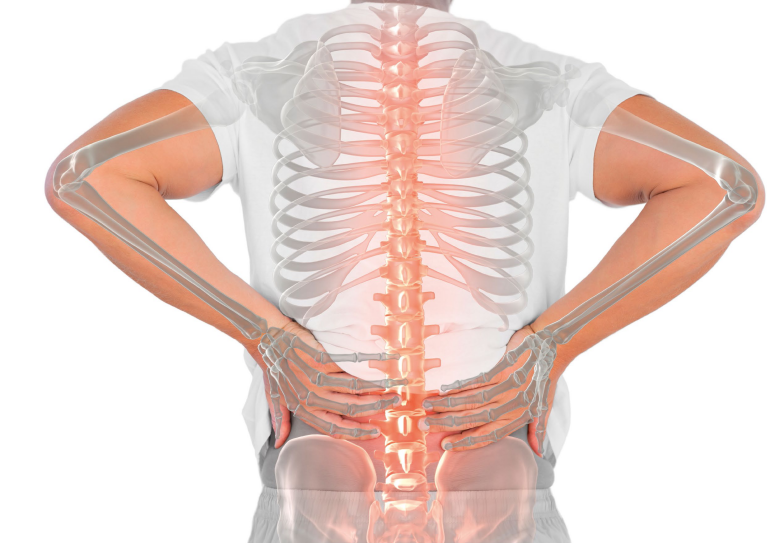
Zwyrodnienie kręgosłupa lędźwiowego związane z wiekiem polega na obniżeniu wysokości krążka międzykręgowego ( potocznie dysku), pogrubieniu więzadła żółtego oraz przeroście stawów międzywyrostkowych na skutek procesów zwyrodnieniowych1,2. Zmiany te mogą prowadzić do znacznego zwężenia kanału kręgowego, znanego również jako stenoza kręgosłupa lędźwiowego (LSS). Typowe objawy kliniczne objawowego LSS (sLSS) to zmęczenie, ból pleców i/lub nóg po pewnym czasie marszu, zwany również obrzękiem kręgosłupa3,4.
Badania analizy chodu wykazały, że pacjenci z sLSS chodzą wolniej, krótszymi krokami, mniejszą kadencją (częstotliwością)5,6,7 i mniejszym zakresem ruchu zgięcia-wyprostu stawu biodrowego8 niż osoby zdrowe. Sztywność miednicy w płaszczyźnie poprzecznej była większa i związana z ciężkością stenozy9. Chociaż kilka badań dotyczyło kinematyki stawów i odnotowało różnice w stosunku do zdrowych osób, niewiele wiadomo na temat wzorców aktywacji mięśni pośladkowych i przykręgosłupowych, które stabilizują miednicę i tułów u pacjentów z sLSS10. Napinacz powięzi szerokiej, ale nie mięsień pośladkowy średni miał wyższe aktywacje podczas chodu u pacjentów z sLSS w porównaniu z grupą kontrolną11, nie oceniono innych parametrów kinematycznych. Jednak podczas chodzenia przy pokonywaniu przeszkody obserwowano u pacjentów wyższe aktywacje mięśnia pośladkowego niż w grupie kontrolnej12. U sześciu pacjentów zgięcie tułowia i aktywacja mięśni przykręgosłupowych podczas chodzenia zmniejszyły się po operacji, ale nie oceniono różnic w porównaniu z grupą kontrolną13. Ponadto pacjenci z sLSS mieli mniejszą aktywność mięśni przykręgosłupowych niż pacjenci z kifozą lędźwiową w pozycji stojącej14, a czas reakcji na nagłe obciążenie mięśni przykręgosłupowych kończyny górnej był dłuższy niż u osób zdrowych15. Co więcej, niedawna metaanaliza wykazała wyższą aktywację mięśni przykręgosłupowych odcinka lędźwiowego podczas chodzenia u pacjentów z przewlekłym bólem krzyża w porównaniu z grupą kontrolną16.
W ostatnich latach pojawiły się sumaryczne wyniki, takie jak Gait Variability Score (GVS), Gait Profile Score (GPS)17,18 oraz Gait Deviation Index (GDI)19, aby określić ilościowo różnice we wzorcach chodu między pacjentami a zdrowymi osobami będącymi grupą kontrolną. Wyniki te wskazują różnicę odległości kątów kończyn dolnych między indywidualnym pacjentem a średnią z grupy kontrolnej i wykazano, że korelują z oceną jakości chodzenia przez ekspertów20. Zastosowania obejmują ilościową ocenę różnic we wzorcach chodu u pacjentów ze skoliozą21 lub niecałkowitym uszkodzeniem rdzenia kręgowego22,23. U pacjentów z sLSS GDI średnio korelował z bólem po 20-minutowym marszu, co wskazuje, że wraz ze wzrostem bólu pogarsza się jakość chodu24. W przypadku sygnałów elektromiograficznych (EMG) podczas chodzenia Ropars i wsp. przeprowadzili ocenę profilu EMG25. Wynik ten oblicza pierwiastek średniej kwadratowej odległości (RMS) między obwiedniami EMG pacjenta a tymi z grupy kontrolnej i został wykorzystany do ilościowego określenia zmian we wzorcach aktywacji mięśni u dzieci z dystrofią mięśniową Duchenne’a25. Wszystkie te wyniki mają wspólną cechę, ponieważ opisują ogólne odchylenie biomechaniki chodu lub wzorców aktywacji mięśni od zdrowych, a zatem potencjalnie odzwierciedlają nasilenie schorzeń i mogą korelować z wynikami klinicznymi.
Celem tego badania było określenie różnic we wzorcach aktywacji mięśni pośladkowych i przykręgosłupowych wraz z parametrami przestrzenno-czasowymi i kinematyką stawu strzałkowego między pacjentami z sLSS a osobami zdrowymi, oraz określenie ilościowe tych różnic za pomocą wyników chodu i EMG w celu określenia związku między wynikami klinicznymi (wynik ODI, ból) a wzorcami chodu i EMG.
Metody
Uczestnicy
Do tego jednorazowego, przekrojowego badania obserwacyjnego zrekrutowano pacjentów z kliniczną diagnozą (na podstawie historii pacjenta i obrazowania metodą rezonansu magnetycznego (MRI)) sLSS, którzy mieli objawy przez co najmniej 6 miesięcy i mieli zaplanowaną operację dekompresji między kwietniem 2019 r. a sierpniem 2020 r. Kryteriami wykluczenia z badania byli pacjenci w wieku poniżej 30 lat, przebyta operacja dekompresyjna, wskaźnik masy ciała (BMI) ≥ 35 kg/m2, korzystanie z pomocy do chodzenia oraz brak możliwości wyrażenia świadomej zgody. Grupa zdrowych osób kontrolnych w tym samym przedziale wiekowym co pacjenci, z BMI ≤ 35 kg/m2 i bez klaudynacji (ból nogi podczas chodzenia) w wywiadzie, przebytej operacji kompleksu lędźwiowo-miedniczno-biodrowego lub bólu kończyny dolnej lub dolnej części pleców w ciągu ostatnich 6 miesięcy.
Zbieranie danych
Dane kliniczne i biomechaniczne pacjentów zebrano w dniu poprzedzającym operację. Ból oceniano na numerycznej skali ocen (0 – brak bólu; 10 – ból maksymalny/ silny). Następnie przeprowadzono test chodzenia we własnym tempie w 200-metrowym korytarzu szpitala. Uczestników poproszono o chodzenie tam i z powrotem po korytarzu przez 30 minut lub do momentu, gdy objawy spowodują ich zatrzymanie. Obustronną aktywację mięśnia pośladkowego średniego, prostownika kręgosłupa (najdłuższego) i wielodzielnego (poziom L5) mierzono w sposób ciągły za pomocą powierzchniowych czujników EMG ze zintegrowanymi trójwymiarowymi akcelerometrami.
Wyniki
Uczestnicy
Do badania włączono 20 pacjentów z sLSS zaplanowanych do operacji i 19 zdrowych osób z grupy kontrolnej. Pacjenci mieli znacznie wyższy wynik ODI niż grupa kontrolna (+28 punktów; p <0,001). Większość pacjentów miała największe nasilenie stenozy stopnia C (ciężkie zwężenie), a średni naciek tłuszczowy przykręgosłupowy wynosił poniżej 2 (mniej niż 50% tłuszczu w mięśniach). Objawy utrzymywały się przez co najmniej 6 miesięcy do ponad 2 lat. Ból był zlokalizowany głównie po lewej stronie (kręgosłupa lędźwiowego i/lub nogi) u sześciu, po prawej stronie u trzech i po obu stronach u 11 pacjentów i występował głównie podczas stania, chodzenia lub innych czynności. Pozostali pacjenci nie wspominali o żadnej konkretnej czynności wywołującej ból.
Dyskusja
Zbadano różnice we wzorcach aktywacji mięśni i kinematyce chodu między pacjentami z sLSS (głównie nasilony stopień stenozy) a zdrowymi osobami i obliczono wyniki EMG i chodu, aby określić ilościowe odchylenia od kontroli. Pacjenci mieli większe odchylenia w aktywacji mięśni i stopniach odchylenia stawów niż osoby zdrowe. Jednak u pacjentów żadna z ocen klinicznych (poziom bólu, ODI) nie korelowała z żadnym z tych parametrów biomechanicznych, co wskazuje, że wyniki EMG i oceny chodu oceniają inne aspekty sLSS niż te kliniczne.
Globalny wynik profilu EMG i wzorce aktywacji mięśni wskazują, że pacjenci pobudzają mięśnie pośladkowe i przykręgosłupowe inaczej niż zdrowe osoby. W innym badaniu na zdrowych osobach zaobserwowano dłuższą aktywację mięśnia pośladkowego przy porównywaniu prędkości chodu z wolnymi, normalnymi lub szybszymi36. W związku z tym możliwe jest, że do stabilizacji biodra i miednicy podczas chodzenia z mniejszą prędkością potrzebna jest dłuższa aktywacja mięśnia pośladkowego średniego. Różnice w aktywacji mięśni przykręgosłupowych wskazują na bardziej ciągłą aktywację z mniej wyraźnym wzorem włączania/wyłączania u pacjentów z sLSS niż w grupie kontrolnej. Podobny wzorzec w porównaniu z grupą kontrolną zaobserwowano u pacjentów z niestabilnością lędźwiową spowodowaną chorobą zwyrodnieniową krążka międzykręgowego, nawet przy odpowiedniej prędkości chodu37. Możliwe, że obserwowany wcześniej naciek tłuszczowy28,38 i przypuszczalnie upośledzona funkcja mięśni przykręgosłupowych wymaga większej aktywacji mięśni, aby utrzymać wyprostowany tułów. Ta kompensacja może być jeszcze bardziej wyraźna podczas chodzenia, gdy osoba chodzi z większym zgięciem tułowia do przodu, tak jak pacjenci z sLSS6,13,39. Ponadto u pacjentów z przewlekłym bólem krzyża zgłaszano wyższe aktywacje mięśni wielodzielnych i/lub prostowników kręgosłupa, zwłaszcza podczas podwójnego podparcia i wymachu16 i przypuszczano, że jest to strategia kompensacyjna mająca na celu zwiększenie stabilności kręgosłupa40. Dlatego porównywalne wzorce pacjentów z sLSS mogą wskazywać na strategię przystosowania się do bólu i niestabilności kręgosłupa.
Wyniki dotyczące parametrów przestrzenno-czasowych chodu i kinematyki stawów są zgodne z wcześniejszymi badaniami, które wykazały mniejszą prędkość chodu5,6,7,41, niższą kadencję6, krótsze kroki5,6,7 oraz mniejszą amplitudę obrotów stawu biodrowo-skokowego8 u pacjentów z sLSS w porównaniu do osób zdrowych. Igawa i in.39 opisali, że pacjenci z sLSS stosują dwie różne strategie łagodzenia bólu i objawów podczas długotrwałego chodzenia: albo zwiększenie zgięcia tułowia, albo zmniejszenie długości kroku i wyprostu bioder. Chociaż powyższe badania nie pozwalały na pomiar kątów zgięcia tułowia podczas chodzenia, obserwowana wyższa aktywacja mięśni przykręgosłupowych może wskazywać, że kąty zgięcia tułowia różniły się między pacjentami z sLSS i zdrowymi osobami, a zatem mogą reprezentować mechanizm kompensacyjny w celu złagodzenia bólu.

Oceniono ilościowo ogólne różnice między pacjentami, a zdrowymi kontrolami, używając podsumowujących wyników chodu dla wzorców EMG i kinematycznych. Wyniki te były znacznie niższe u pacjentów niż w grupie kontrolnej i potwierdzają badania Garbelotti i in.24, który zgłosił GDI około 75 (około 2,5 SD z grupy kontrolnej) dla kinematyki chodu u pacjentów z LSS24. Dlatego powyższe wyniki sugerują, że wyniki chodu oparte na kątach stawu strzałkowego mierzonych za pomocą czujników inercyjnych lub na podstawie wzorców EMG przykręgosłupowego i pośladkowego mogą potencjalnie różnicować pacjentów z sLSS i zdrowe osoby. Jednak ani wynik profilu EMG, ani wynik mGPS nie korelowały z bólem ani wynikiem ODI, co potwierdza wcześniejsze wyniki, w których GDI nie korelował z bólem przed 20-minutowym marszem na bieżni, ale korelował pod koniec marszu24. Chociaż wskazuje to, że te funkcjonalne wyniki chodu oceniają inne aspekty choroby niż wyniki kliniczne, możliwe jest również, że inne wyniki kliniczne zaprojektowane specjalnie do oceny pacjentów z sLSS mogą uchwycić globalne zmiany w chodzie i aktywacji mięśni lepiej niż bardziej ogólny wynik ODI.
Główną siłą tych badań jest to, że zmierzono wzorce aktywacji mięśni wraz z parametrami czasowo-przestrzennymi chodu i kinematyką kończyn dolnych podczas chodzenia w tym samym badaniu.
Użyto dwóch niezależnych systemów pomiarowych, a algorytmy mogły wykryć uderzenia piętą w nieco innych punktach czasowych. Co więcej, włączeni pacjenci byli raczej podobni pod względem ciężkości zwężenia i poziomu nacieku tłuszczowego w mięśniach przykręgosłupowych i wykazywali jedynie umiarkowaną niepełnosprawność zgodnie z wynikiem ODI. W związku z tym wyników nie można uogólniać na pacjentów z cięższą niepełnosprawnością lub z innym stopniem stenozy lub nacieku tłuszczowego. Dodatkowo, chociaż wszyscy uczestnicy, w tym grupa kontrolna, byli starsi niż 50 lat, grupa kontrolna była nieco młodsza od pacjentów, i nie można wykluczyć wpływu tej różnicy na wyniki. Pacjenci chodzili wolniej niż grupa kontrolna, a wiadomo, że prędkość chodu wpływa na kinematykę stawów i wzorce aktywacji mięśni19,36, dlatego nie jest możliwe rozróżnienie wpływu prędkości chodu oraz choroby na chód i aktywację mięśni w niniejszym badaniu.
Niemniej jednak zaobserwowane różnice potencjalnie wskazują na zmienione zapotrzebowanie układu mięśniowo-szkieletowego podczas chodzenia w życiu codziennym w porównaniu ze zdrowymi osobami z grupy kontrolnej. Potrzebne są dalsze badania, aby lepiej zrozumieć strategie kompensacyjne i związek między objawami klinicznymi, a funkcją mięśni i chodu w całym procesie chorobowym. Ocena różnic w równowadze strzałkowej oraz szczegółowe ruchy tułowia i kręgosłupa podczas chodu nie były możliwe. Uwzględnienie tych aspektów wraz z jednostronnością objawów w przyszłych badaniach pozwoliłoby uzyskać lepszy wgląd w mechanizmy powodujące różnice w aktywacji mięśni i wzorcach chodu między pacjentami z sLSS a osobami zdrowymi. Ponadto, ponieważ badanie to obejmowało tylko pacjentów przedoperacyjnych, wpływ leczenia chirurgicznego lub zachowawczego na obserwowane zmiany chodu nie jest znany i powinien zostać zbadany w przyszłych badaniach.
Wniosek
Badanie to ujawniło, że oprócz znanych różnic we wzorcach chodu, pacjenci aktywują mięśnie pośladkowe i przykręgosłupowe inaczej niż zdrowi kontrolni. Przedstawione zbiorcze wyniki odchyleń chodu i EMG (mGPS i EMG-Profile Score) mogą stanowić dodatkowe parametry opisujące stan funkcjonalny pacjentów z sLSS, który można ocenić w praktyce klinicznej za pomocą czujników do noszenia na ciele. Większe badania grupowe na pacjentach z różnym stopniem stenozy i zaniku tkanki tłuszczowej z dodatkową oceną wyrównania tułowia i ruchu są niezbędne, aby lepiej zrozumieć proces chorobowy i potencjalnie poprawić planowanie leczenia (takie jak czas operacji, dodatkowy trening mięśni przykręgosłupowych).
Żródło: (np.) Gait & Posture 100 (2023) 96–102
(C) 2023 The Authors
Adaptacja: Klaudia Gregorczyk
Na podstawie licencji CC BY
(http://creativecommons.org/licenses/by/4.0/)
- T. Okuda, I. Baba, Y. Fujimoto, N. Tanaka, T. Sumida, H. Manabe, et al., The pathology of ligamentum flavum in degenerative lumbar disease, Spine 29 (15) (2004) 1689–1697.
- W. Kirkaldy-Willis, J. Wedge, K. Yong-Hing, J. Reilly, Pathology and pathogenesis of lumbar spondylosis and stenosis, Spine 3 (4) (1978) 319–328.
- C.C. Tomkins-Lane, M.C. Batti´e, Predictors of objectively measured walking capacity in people with degenerative lumbar spinal stenosis, J. Musculoskelet. Rehabil. 26 (4) (2013) 345–352.
- T. Amundsen, H. Weber, H.J. Nordal, B. Magnaes, M. Abdelnoor, F. Lilleås, Lumbar spinal stenosis: conservative or surgical management? A prospective 10-year study, Spine 25 (11) (2000) 1424–1436.
- S. Loske, C. Nuesch, K.S. Byrnes, O. Fiebig, S. Scharen, A. Mundermann, et al., Decompression surgery improves gait quality in patients with symptomatic lumbar spinal stenosis, Spine J. 18 (12) (2018) 2195–2204.
- W. Kuwahara, M. Deie, N. Fujita, N. Tanaka, K. Nakanishi, T. Sunagawa, et al., Characteristics of thoracic and lumbar movements during gait in lumbar spinal stenosis patients before and after decompression surgery, Clin. Biomech. 40 (2016) 45–51.
- Y.G. Li, L.P. Li, Z.J. Li, H. Li, Y. Li, Q. Li, et al., Gait analysis in the elderly patients with lumbar spinal stenosis, Int. Orthop. 45 (3) (2021) 673–679.
- H. Hayashi, Y. Toribatake, H. Murakami, T. Yoneyama, T. Watanabe, H. Tsuchiya, Gait analysis using a support vector machine for lumbar spinal stenosis, Orthopedics 38 (11) (2015) e959–e964.
- H. Bumann, C. Nuesch, S. Loske, S.K. Byrnes, B. Kovacs, R. Janssen, et al., Severity of degenerative lumbar spinal stenosis affects pelvic rigidity during walking, Spine J. 20 (1) (2020) 112–120.
- J. Wang, S. Ullah, M.A. Solano, S.C. Overley, D.B. Bumpass, E.M. Mannen, Changes in kinematics, kinetics, and muscle activity in patients with lumbar spinal stenosis during gait: systematic review, Spine J. (2021).
- J.J. Kim, H. Cho, Y. Park, J. Jang, J.W. Kim, J.S. Ryu, Biomechanical influences of gait patterns on knee joint: Kinematic & EMG analysis, PLoS One 15 (5) (2020),e0233593.
- S.S. Shin, W.G. Yoo, Stepping over an obstacle in patients with lumbar spinal stenosis: trunk and lower extremities of kinematic and muscle activation normalized by double limb support. A preliminary study, Technol. Health Care 27(1) (2019) 1–11.
- T. Goto, T. Sakai, T. Enishi, N. Sato, K. Komatsu, K. Sairyo, et al., Changes of posture and muscle activities in the trunk and legs during walking in patients with lumbar spinal stenosis after decompression surgery. A preliminary report, Gait Posture 51 (2017) 149–152.
- M. Enomoto, D. Ukegawa, K. Sakaki, S. Tomizawa, Y. Arai, S. Kawabata, et al., Increase in paravertebral muscle activity in lumbar kyphosis patients by surface electromyography compared with lumbar spinal canal stenosis patients and healthy volunteers, J. Spinal Disord. Tech. 25 (6) (2012) E167–E173.
- T. Kaariainen, V. Leinonen, S. Taimela, T. Aalto, H. Kroger, A. Herno, et al., Lumbar paraspinal and biceps brachii muscle function and movement perception in lumbar spinal stenosis, Eur. Spine J. 22 (4) (2013) 788–793.
- J.A. Smith, H. Stabbert, J.J. Bagwell, H.L. Teng, V. Wade, S.P. Lee, Do people with low back pain walk differently? A systematic review and meta-analysis, J. Sport Health Sci. (2022).
- R. Baker, J.L. McGinley, M.H. Schwartz, S. Beynon, A. Rozumalski, H.K. Graham, et al., The gait profile score and movement analysis profile, Gait Posture 30 (3) (2009) 265–269.
- R. Baker, J.L. McGinley, M. Schwartz, P. Thomason, J. Rodda, H.K. Graham, The minimal clinically important difference for the gait profile score, Gait Posture 35 (4) (2012) 612–615.
- M.H. Schwartz, A. Rozumalski, The gait deviation index: a new comprehensive index of gait pathology, Gait Posture 28 (3) (2008) 351–357.
- S. Beynon, J.L. McGinley, F. Dobson, R. Baker, Correlations of the gait profile score nd the movement analysis profile relative to clinical judgments, Gait Posture 32(1) (2010) 129–132.
- B. Garg, M. Gupta, N. Mehta, R. Malhotra, Influence of etiology and onset of deformity on spatiotemporal, kinematic, kinetic, and electromyography gait variables in patients with scoliosis—a prospective, comparative study, Spine 46 (6) (2021) 374–382.
- P. Wedege, K. Steffen, V. Strom, A.I. Opheim, Reliability of three-dimensional kinematic gait data in adults with spinal cord injury, J. Rehabil. Assist. Technol. Eng. 4 (2017), 2055668317729992.
- A.T. Murphy, S. Kravtsov, M. Sangeux, B. Rawicki, P.W. New, Utilizing three dimensional clinical gait analysis to optimize mobility outcomes in incomplete spinal cord damage, Gait Posture 74 (2019) 53–59.
- A. Garbelotti, P.R.G. Lucareli, A. Ramalho, W. de Godoy, M. Bernal, J.M.D. A. Greve, An investigation of the value of tridimensional kinematic analysis in functional diagnosis of lumbar spinal stenosis, Gait Posture 40 (1) (2014) 150–153.
- 25. J. Ropars, M. Lempereur, C. Vuillerot, V. Tiffreau, S. Peudenier, J.M. Cuisset, et al., Muscle activation during gait in children with duchenne muscular dystrophy, PLoS One 11 (9) (2016), e0161938.
- 26. C. Schizas, N. Theumann, A. Burn, R. Tansey, D. Wardlaw, F.W. Smith, et al., Qualitative grading of severity of lumbar spinal stenosis based on the morphology of the dural sac on magnetic resonance images, Spine 35 (21) (2010) 1919–1924.
- 27. D. Goutallier, J.-M. Postel, J. Bernageau, L. Lavau, M.-C. Voisin, Fatty muscle degeneration in cuff ruptures: pre- and postoperative evaluation by CT scan, Clin. Orthop. Relat. Res. 304 (1994) 78–83.
- 28. F. Mandelli, C. Nüesch, Y. Zhang, F. Halbeisen, S. Scharen, ¨ A. Mündermann, et al., Assessing fatty infiltration of paraspinal muscles in patients with lumbar spinal stenosis: goutallier classification and quantitative MRI measurements, Front. Neurol. (2021) 12.
- J.C. Fairbank, P.B. Pynsent, The Oswestry disability index, Spine 25 (22) (2000) 2940–2953.
- H.J. Hermens, B. Freriks, C. Disselhorst-Klug, G. Rau, Development of recommendations for SEMG sensors and sensor placement procedures, J. Electromyogr. Kinesiol. 10 (5) (2000) 361–374.
- Gait phase detection and step length estimation of gait by means of inertial sensors N. Negaard R. Kauert S. Andres T. Schauer J. Raisch IFMBE Proc 2005.
- T. Seel, J. Raisch, T. Schauer, IMU-based joint angle measurement for gait analysis, Sensors 14 (4) (2014) 6891–6909.
- W. Zijlstra, A.L. Hof, Assessment of spatio-temporal gait parameters from trunk accelerations during human walking, Gait Posture 18 (2) (2003) 1–10.
- T.C. Pataky, J. Vanrenterghem, M.A.Z. Robinson, one-dimensional, parametric vs. non-parametric, and confidence interval vs. hypothesis testing procedures in onedimensional biomechanical trajectory analysis, J. Biomech. 48 (7) (2015) 1277–1285.
- T.C. Pataky, One-dimensional statistical parametric mapping in Python, Comput. Methods Biomech. Biomed. Eng. 15 (3) (2012) 295–301.
- C. Anders, K. Sander, F. Layher, S. Patenge, R.W. Kinne, Temporal and spatial relationship between gluteal muscle Surface EMG activity and the vertical component of the ground reaction force during walking, PLoS One 16 (5) (2021), e0251758.
- M. Miscusi, M. Serrao, C. Conte, G. Ippolito, F. Marinozzi, F. Bini, et al., Spatial and emporal characteristics of the spine muscles activation during walking in patients with lumbar instability due to degenerative lumbar disk disease: evaluation in presurgical setting, Hum. Mov. Sci. 66 (2019) 371–382.
- J.A. Yarjanian, A. Fetzer, K.S. Yamakawa, H.C. Tong, M. Smuck, A. Haig, Correlation of Paraspinal atrophy and denervation in back pain and spinal stenosis relative to asymptomatic controls, PM&R. 5 (1) (2013) 39–44.
- T. Igawa, J. Katsuhira, A. Hosaka, K. Uchikoshi, S. Ishihara, K. Matsudaira, Kinetic and kinematic variables affecting trunk flexion during level walking in patients with lumbar spinal stenosis, PLoS One 13 (5) (2018), e0197228-e.
- L. Ghamkhar, A.H. Kahlaee, Trunk muscles activation pattern during walking in subjects with and without chronic low back pain: a systematic review, PM R. 7 (5) (2015) 519–526.
- H.C. Tong, A.J. Haig, M.E. Geisser, K.S.J. Yamakawa, J.A. Miner, Comparing pain severity and functional status of older adults without spinal symptoms, with lumbar spinal stenosis, and with axial low back pain, Gerontology 53 (2) (2007) 111–115.
- G. Stucki, L. Daltroy, M.H. Liang, S.J. Lipson, A.H. Fossel, J.N. Katz, Measurement properties of a self-administered outcome measure in lumbar spinal stenosis, Spine 21 (7) (1996) 796–803.