W obrębie kręgosłupa lędźwiowego bardzo często zdarzają się uszkodzenia krążka. Typowa tylno-boczna wypuklina krążka zwykle powstaje w mechanizmie zgięcia połączonego z rotacją i zazwyczaj wiąże się z obciążeniem, jakie występuje np. podczas prac w ogrodzie czy podnoszenia ciężkiego przedmiotu.
Pacjent opisuje, jak doszło do uszkodzenia, często posługując się obrazowym językiem – "coś trzasnęło w plecach" czy "połamało mnie w krzyżu" – który fizjoterapeuta musi umieć zidentyfikować.
Pacjent wspomina o odczuciu, jakby w plecach coś się stało, ale nadal starał się wykonywać podjętą czynność. W ciągu godziny lub dwóch ból w plecach pacjenta nasilił się na tyle, że musiał wrócić do domu lub udać się w miejsce, gdzie mógł usiąść czy się położyć, by przyjąć pozycję najbardziej redukującą ból.
W ciągu 12 do 24 godzin pacjent zaczyna odczuwać ból w dole pleców oraz pojawiają się nowe symptomy: ból kończyny dolnej z ewentualnym przesunięciem bocznym (tzw. shiftem). Nie jest w stanie przyjąć pozycji wyprostowanej bez odczuwania znacznego bólu.
Urazy międzykręgowe krążków lędźwiowych - diagnoza
W przeszłości tego typu scenariusz kliniczny przypisywano uszkodzeniu pierścienia włóknistego i wynikłej z niego wypuklinie krążka międzykręgowego, która stykając się z korzeniem nerwowym, powodowała jego podrażnienie i w rezultacie ból kończyny dolnej oraz przyjmowanie pozycji antalgicznej pod postacią przesunięcia bocznego.
Jeśli jednak jest to jedyne wytłumaczenie patologii powodującej opisane objawy, dlaczego tak dużo czasu upływa do wystąpienia przesunięcia bocznego i objawów w kończynie? Jeśli do wypukliny krążka dochodzi od razu, dlaczego ból kończyny i przesunięcie boczne nie pojawiają się w ciągu pierwszej godziny po urazie?
Odpowiedź na to pytanie znajdziemy po bliższym przyjrzeniu się anatomii i unerwieniu krążka międzykręgowego. Podczas płodowego rozwoju krążka pierścień włóknisty, jądro miażdżyste oraz kość kręgu zaczynają powstawać z tej samej matrycy komórkowej, choć rozwój trzech części krążka jest zróżnicowany: powstaje chrzęstna płytka graniczna kręgu, pierścień włóknisty i jądro miażdżyste.
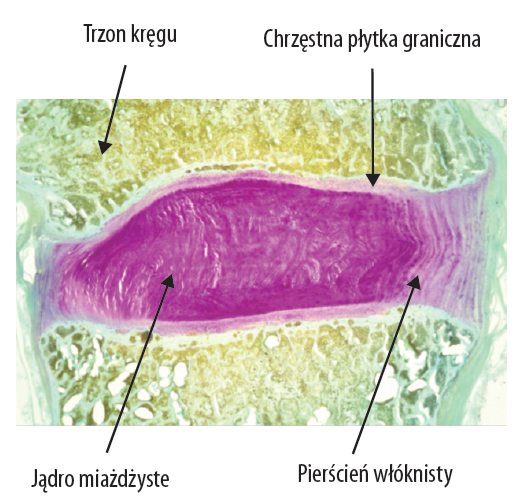
Kluczową dla owego rozwoju kwestią jest, aby włókna pierścienia stanowiły integralną część płytki chrzęstnej, a nie strukturę osobną (ryc. 1). Kilka zewnętrznych warstw pierścienia włóknistego zostaje wchłoniętych przez nasadę pierścienia kręgu, jednak większość pozostaje dokoła jądra miażdżystego i zostaje włączona w płytkę chrzęstną poprzez włókna Sharpeya. Każdemu z włókien Sharpeya towarzyszy tętniczka i jedno lub więcej włókien nerwowych.
Ryc. 1. Na stan krążka kręgowego mają wpływ płytki graniczne, które łączą go z trzonem kręgu i umożliwiają wymianę substancji.
Płytka chrzęstna zbudowana jest z chrząstki szklistej. Ma ona około 1 mm grubości i pokrywa płytkę graniczną kręgu. Płytka chrzęstna jest unaczyniona, gdyż wnikają w nią drobne naczynia krwionośne z tkanki kostnej kręgu.
Pierścień nie jest unaczyniony. Odżywianie pierścienia i jądra zależne jest więc od dyfuzji płynów z unaczynionej płytki chrzęstnej oraz pozbawionego ukrwienia pierścienia i jądra miażdżystego.
Z klinicznego punktu widzenia najważniejszy jest fakt, że płytka chrzęstna stanowi obszar, w obrębie którego po urazie może dojść do wynaczynienia, podczas gdy nie ma takiej możliwości w obszarze pozbawionego zaopatrzenia krwionośnego pierścienia włóknistego i jądra miażdżystego.
Wspomnieliśmy, że włóknom Sharpeya towarzyszą włókna nerwowe. Bliższe spojrzenie na pierścień ujawnia, że w trzech zewnętrznych warstwach pierścienia włóknistego znajdują się unerwiające je włókna czuciowe. Komórki włókien czuciowych połączonych z krążkiem znajdują się na zewnątrz ośrodkowego układu nerwowego i są umiejscowione w zwoju grzbietowym korzeni rdzeniowych z wielu poziomów kręgosłupa. Krążek L4-L5 unerwiony jest przez zwój grzbietowy korzeni rdzeniowych z T12-L2.
Szlak czuciowy między pierścieniem a zwojem grzbietowym korzeni rdzeniowych utworzony jest przez nerw zatokowo-kręgowy (n. sinuvertebralis) oraz przykręgowy pień współczulny. Bliższe spojrzenie na omawiane włókna czuciowe powoduje jednak, że nie przypisuje się im charakteru nocyceptywnego.
Badania na zwierzętach umocniły pogląd, że zdrowy krążek jest unerwiony na obwodzie głównie przez mechanoreceptory, które uważa się za ważne dla propriocepcji. Rzeczywiście w niektórych badaniach (Inderhal) stwierdzono, że stymulacja zewnętrznej 1/3 pierścienia włóknistego skutkuje dwustronnym skurczem mięśnia wielodzielnego (m. multifidus). To tłumaczyłoby także szybkie męczenie się mięśnia wielodzielnego po urazie pierścienia włóknistego.
Badania na zwierzętach wykazały, że pozostałe włókna czuciowe, które nie są proprioceptywne, to włókna C, które mogą brać udział w nocycepcji. Nie reagują one jednak na bodźce mechaniczne ani cieplne. Reagują na bodźce chemiczne – głównie na mediatory stanu prozapalnego.
Istnieją pewne dowody z badań na zwierzętach, że przed upływem jednego dnia od urazu krążka komórki jądra miażdżystego zaczynają wydzielać TNF oraz IL-1, będące substancjami prozapalnymi. Jednakże sposób, w jaki do tego dochodzi, opisywany jest jako powolny, podzielony na fazy i nie tłumaczy obrazu klinicznego, jaki obserwujemy po ostrym urazie krążka.
Co więcej, jako że unerwienie pochodzi ze zwoju grzbietowego korzeni rdzeniowych górnego odcinka kręgosłupa lędźwiowego, jak już wspominaliśmy, ból – gdyby pochodził z pierścienia włóknistego – byłby tępym, słabo określonym bólem pleców, zupełnie innym niż opisany na początku stanu klinicznego.
Wracając do anatomii, unaczynienia i unerwienia poszczególnych części krążka – jedyne, co mogłoby tłumaczyć kliniczny opis objawów u typowego pacjenta z tylno-boczną wypukliną krążka, to sytuacja, gdy włókna Sharpeya, obecne w płytce chrzęstnej kręgu, zostają awulsyjnie oderwane od płytki chrzęstnej podczas urazu.
Uszkadzałoby to mocno unerwioną i unaczynioną płytkę chrzęstną, powodując początkowy ból, a nawet odczucie "przełamania", które opisują pacjenci.
Jako że płytka chrzęstna jest unaczyniona, wynaczynienie po jej uszkodzeniu prowadzi do powstania w tym miejscu wysięku, który z czasem musi wejść w kontakt z wychodzącym korzeniem nerwowym. Taki scenariusz musi doprowadzić do wytworzenia się nasilonego chemicznego stanu zapalnego opony twardej i korzenia nerwowego oraz uwrażliwienia korzenia nerwowego na zwiększające się z powodu krwawienia płytki chrzęstnej ciśnienie hydrostatyczne w tym obszarze.
Scenariusz ten tłumaczy również, dlaczego do pojawienia się bólu w kończynie dolnej dochodzi z wielogodzinnym opóźnieniem. Wyjaśnia także powstanie przesunięcia bocznego.
Gdy wysięk osiąga ciśnienie krytyczne, ośrodkowy układ nerwowy nakazuje układowi mięśniowemu przesunąć ciężar górnej części ciała poza obszar objęty urazem. Klinicznie skutkuje to powstaniem przesunięcia bocznego, które pojawia się 8–12 godzin po pierwotnym wypadku.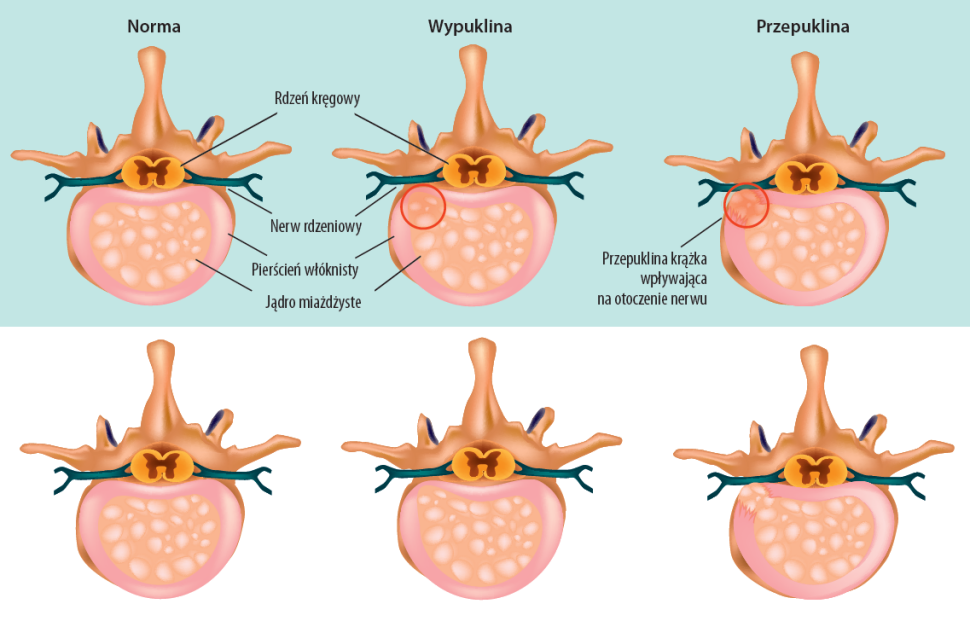
Szybka i skuteczna interwencja w przypadku urazu krążków lędźwiowych
Ma to istotne znaczenie w postępowaniu klinicznym z pacjentem z ostrą tylno-boczną wypukliną krążka – przy lepszym rozumieniu tej patologii popularny protokół McKenziego staje się jeszcze ważniejszy w leczeniu tego problemu zdrowotnego.
Gdy pacjent jest już w stanie się wyprostować, rytmiczne półpompki zadziałają niczym pompa naczyniowa, oczyszczając miejsce urazu z zapalnego wysięku i centralizując w ten sposób ból. Jednak ponieważ wiemy, że płytka chrzęstna jest uszkodzona, potrzeba umieszczenia pacjenta w pozycji wyprostowanej jest pilniejsza i nie należy przeprowadzać tego zbyt wolno.
Gdy pacjent znajdzie się w gabinecie i zdiagnozujemy u niego tę patologię, konieczna jest jak najszybsza korekcja przesunięcia bocznego i umieszczenie pacjenta w pozycji wyprostowanej. Pacjent może leżeć na brzuchu na kilku poduszkach i wtedy można przeprowadzić bezobciążeniową korekcję przesunięcia bocznego.
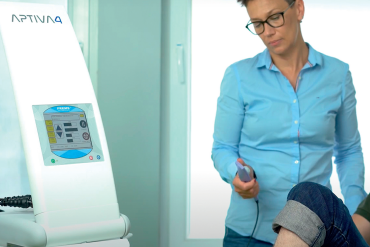
Do wytworzenia pompy mięśniowej i wspomożenia ruchu wyprostu można wykorzystać elektryczną stymulację mięśni. Umieszczenie elektrod nad miejscem urazu i ustawienie stymulatora na 100 pps, po 10 sekund z 10-sekundowymi przerwami, ułatwi skurcze mięśnia prostownika grzbietu i mięśnia wielodzielnego, powodując odcinkowy wyprost na tych poziomach.
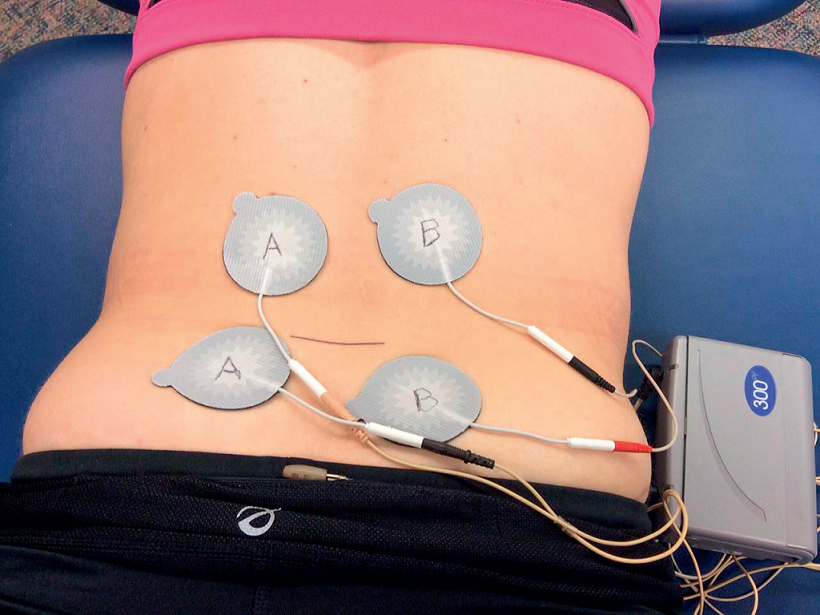
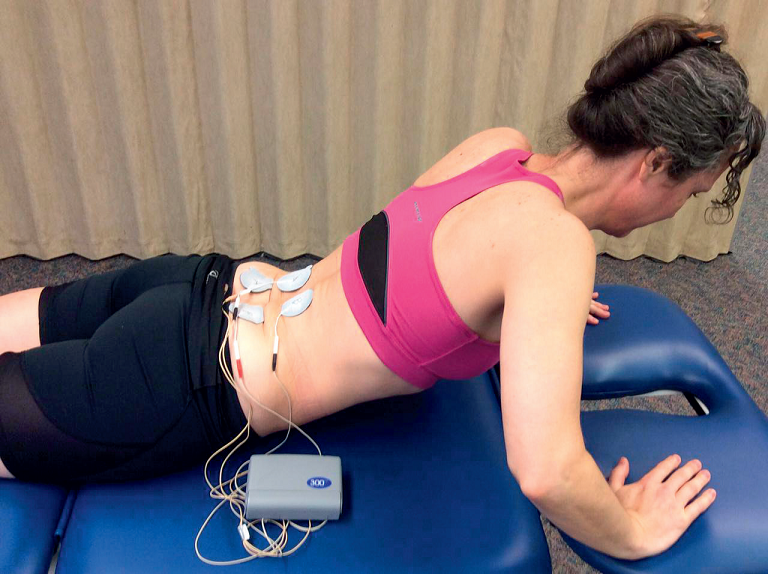
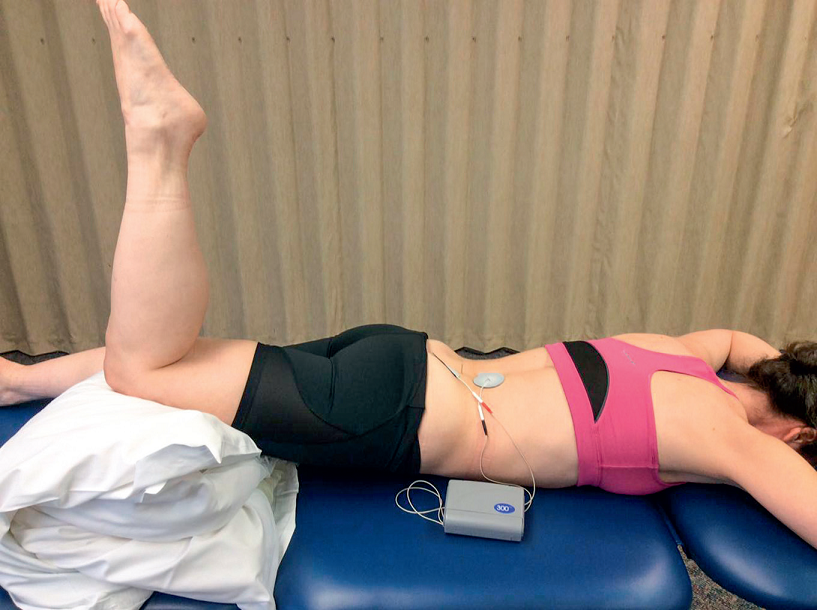
Jeśli pacjent jest w stanie, może również wykonywać półpompki podczas elektrostymulacji (ryc. 2 i 3). Jeśli nie, korzystanie z elektrostymulatora z czasem pomoże pacjentowi przejść do leżenia przodem bez poduszek.
Ryc. 2. Zastosowanie elektrycznej stymulacji mięśni.
Ryc. 3. Półpompki z elektryczną stymulacją mięśni.
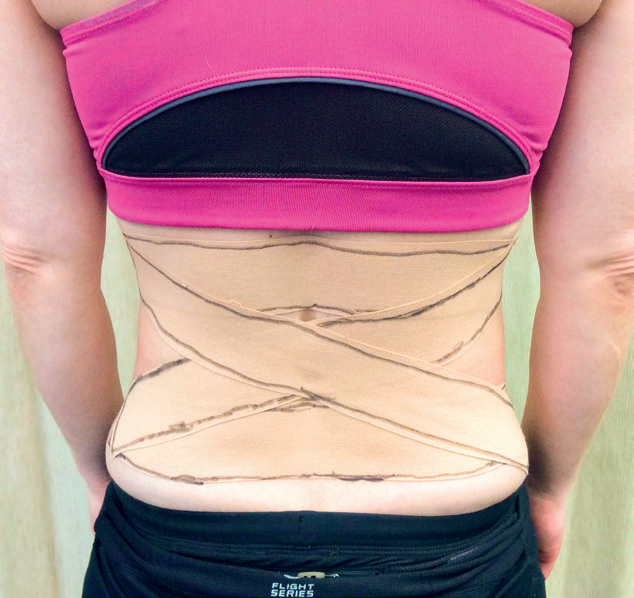
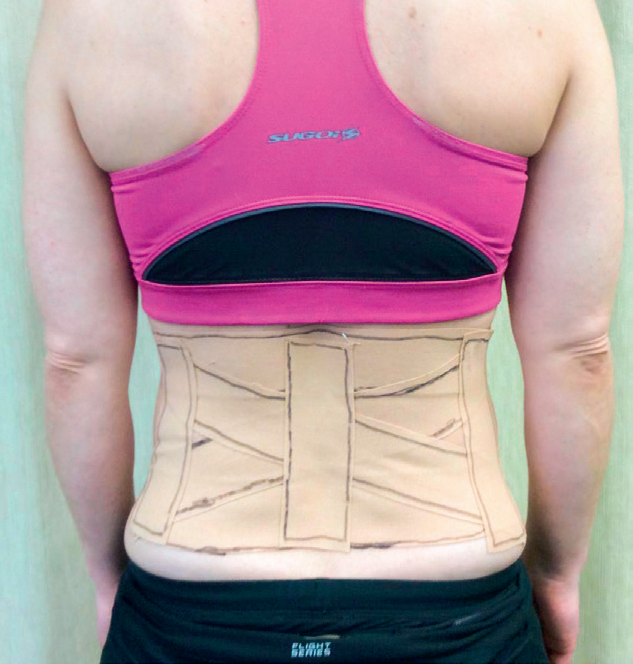
Po każdej sesji elektrostymulacji plecy należy otejpować przy użyciu i zalecić niezdejmowanie jej aż do następnej wizyty (ryc. 4 i 5).
Należy pacjenta poinstruować także, aby w miarę możliwości unikał siedzenia i schylania się, by nie doszło do dalszych uszkodzeń pozostałych włókien pierścienia włóknistego w płytce chrzęstnej. Pacjent ma jak najczęściej leżeć na brzuchu i wykonywać półpompki w sposób zalecony przez fizjoterapeutę.
Gdy pacjent może już pozostawać w pozycji wyprostowanej i regularnie wykonywać w domu półpompki, ze stosowania taśmy można zrezygnować. Może to zająć 2–4 tygodnie.
Ryc. 4. Pierwsza warstwa taśmy.
W tym momencie celem biomechanicznym jest upewnienie się, czy pacjent ma dostęp do odnośnego kwadrantu wyprostu danego segmentu, czyli: jeśli do urazu doszło na wysokości L4/5 po prawej stronie – pacjent powinien być w stanie w pozycji stojącej prostować się, a następnie zginać w prawo w pełnym zakresie tego ruchu kombinowanego. By wspomóc ten ruch, można ponownie skorzystać z elektrostymulacji, tym razem tylko z dwiema elektrodami po stronie urazu.
Do aktywacji mięśni lędźwiowych z danej strony – w celu wykonania skłonu bocznego w tę stronę – kolano tej samej strony umieszcza się na twardym wałku, co umożliwia rozciągnięcie ipsilateralnych mięśni lędźwiowych. Użycie stymulatora, ustawionego nadal na 100 pps, z interwałami pracy/odpoczynku długości 10/10, wywoła izometryczny skurcz mięśni lędźwiowych poprzez naciśnięcie kolanem na wałek. Po tej procedurze mięśnie lędźwiowe wykonają pożądany ruch wyprostu po stronie z urazem oraz zgięcia bocznego kręgosłupa wraz z mięśniami prostownikami, aktywowanymi przez stymulację elektryczną (ryc. 6).
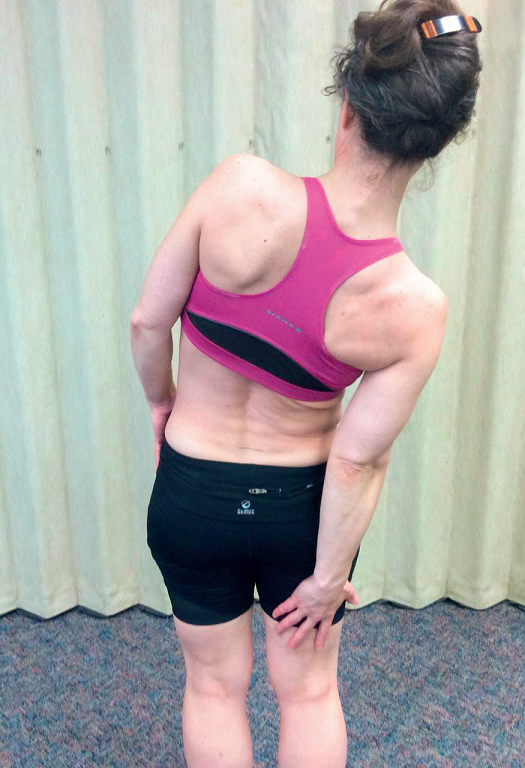
Po tych zabiegach pacjent może wykonywać w domu półpompki z taką samą aktywacją mięśni lędźwiowych, jaką uzyskano w gabinecie przy pomocy stymulatora. Może też wykonywać na stojąco ćwiczenia prostowania i bocznego zginania strony z urazem (ryc. 7).
Ryc. 6. Aktywacja jednostronnego wyprostu z prawej strony.
Ryc. 7. Ćwiczenie w domu – jednostronny wyprost po prawej stronie.
Ostatnia kliniczna implikacja tej patologii dotyczy czasu, jaki może upłynąć do wyzdrowienia. Jeśli przyjmiemy teorię, że uraz polega na oderwaniu awulsyjnym pierścienia włóknistego od płytki chrzęstnej, w patologii tej bierze udział struktura kostna. Podnoszenia ciężkich przedmiotów należy zaniechać przez jeszcze dłuższy okres. To wyjaśnienie pomoże nam pogłębić nasze zrozumienie ostrej tylno-bocznej wypukliny krążka.
Ale co z pacjentami z bardziej przewlekłymi stanami, którzy zgłaszają się z objawami powodowanymi przez krążek? Istnieją dowody, że w przypadku, gdy opisany powyżej scenariusz zrealizuje się w odniesieniu do pierścienia włóknistego i jądra miażdżystego – długoterminowe konsekwencje obejmują wrastanie w obszar urazu nowych włókien czuciowych.
W badaniu przeprowadzonym przez Freemonta i in. odkryto, że w przewlekłym bólu pleców dochodzi do wrastania nerwów w chory krążek międzykręgowy. Badanie to ujawniło, że spośród 30 pacjentów z chorobą krążka międzykręgowego i dodatnim wynikiem dyskografii:
- u 83% stwierdzono wrastanie włókien nerwowych w obszarze zewnętrznej 1/3 krążka międzykręgowego lub głębiej,
- u 77% obejmowało ono także środkową 1/3 lub głębsze warstwy,
- a u 57% nowe włókna nerwowe docierały do 1/3 wewnętrznej pierścienia włóknistego lub nawet do jądra miażdżystego.
- U osób bez objawów liczby te wyniosły odpowiednio: 26%, 6% i 0%.
Specyfika nowo wrastających włókien polega na tym, że uwalniają one wyłącznie substancję P, która każe nerwom wysyłać informację o bólu do ośrodkowego układu nerwowego. W krążkach z wrastaniem nerwów obserwuje się podwyższony poziom mediatorów stanu zapalnego, takich jak prostaglandyna E, które mogą zmieniać wrażliwość nocyceptorów. W tkankach stwierdzono również podwyższony poziom TNF, IL-1B oraz czynnika wzrostu nerwów (NGR) – wszystkie te substancje są mediatorami stanu zapalnego.
W rezultacie dochodzi do sensytyzacji nocyceptorów i indukcji zwiększonego wytwarzania cytokin w innych komórkach. To z kolei nasila wydzielanie substancji zapalnych i powoduje uogólnioną sensytyzację ośrodkowego układu nerwowego, nasilając ból odczuwany przez pacjenta, doprowadzając do hiperalgezji i allodynii.
Jest to istotne klinicznie, jako że większość badań wykazuje, iż terapia manualna, ćwiczenia i edukacja na temat bólu zmniejszają ten rodzaj przewlekłego niespecyficznego bólu dołu pleców, czyli stanowią metody interwencji u tych pacjentów.
Zmiany w krążkach według Modica i ich implikacje
Ostatnim czynnikiem istotnym z punktu widzenia klinicysty leczącego pacjentów z przewlekłym bólem dołu pleców – będącym najprawdopodobniej wynikiem choroby krążka międzykręgowego lub skutkiem mającej miejsce w przeszłości ostrej tylno-bocznej wypukliny krążka – jest kwestia, czy badania obrazowe pacjenta wykazują zmiany zwyrodnieniowe według Modica.
Odzwierciedlają one zmiany w szpiku kostnym – obrzęki w obrębie samej kości kręgu, zwykle w rejonie płytki chrzęstnej, rozprzestrzeniające się ku wnętrzu kości kręgu. Istnieją trzy typy zmian według Modica do jakich może dochodzić w kości kręgu.
Typy zmian w kości kręgu według Modica
- Typ I wiąże się z przerwaniem ciągłości i pojawieniem się szczelin w płytkach granicznych oraz wytworzeniem się ziarnistej tkanki włóknisto-naczyniowej. Ten etap uważa się za zapalne stadium choroby krążka międzykręgowego.
- Typ II wiąże się ze stłuszczeniem czerwonego szpiku kostnego i zastąpieniem go żółtym szpikiem, co stanowi stabilne i przewlekłe stadium choroby krążka międzykręgowego.
- Typ III to stadium sklerotyzacji, czyli kostnienia.
Jeśli chodzi o kliniczne implikacje zmian zwyrodnieniowych według Modica, stwierdza się, że zmiany typu I związane są z bólem dołu pleców.
Braithwaite i in. odkryli, że czułość, specyficzność oraz pozytywna wartość predykacyjna zmian według Modica jako markera bolesnego krążka wynoszą odpowiednio: 23,3%, 96,8% i 91,3%. Dlatego też zmiany według Modica, zwłaszcza typu I, wydają się specyficzną, ale stosunkowo mało wrażliwą oznaką bolesnego krążka lędźwiowego u pacjentów z powodowanym przez krążek bólem w dole pleców.
Kjaer i in. zgodzili się z tymi obserwacjami, a Toyone i in. zauważyli, że 73% pacjentów ze zmianami typu I doświadczało bólu dolnej partii pleców. Toyone i in. stwierdzili także, że 70% pacjentów ze zmianami typu I według Modica – ale jedynie 16% pacjentów ze zmianami typu II – miało odcinkową hipermobilność, określaną jako co najmniej 3-mm translacja w płaszczyźnie strzałkowej, widoczna w dynamicznym obrazowaniu ruchu zgięcia i wyprostu.
Inne badania kwestionowały te ustalenia, ale po podsumowaniu wszystkich badań generalnie można zgodzić się ze stwierdzeniem, że zmiany typu I według Modica powiązane są z odcinkową hipermobilnością. Odcinkowa hipermobilność wiąże się również z bólem dołu pleców, tak więc u pacjenta z chorobą krążka międzykręgowego i zmianami według Modica odcinkowa hipermobilność odgrywa pewną rolę w utrzymującym się bólu w dole pleców i uzasadnia potrzebę ćwiczeń stabilizujących.
W innym, nowszym badaniu Henne i in. przyjrzeli się leczeniu zmian według Modica za pomocą antybiotykoterapii. Podwójnie zaślepione randomizowane badanie z grupą kontrolną objęło 162 pacjentów bez żadnych zdiagnozowanych chorób innych niż ból dołu pleców utrzymujący się od ponad 6 miesięcy.
Tych pacjentów, u których stwierdzono zmiany typu I według Modica, poddano 100-dniowej antybiotykoterapii (Bioclavid – amoksycylina z kwasem klawulonowym) lub leczeniu placebo. W grupie przyjmującej antybiotyk zaszła bardzo znacząca statystycznie poprawa wszystkich wyników, która utrzymywała się od kontroli po 100 dniach do kontroli po roku.
Liczne badania nad tkanką jądra pochodzącą z pękniętych krążków wykazały obecność drobnoustrojów beztlenowych o niskiej zjadliwości, głównie Propionibacterium acnes, u 7–53% pacjentów. W momencie powstania przepukliny, czy raczej oderwania awulsyjnego pierścienia włóknistego od płytki chrzęstnej, owe mało zjadliwe bakterie beztlenowe mogą przedostać się do krążka i wywołać podstępną infekcję. Jedyna ścieżka dostępu tych bakterii do krążka jest pochodzenia naczyniowego, co dodatkowo potwierdza teorię, że ostre uszkodzenie krążka wiąże się z awulsyjnym pęknięciem płytki granicznej.
Wysięk zapalny i miejscowy stan zapalny mogą nawet rozprzestrzeniać się na przyległą kość. Może być to efekt wtórny, wywołany przez wytwarzanie cytokin i kwasu propionowego. Odkryto, że kwas propionowy doprowadza do mikropęknięć otaczającej kości.
Dlatego też u pacjentów, u których podejrzewa się przewlekły ból dołu pleców po urazie krążka w przeszłości lub ze zdiagnozowaną chorobą krążka międzykręgowego, należy wykonywać rezonans magnetyczny, jeśli nie reagują oni w spodziewany sposób na leczenie fizjoterapeutyczne.
Urazy międzykręgowe krążków lędźwiowych - podsumowanie
Konkludując, brak jest dowodów na to, że uwypuklony krążek styka się z korzeniem nerwowym i daje typowy wzorzec kliniczny ostrej tylno-bocznej wypukliny. Wydają się natomiast istnieć dowody, że uraz związany z awulsyjnym oderwaniem włókien Sharpeya od płytki chrzęstnej powoduje powstanie zapalnego wysięku obejmującego oponę twardą i pobliski korzeń nerwowy.
Wiedza ta podkreśla potrzebę pilnego zajęcia się tymi pacjentami przez fizjoterapeutę w celu wdrożenia u nich szybkiego i progresywnego leczenia w kierunku wyprostu. Podczas wizyty pacjenta z przewlekłym bólem krążka fizjoterapeuta powinien pamiętać o wrastaniu nowych włókien nerwowych w uszkodzony krążek, co powoduje uogólnioną sensytyzację danego obszaru.
Ponadto im bardziej nasilona jest choroba krążka międzykręgowego u danego pacjenta, tym większą rolę w wywoływaniu bólu dolnej partii pleców może odgrywać odcinkowa hipermobilność, co wskazuje na potrzebę stabilizacji kręgosłupa.
Wreszcie u pacjentów przewlekłych, których stan się nie poprawia – mimo edukacji na temat bólu, leczenia sensytyzacji, terapii manualnej i ćwiczeń – zalecany jest rezonans magnetyczny w kierunku zmian według Modica.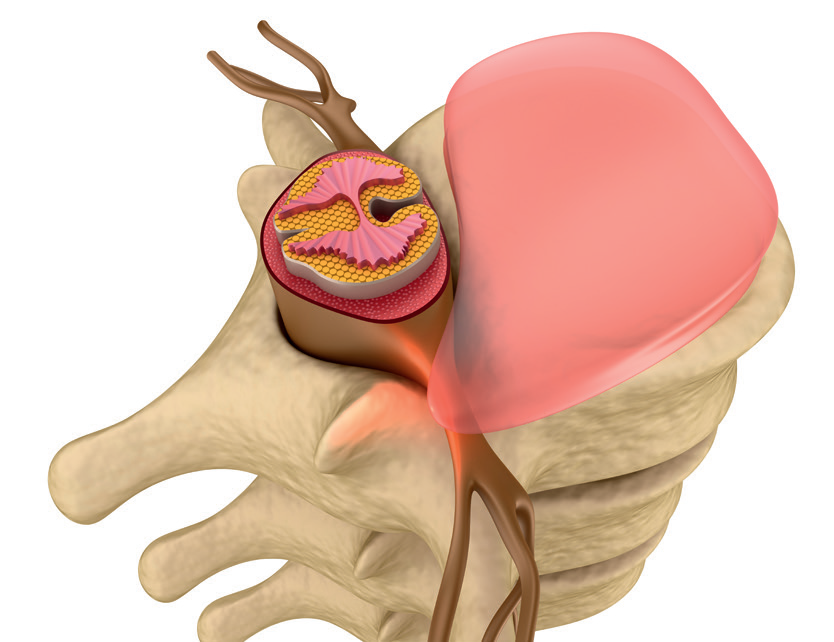
- Orita et al. Direct evidence for sensory innervation of dorsal portion of Co5/6 coccygeal disc in intervertebral discs in rats. Spine. Vol 35,(14):1346-1352, 2010
- Kallewaard et al. Discogenic low back pain. Pain Practice. Vol 10;(6):560-579, 2010.
- Role of the sinuvertebral nerve in LBP and anatomical basis of therapeutic implications. Surgical Radiol Anatomy. Feb(24):366-71. 2003.
- Schliessbach J, Siegenthaler A, Heini P, Bogduk N, Curatolo M. Blockade of the sinuvertebral nerve for diagnosis of lumbar discogenic pain: an exploratory study. Anaesthesia and Analgesia. Vol.111, (1):204-206. July 2010.
- Hsu P, Armon C, Levin K. Lumbosacral radiculopathy: pathophysiology, clinical features and diagnosis; www.uptodate.com; Jan. 11, 2011.
- Sugiura A, et al. Existence of nerve growth factor receptors tyrosine kinase A and p75 neurotrophin receptors in intervertebral discs and on dorsal root ganglion neurons innervating intervertebral discs in rats. Spine, Vol. 33(19): 2047-2051; 2008.
- Lotz J, Ulrich J. Innervation, inflammation and hypermobility may characterize pathologic disc degeneration: review of animal model data. JBJS. Vol. 88A(2):76-82; 2006
- Fagan A et al. Innervation of annular tears: an experimental animal study. Spine, Vol. 35(12):1200-1210; 2010.
- Freemont AJ, et al. Nerve in-growth into the diseased intervertebral disc (DDD) in chronic back pain. Lancet, 350:178-81; 1997.
- Ozawa T et al. The degenerated lumbar intervertebral disc is innervated primarily by peptide containing sensory nerve fibers in humans. Spine, Vol. 31(21): 2418-2422; 2006.
- Fagan A et al. ISSLS prize winner: the innervation of the intervertebral disc: a quantitative analysis. Spine, Vol. 28(23): 2570-2576; 2003.
- Edgar MA. The nerve supply of the intervertebral disc. JBJS, Vol. 89b(9): 1135-1139; 2007.
- Rahme R, Moussa R. The modic vertebral endplate and marrow changes: pathological significance and relation to lower back pain and spinal instability of the lumbar spine. Am J Neuroradiol 29:838-42; 2008