Stwardnienie rozsiane to najpowszechniej występująca choroba demielinizacyjna, będąca jednocześnie chorobą autoimmunologiczną. Należy ona do chorób neurologicznych i powoduje niepełnosprawność pacjenta. Kobiety chorują dwa razy częściej niż mężczyźni. Według danych z 2020 roku na stwardnienie rozsiane choruje 2,8 mln osób na świecie, a globalna częstość występowania wynosi 39,5 na 100 tys. osób1. Polska należy do krajów o wysokiej częstości występowania choroby, ponieważ zapada na nią u nas od 45 do 92 osób na 100 tys. mieszkańców2.
Stwardnienie rozsiane - charakterystyka choroby
W przebiegu stwardnienia rozsianego (łac. sclerosis multiplex – SM) układ odpornościowy organizmu atakuje centralny układ nerwowy, czyli mózg i rdzeń kręgowy, a także nerwy wzrokowe. W wyniku stanu zapalnego wywołanego przez układ immunologiczny dochodzi do uszkodzenia mieliny (substancji chroniącej włókna nerwowe), samych włókien nerwowych oraz komórek wytwarzających mielinę. Uszkodzenia te doprowadzają do zakłócenia lub zupełnego zatrzymania przepływu informacji w obrębie centralnego układu nerwowego.
Choć nie ma dwóch pacjentów z dokładnie takimi samymi objawami, identyfikuje się najczęstsze symptomy choroby, do których należą: dyzestezja, zmęczenie, osłabienie, problemy z chodzeniem, spastyczność, drętwienie lub mrowienie, problemy ze wzrokiem, zawroty głowy, problemy z pęcherzem, problemy z jelitami, zaburzenia funkcji seksualnej, ból i swędzenie, zmiany poznawcze, zmiany emocjonalne oraz depresja3.
Przyczyny stwardnienia rozsianego wciąż są nieznane, przypuszcza się jednak, że chorobę wywołuje połączenie genetycznej podatności, nieprawidłowości układu odpornościowego oraz czynników środowiskowych. Do tych ostatnich zalicza się: przebycie infekcji wirusem Epsteina-Barr – zwłaszcza objawowej i w okresie dziecięcym, palenie papierosów oraz być może niedobór witaminy D, choć w tym ostatnim przypadku nie udowodniono związku przyczynowo-skutkowego (obserwuje się natomiast powszechność takich niedoborów u pacjentów ze stwardnieniem rozsianym)4. Ważną rolę mogą odgrywać również hormony płciowe, jako że największe nasilenie objawów obserwuje się u kobiet o bardzo wysokim poziomie estradiolu oraz niskim poziomie progesteronu5.
U pacjentów z SM obserwuje się typowo jeden z czterech przebiegów choroby:
- klinicznie izolowany zespół (Clinically Isolated Syndrom – CIS) – pierwszy epizod choroby, trwający co najmniej 24 godziny; jeśli nie towarzyszą mu zmiany w mózgu (można je uwidocznić podczas rezonansu magnetycznego), prawdopodobieństwo rozwinięcia pełnoobjawowego stwardnienia rozsianego jest o wiele niższe niż u osób z widocznymi zmianami;
- postać rzutowo-remisyjna SM (relapsing-remitting multiple sclerosis – RRMS) – najczęstsza postać choroby, charakteryzująca się występowaniem na przemian okresów pogorszenia i poprawy; przy tej postaci choroba w danym momencie może być aktywna lub nieaktywna, pogarszająca się lub niepogarszająca się;
- postać wtórnie postępująca (secondary progressive multiple sclerosis – SPMS) – następuje po postaci rzutowo- remisyjnej i charakteryzuje się pogarszaniem się funkcji neurologicznej;
- postać pierwotnie postępująca (primary progressive multiple sclerosis – PPMS) – występuje, jeśli u pacjenta już od pojawienia się pierwszych objawów stale pogarszają się funkcje neurologiczne, bez okresów remisji; postać ta dotyka ok. 15% pacjentów z SM6.
Leczenie farmakologiczne stwardnienia rozsianego
Według zaleceń Polskiego Towarzystwa Neurologicznego podstawowymi lekami stosowanymi podczas rzutów stwardnienia rozsianego są glikokortykosteroidy, których podawanie powoduje szybsze ustępowanie objawów neurologicznych poprzez ograniczanie procesu zapalnego i hamowanie syntezy przeciwciał IgG. W przypadku braku poprawy lub występowania przeciwwskazań do stosowania glikokortykosteroidów rozważa się użycie plazmaferezy lub immunoglobulin.
Natomiast lekami modyfikującymi przebieg choroby są: interferony beta, octan glatirameru, fumaran dimetylu, teryflunomid i alemtuzumab (leki pierwszego wyboru) oraz natalizumab, fingolimod i mitoksantron (leki drugiej linii).
Leczenie objawowe SM
Oprócz wyżej wymienionych form leczenia pacjenci ze stwardnieniem rozsianym powinni być objęci leczeniem objawowym – zarówno farmakologicznym, jak i fizjoterapeutycznym oraz psychologicznym. Do dolegliwości wymagających takiej terapii należą zwłaszcza: zwiększenie napięcia mięśni (spastyczność), niedowład kończyn, ataksja (niezborność), dysfunkcja zwieraczy, ból, zaburzenia psychiczne, zaburzenia funkcji poznawczych, zmęczenie oraz zaburzenia funkcji seksualnej.
Do leków stosowanych w spastyczności należą: baklofen, tyzanidyna, diazepam, klonazepam i kannabinoidy. Jeśli leki pierwszego wyboru nie skutkują, ważną rolę w terapii ograniczonej spastyczności, zwłaszcza mięśni przywodzicieli, mogą odegrać zastrzyki z toksyny botulinowej7.
Toksyna botulinowa w stwardnieniu rozsianym może być pomocna nie tylko przy spastyczności, ale również przy problemach z nietrzymaniem moczu. W przeglądzie badań z 2017 roku czytamy, że istnieją dowody poziomu B (prawdopodobnie skuteczne) odnośnie do użyteczności domięśniowych zastrzyków tej toksyny przy spastyczności w SM oraz dowody klasy A (skuteczne), że zastrzyki takie – podawane do mięśnia wypierającego pęcherza –poprawiają neurogeniczną nadreaktywność tego mięśnia oraz nadreaktywność pęcherza związaną z chorobą. Pojawiają się też dane z badań niższej klasy sugerujące, że toksyna botulinowa podawana domięśniowo może pomagać w łagodzeniu również innych objawów SM, takich jak ogniskowe skurcze toniczne, ogniskowe miokimie, dysfagia spastyczna oraz podwójne widzenie w porażeniu międzyjądrowym8.
Rola i cele rehabilitacji w stwardnieniu rozsianym
Amerykańskie Narodowe Towarzystwo Stwardnienia Rozsianego zaleca, aby zespół prowadzący rehabilitację osób ze stwardnieniem rozsianym miał w swoim składzie następujących specjalistów:
- fizjoterapeutę – badającego i pracującego nad takimi obszarami jak poruszanie się i funkcjonowanie, z naciskiem na chodzenie, mobilność, siłę, równowagę, postawę, męczliwość i ból; fizjoterapia może obejmować program ćwiczeń, trening chodzenia, trening korzystania z narzędzi ułatwiających poruszanie się oraz ćwiczenia dna miednicy (przy problemach z układem moczowym);
- terapeutę zajęciowego – zapewniającego szkolenie z technik zachowywania energii i korzystania z narzędzi adaptacyjnych ułatwiających wykonywanie czynności życia codziennego; może on także zalecać modyfikacje w domu lub miejscu pracy – dla zwiększenia ich dostępności, wygody i bezpieczeństwa lub zajmować się problemami z myśleniem i pamięcią;
- specjalistę rehabilitacji zawodowej – oferującego szkolenie odnośnie wykonywania pracy i trening mobilności w miejscu pracy (jego celem jest pomoc osobom chorym w utrzymaniu zatrudnienia lub znalezieniu innego, bardziej odpowiadającego nowym potrzebom);
- logopedę – rozwiązującego problemy z mową i połykaniem, jakie mogą nastąpić w wyniku uszkodzenia centralnego układu nerwowego;
- neuropsychologa – leczącego zmiany w zdolnościach poznawczych pacjenta, dotyczące myślenia, rozumowania, pamięci czy skupiania uwagi9.
Według zaleceń Polskiego Towarzystwa Neurologicznego rozpoznanie stwardnienia rozsianego, a nawet prawdopodobne podejrzenie takiego rozpoznania, kwalifikuje pacjenta do rozpoczęcia terapii ruchowej – również w przypadku braku jakichkolwiek objawów neurologicznych. Wcześnie podjęta rehabilitacja ruchowa może poprawić reprezentację motoryczną w ogólnym układzie nerwowym i korzystnie wpływać na przyszłe wzorce ruchowe pacjenta.
Autorzy zaleceń zaznaczają jednocześnie, że osoby ze stwardnieniem rozsianym już w początkach choroby, przy niewielkim nasileniu objawów neurologicznych, muszą zwracać uwagę na to, by bezwzględny czas trwania konkretnego zadania (aktywności ruchowej) był u nich krótszy niż u osób zdrowych.
Poza tym opieka fizjoterapeutyczna musi stanowić nieodłączną część całorocznej opieki nad pacjentem. Konsultacje takie pomagają choremu rozwiązywać problemy funkcjonalne, planować rodzaj i dawkowanie obciążeń fizycznych oraz nauczyć się nowych ćwiczeń ruchowych7.
Według polskich naukowców pracujących pod kierownictwem A.M. Kubsik-Gidlewskiej to właśnie rehabilitacja, obejmująca także leczenie objawowe i psychoterapię, jest uważana obecnie za najlepszą formę leczenia stwardnienia rozsianego10.
Rehabilitację powinna poprzedzać dogłębna ocena diagnostyczna stanu funkcjonalnego pacjenta oraz określenie rokowania co do stanu umysłowego, stanu neurologicznego oraz świadomości pacjenta. Program fizjoterapeutyczny powinien być dostosowany do fazy choroby, stopnia niepełnosprawności pacjenta oraz jego deficytów neurologicznych. Program kinezyterapii powinien uwzględniać zasadę stopniowania ćwiczeń, czyli stopniowe przechodzenie od ruchów podstawowych do bardziej złożonych. Najwłaściwszą formą leczenia jest rehabilitacja funkcjonalna połączona z procedurami fizykoterapeutycznymi, a dodatkowo ostatnio postuluje się konieczność zalecania pacjentom również ćwiczeń aerobowych.
Fizjoterapeuta powinien pamiętać, że wrogiem pacjenta jest bezruch. Dlatego nawet podczas zaostrzenia choroby należy pacjenta mobilizować poprzez częste zmiany pozycji ciała (profilaktyka odleżyn), stosowanie ćwiczeń biernych (profilaktyka przykurczów) oraz wykonywanie ćwiczeń oddechowych (profilaktyka powikłań ze strony układu oddechowego). Ważne jest również zapobieganie infekcjom układu moczowo-płciowego oraz zapewnienie pomocy w czynnościach życia codziennego. W okresach remisji natomiast należy prowadzić fizjoterapię dostosowaną do stanu pacjenta. Poprzez poprawę umiejętności motorycznych chorego staramy się wzmacniać jego siłę mięśni, normalizować napięcie mięśniowe, zwiększać lub utrzymywać zakres ruchu stawów, zapobiegać zanikowi mięśni, poprawiać koordynację i równowagę, przeciwdziałać konsekwencjom unieruchomienia oraz zapobiegać nietrzymaniu moczu10.
Skuteczność różnych form fizjoterapii w SM
Stwardnienie rozsiane to choroba dotykająca układ nerwowy, dlatego w jej leczeniu szczególne znaczenie mają metody neurofizjologiczne, takie jak torowanie nerwowo- mięśniowe, terapia NDT-Bobath, biofeedback, mobilizacja i reedukacja chodu.
W badaniu irańskim z 2020 roku sprawdzano skuteczność torowania nerwowo-mięśniowego połączonego z ćwiczeniami wyobrażania umysłowego lub pamięci roboczej (lub z oboma tymi typami ćwiczeń). Wszystkie te połączenia okazały się skutecznie wpływać na równowagę dynamiczną, zakres ruchu stawu kolanowego oraz jego spastyczność u pacjentów ze stwardnieniem rozsianym. Nie zaobserwowano znaczących różnic między grupami – wszystkie te rodzaje ćwiczeń były równie efektywne11. W nieco wcześniejszym badaniu, również z Iranu, stwierdzono, że 8-tygodniowy program torowania nerwowo-mięśniowego i treningu oporowego znacząco zmniejszył męczliwość i poprawił jakość życia (zarówno komponentu fizycznego, jak i psychicznego) u pacjentów z SM12.
Terapia NDT-Bobath początkowo była stosowana u osób z porażeniem mózgowym, ale znajduje również inne zastosowania. W badaniu z 2019 roku czytamy, że dowody z ostatnich lat wykazały skuteczność tej terapii w poprawianiu funkcjonowania i mobilności pacjentów z SM. Cytowane badanie również potwierdziło skuteczność tej metody w owych obszarach, nie zaobserwowano jedynie żadnego jej korzystnego wpływu na spastyczność13.
W badaniu australijskim z 2015 roku sprawdzono skuteczność biofeedbacku jako interwencji psychologicznej dodanej do technik relaksacji, uważności, społecznego wsparcia i edukacji. Okazało się, że w grupie stosującej biofeedback zaobserwowano widoczne zmniejszenie poziomu lęku, zmęczenia i stresu w porównaniu z grupą kontrolną. Metoda ta przyniosła również takie korzystne zmiany jak zmniejszenie tempa oddychania i niższe napięcie mięśniowe14.
Neurofeedback to terapia wykorzystująca elektroencefalografię do nauczenia pacjenta wytwarzania fal mózgowych o pożądanych wzorcach. Badanie kliniczne z 2015 roku wykazało, że neurofeedback znacząco zmniejsza zmęczenie i objawy depresyjne u osób ze stwardnieniem rozsianym. Efekty leczenia utrzymywały się podczas kontroli przeprowadzonej dwa miesiące po jego zakończeniu15.
W przeglądzie badań z 2016 roku, przeprowadzonym pod kierownictwem E. Campbella, sprawdzano skuteczność różnych typów rehabilitacji u osób z postępującym stwardnieniem rozsianym. Jednym z nich jest fizjoterapia jako część multidyscyplinarnego programu rehabilitacyjnego. Taki sześciotygodniowy program zmniejszał niepełnosprawność uczestników, mierzoną skalą niezależności funkcjonalnej (FIM – functional independence measure), choć nie wpływał na wyniki Rozszerzonej Skali Niepełnosprawności (EDSS – expanded disability status scale).
W dwóch badaniach elektrostymulacja funkcjonalna lepiej wpłynęła na układ mięśniowo-szkieletowy oraz redukcję upadków niż domowy plan ćwiczeń mający na celu poprawę stabilności. Natomiast w jednym z tych badań elektrostymulacja funkcjonalna poprawiła również jakość chodu, podczas gdy w drugim na szybkość i wytrzymałość podczas chodzenia lepiej wpłynął plan ćwiczeń domowych – rozbieżność ta może wynikać z różnic w projektach owych badań (np. w badaniu pierwszym stymulacji poddawano nie tylko mięśnie strzałkowe, ale również pośladkowe).
Jeśli chodzi o terapię ćwiczeniową, dwa badania sprawdziły skuteczność treningu wytrzymałościowego w środowisku klinicznym, a jedno – skuteczność treningu oporowego i ćwiczeń funkcjonalnych w środowisku domowym. Trening wytrzymałościowy okazał się poprawiać kondycję fizyczną, ale tylko w jednym z dwóch badań poprawa ta była znacząca. Ponadto w jednym z badań zaobserwowano także znaczącą poprawę odnośnie do mobilności, depresji, zmęczenia, a w drugim – poprawę siły mięśni i zmniejszenie zaburzeń lękowych. Ponownie rozbieżności te mogą być wynikiem różnic między protokołami badań (np. różnym poziomem niepełnosprawności uczestników).
Wyniki badań potwierdzają również skuteczność terapeutyczną połączenia zastrzyków z toksyny botulinowej oraz rozciągania manualnego, choć nie wskazują, jaki rodzaj połączenia byłby najkorzystniejszy – czy zastrzyki z samym rozciąganiem, czy również z segmentowymi wibracjami mięśni. Wiadomo jedynie, że każde połączenie działa lepiej od samych zastrzyków. Terapia łącząca zastrzyki z rozciąganiem manualnym przynosiła zmniejszenie spastyczności, ale także poprawę subiektywnej oceny objawów, mniejsze zmęczenie i usprawnienie czynności życia codziennego. Zmniejszenie spastyczności utrzymywało się sześć tygodni po interwencji, ale 18 tygodni po leczeniu nie było już widoczne. Natomiast zmniejszenie spastyczności osiągnięte w wyniku leczenia obejmującego również segmentowe wibracje mięśniowe utrzymywało się dłużej.
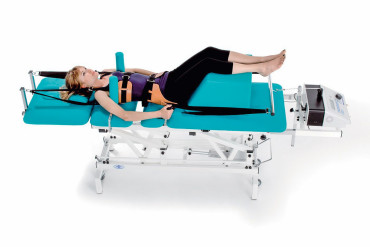
W jednym badaniu porównano stosowanie trenażera mięśni oddechowych z głębokim oddychaniem. Trenażer taki, zwiększający siłę mięśni wdechowych, znacząco zwiększył maksymalne ciśnienie wdechowe oraz maksymalne ciśnienie wydechowe u pacjentów. Tylko w jednym badaniu porównywano skuteczność samego treningu na bieżni z odciążeniem masy ciała z takim treningiem połączonym z zastosowaniem ortez robotycznych. W obu grupach zaobserwowano znaczącą poprawę szybkości chodzenia, wytrzymałości, czasu utrzymywania się na obu kończynach oraz zmniejszenie niepełnosprawności. Czas utrzymywania się na obu kończynach był większy w grupie stosującej sam trening na bieżni niż w grupie z ortezami robotycznymi.
W jednym badaniu porównano stanie terapeutyczne przy użyciu pionizatora z programem codziennych ćwiczeń w domu, obejmującym brzuszki, przetaczanie bioder, przenoszenie kolan w leżeniu na plecach oraz unoszenie miednicy ("mostek"). Okazało się, że stanie terapeutyczne dało znaczącą poprawę zakresu biernego ruchu stawu biodrowego i stawu skokowego oraz zmniejszenie spastyczności w stawie skokowym, natomiast program ćwiczeń przyniósł zmniejszenie częstotliwości skurczów nóg, tak więc najkorzystniejsze wydaje się połączenie obu tych form terapii.
Autorzy przeglądu konkludują, że choć dane z różnych badań często są trudno porównywalne, a siła dowodów niezbyt wysoka, to większość materiału wskazuje na skuteczność fizjoterapii w postępującym stwardnieniu rozsianym16.
Szczególne zalecenia przy SM
U wielu pacjentów z SM może dochodzić do niedowładu w wyniku podniesienia się temperatury ciała. Zjawisko to jako pierwszy zaobserwował niemiecki okulista Wilhelm Uhthoff, wiązał je jednak nie z ciepłotą ciała, a z wykonywanymi ćwiczeniami. Tak naprawdę 60–80% pacjentów z SM doświadcza odwracalnego nasilenia objawów neurologicznych pod wpływem np. energicznej aktywności fizycznej, gorączki lub gorącej kąpieli.
Fizjoterapeuci powinni pamiętać o możliwości wystąpienia efektu Uhthoffa. U pacjentów wrażliwych na ciepło zalecane jest przeprowadzanie treningu rano (fizjologicznie ciepłota ciała jest wtedy niższa) lub w wodzie o temperaturze 27–28ºC. Pomocne może być także schładzanie ciała przed lub w trakcie ćwiczeń. Jeśli i to nie pomaga, trening wytrzymałościowy można zastąpić treningiem oporowym.
U 75–90% pacjentów z SM wraz z postępem choroby dochodzi do męczliwości, która może prowadzić do błędnego koła: rezygnacja z ćwiczeń (z powodu męczliwości) będzie skutkować jeszcze większą męczliwością. Najlepszy wpływ na to zjawisko ma schładzanie ciała oraz stosowanie ćwiczeń o umiarkowanej intensywności, zwłaszcza aerobowych. Jako że zmęczenie rośnie z upływem dnia, zalecane jest przeprowadzanie ćwiczeń przed południem oraz nieprzeciążanie pacjenta. Pomóc może również zwiększenie motywacji do treningu poprzez wsparcie psychologiczne lub ćwiczenia w grupie. Użyteczne są też strategie oszczędzające energię, dzięki którym pacjenci uczą się wykonywać codzienne czynności z minimalnym wysiłkiem17.
Pomocne formy fizykoterapii przy SM
Planując rehabilitację osoby ze stwardnieniem rozsianym, należy pamiętać o tym, że pozytywne efekty przynosi poprzedzenie kinezyterapii jakąś formą fizykoterapii. Należy również zwracać uwagę, aby wysiłek fizyczny nie był dla pacjenta zbyt duży, ponieważ może to zwiększyć i tak już zbyt duże napięcie mięśni18. Dobrą metodą fizykoterapii przed ćwiczeniami jest krioterapia. Schładza ona określone obszary ciała, dzięki czemu osiągany jest efekt miejscowego znieczulenia, a także zmniejsza się możliwość wystąpienia efektu Uhthoffa.
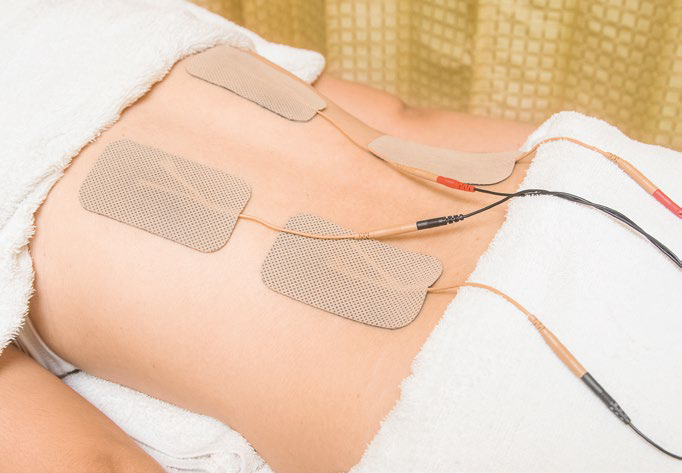
Często stosowane w stwardnieniu rozsianym są różne rodzaje elektroterapii. Dzieje się tak, ponieważ stymulacja elektryczna wydaje się być bardzo dobrym rodzajem leczenia, uszkodzenia górnego neuronu ruchowego nie zmieniają bowiem pobudliwości mięśni pod wpływem bodźców elektrycznych. Dzięki temu można zastąpić bioelektryczną funkcję mięśni zastosowaniem urządzeń elektrycznych. Stymulację elektryczną przeprowadza się za pomocą zaimplantowanych elektrod (ten sposób wiąże się z ryzykiem powikłań takich jak przemieszczenie elektrody lub niepożądana reakcja organizmu na implant) lub metod przezskórnych. Niezależnie od sposobu zastosowania osiąga się zmniejszenie napięcia mięśni, a dzięki niemu – większy zakres ruchu stawów i lepszą jakość chodu.
Do metod elektroterapeutycznych stosowanych w stwardnieniu rozsianym należy wspomniana już elektrostymulacja funkcjonalna. Stosuje się w niej ministymulatory pobudzające sparaliżowane mięśnie będące poza kontrolą ośrodkowego układu nerwowego, a najczęstszym zastosowaniem elektrostymulacji funkcjonalnej jest leczenie uszkodzonego nerwu strzałkowego u pacjentów z paraliżem połowicznym w celu poprawy różnych faz chodu.
Przezskórna elektrostymulacja nerwów, czyli TENS (transcutaneous electrical nerve stimulation) stosowana jest w stwardnieniu rozsianym jako sposób łagodzenia bólu. Elektrody umieszcza się w miejscach dotkniętych bólem lub wzdłuż nerwów; czasem stosuje się układ segmentalny, aplikowany na dany dermatom (obszar unerwiany przez nerw rdzeniowy danego odcinka rdzenia kręgowego).
Częstotliwości mieszczą się w przedziale od 1 do 100 Hz, a intensywność zależy od indywidualnych odczuć pacjenta. W kanadyjskiej metaanalizie z 2015 roku stwierdzono, że terapia TENS skutecznie i bezpiecznie zmniejsza ból uogólniony u pacjentów z SM. Efekt ten był niezależny od zastosowanej częstotliwości i od metody pomiaru bólu20.
Popularnym rodzajem elektroterapii jest metoda Hufschmidta, która normalizuje napięcie mięśniowe poprzez stymulację mięśni spastycznych i ich antagonistów. Umożliwia ona torowanie proprioceptywne i wpływa na motoneurony alfa21.
Elektrostymulacja nerwowo-mięśniowa, czyli NMES (neuromuscular electrical stimulation) to dobrze tolerowana metoda fizykoterapii wspomagająca regenerację mięśniowo- -szkieletową, stosowana w celu zmniejszenia skurczów mięśni, bólów mięśni oraz ich atrofii wywołanej nieużywaniem. W serii opisów przypadków, opublikowanej w 2010 roku, terapia NMES dała mierzalne korzyści w zakresie funkcji chodzenia u pacjentów z wtórnie postępującą i pierwotnie postępującą postacią stwardnienia rozsianego22.
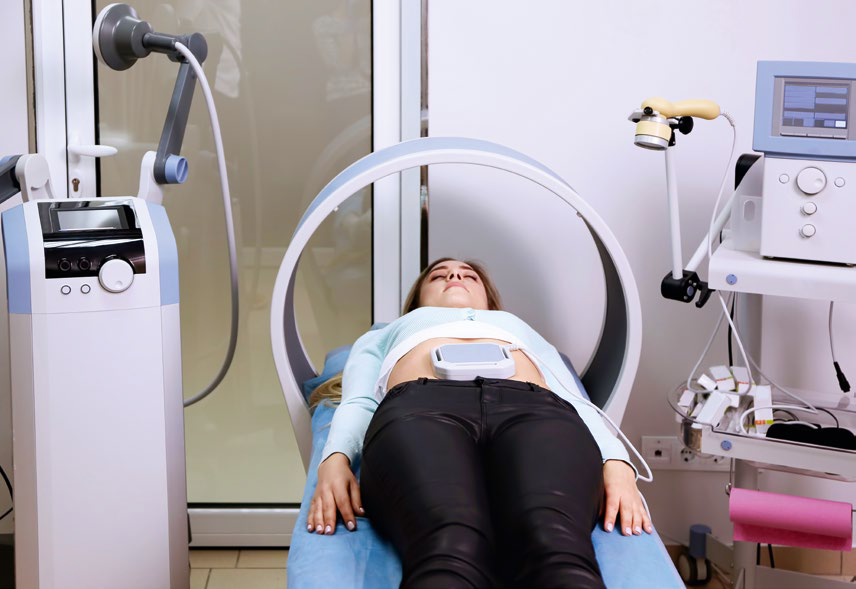
Inną formą fizykoterapii pomocną w SM jest magnetoterapia. Pozwala ona na bezbolesną penetrację tkanek. Stosowane impulsy – o trójkątnym, prostokątnym, sinusoidalnym lub trapezoidalnym kształcie fali – mogą mieć częstotliwość od 2 do 60 Hz, a intensywność może wynosić do 20 mT (przy intensywności nieprzekraczającej 100 μT mówimy o magnetycznej stymulacji)23.
Magnetoterapia przynosi pacjentom z SM ulgę w bólu i zmniejsza napięcie mięśni. Działanie przeciwbólowe polega tutaj po pierwsze na stymulacji wydzielania opiatów endogennych z grupy beta-endorfin dzięki hiperpolaryzacji zakończeń nerwowych, a po drugie – na redukowaniu przepuszczalności błon komórkowych24. W niewielkim badaniu klinicznym z 2016 roku ustalono, że magnetoterapia (o intensywności 4 mT, częstotliwości 15 Hz i sinusoidalnym kształcie fali) może również łagodzić parestezje stanowiące jeden z objawów stwardnienia rozsianego25.
Natomiast stymulacja magnetyczna ogólnie sprzyja nasileniu procesów życiowych i utrzymywaniu homeostazy. W stwardnieniu rozsianym najczęściej stosowana jest ogólnoustrojowa stymulacja magnetyczna, która przynosi zmniejszenie napięcia mięśni i odprężenie, przyczyniające się do łagodzenia męczliwości. Badania potwierdzają, że ta forma terapii skutecznie pobudza wydzielanie melatoniny, która wiąże się z efektem przeciwbólowym, oraz serotoniny, która pozytywnie wpływa na nastrój26. Specyficzną formą tej fizykoterapii jest przezczaszkowa stymulacja magnetyczna. Według hiszpańskiego systematycznego przeglądu literatury z 2020 roku poddanie mózgu działaniu impulsów elektromagnetycznych pozwala na optymizację aktywności tego organu, w tym – poprawę transmisji impulsów nerwowych w zdemielinizowanym centralnym układzie nerwowym. Liczne badania nad przezczaszkową stymulacją magnetyczną wykazały statystycznie znaczącą poprawę odnośnie do takich objawów jak męczliwość, spastyczność, dysfunkcja dolnych dróg moczowych, obniżona sprawność manualna, pogorszenie chodu oraz deficyty poznawcze związane z pamięcią roboczą. Korzyści te opierają się prawdopodobnie na mechanizmie sprzyjania regeneracji mózgu poprzez neuroplastyczność. W badaniach na zwierzętach ustalono, że taka stymulacja skutecznie łagodzi zaburzenia ruchowe, zmniejsza proliferację astrocytów po ataku autoimmunologicznym, zwiększa gęstość komórek mózgu i zmniejsza liczbę jąder piknotycznych. Ponadto zmniejsza poziom stresu oksydacyjnego. Badania te sugerują, że stymulacja magnetyczna dawała silniejszy efekt antyoksydacyjny i neuroprotekcyjny niż leczenie farmakologiczne. Wymagane są dalsze badania, zwłaszcza kliniczne, z udziałem większej liczby pacjentów – w celu uzyskania dowodów lepszej jakości i dla ustalenia konkretnych protokołów leczenia. Obecnie przezczaszkowa stymulacja magnetyczna stosowana jest jako terapia pomocnicza, a najszersze zastosowanie znajduje w badaniach eksperymentalnych27.
W stwardnieniu rozsianym stosowana jest również laseroterapia niskiej i średniej mocy, która wywołuje zmiany na poziomie komórkowym (powstawanie składników bioaktywnych, które prowadzą do zmian w metabolizmie komórkowym) oraz wykazuje działanie przeciwbólowe, przeciwzapalne i przeciwobrzękowe. Laseroterapia działa regenerująco m.in. poprzez stymulację wzrostu komórek Schwanna, które sprzyjają przewodzeniu nerwowemu. Ta właściwość tej metody jest bardzo pomocna w stwardnieniu rozsianym. Ponadto w brazylijskim badaniu klinicznym z 2020 roku zauważono, że laseroterapia niskoenergetyczna stymuluje wytwarzanie interleukiny 10, która z kolei hamuje produkcję cytokin, ma więc działanie przeciwzapalne, korzystne u pacjentów z SM28.
IHHT – terapia przyszłości?
Innowacyjną formą terapii wspomagającej leczenie jest IHHT (ang. intermittent hypoxic-hyperoxic training), czyli trening komórkowy polegający na podawaniu pacjentom naprzemiennie niskich i wysokich stężeń tlenu we wdychanym powietrzu.
Metoda ta opiera się na odkryciu, że krótkie okresy łagodnego niedotlenienia prowadzą w organizmie do zmian funkcjonalnych i metabolicznych, które nasilają adaptację do hipoksji i niosą ze sobą cały szereg właściwości protekcyjnych. Mechanizm ten nie został jeszcze zgłębiony, wiadomo jednak, że jednym z głównych czynników wywołujących odpowiedź adaptacyjną na niedotlenienie jest wytwarzanie reaktywnych form tlenu, które sprzyjają aktywacji licznych reakcji ochronnych, takich jak obrona antyoksydacyjna, potencjał przeciwzapalny czy inicjacja sygnalizacji redoks. Dochodzi jednocześnie do optymalizacji energetycznej procesów metabolicznych i do zwiększenia transportu tlenu do komórek29.
IHHT stosowana jest obecnie z powodzeniem przy różnych problemach zdrowotnych, w tym w zespole przewlekłego zmęczenia czy w zespole przetrenowania u sportowców. Z punktu widzenia pacjentów z SM obiecujące wydają się również wyniki badania klinicznego z udziałem grupy pacjentów geriatrycznych (w wieku od 64 do 92 lat). W badaniu tym ustalono, że trening hipoksją-hiperoksją połączony z programem ćwiczeń multimodalnych dał znacząco lepsze wyniki niż sam program ćwiczeń multimodalnych. Poprawę zaobserwowano w obszarze funkcji poznawczych oraz zdolności do ćwiczeń fizycznych, mierzonej 6-minutowym testem marszowym30.
Badania nad zastosowaniem IHHT u chorych ze stwardnieniem rozsianym dopiero zostały rozpoczęte. Pilotażowe badanie kliniczne przeprowadzane jest właśnie – pod kierownictwem Manuela Friese oraz Christopha Heesena – przez Institut für Neuroimmunologie und Multiple Sklerose w Hamburgu. Pierwsze wyniki spodziewane są jeszcze w tym roku.
Leczenie uzdrowiskowe SM
Cennym elementem rehabilitacji pacjenta ze stwardnieniem rozsianym – zwłaszcza takiego, który zachował podstawową samodzielność funkcjonalną – jest terapia w uzdrowisku, gdzie oprócz wymienionych już form fizjoterapii oferowane są metody niedostępne gdzie indziej, takie jak kąpiele solankowe, perełkowe, kwasowęglowe i siarczkowe oraz masaż wodny.
Chorzy mogą też korzystać z różnych form hydroterapii. Wiadomo, że pływanie rozluźnia mięśnie i zmniejsza spastyczność. Rozluźnienie takie sprzyja zwiększeniu zakresu ruchu stawów. Ponadto właściwości wody pozwalają na wykonywanie ćwiczeń oporowych, które zwiększają siłę i wytrzymałość mięśni otaczających kręgosłup. Zaleca się, by hydroterapię przeprowadzać dwa razy w tygodniu przez 20 minut, w temperaturze ok. 26°C. Ze względu na męczliwość pacjentów należy bacznie monitorować ich samopoczucie31.
Suplementy diety przy SM
Pacjenci ze stwardnieniem rozsianym powinni przyjmować witaminę D, ponieważ często obserwuje się u nich jej niedobory. Spekuluje się, czy mogą one stanowić czynnik ryzyka choroby. Ponadto u pacjentów z niższym stężeniem witaminy D dochodzi do cięższego przebiegu stwardnienia rozsianego. Według przeglądu badań z 2020 roku suplementacja tej witaminy może wspomagać długoterminowe leczenie immunoterapeutyczne oraz korzystnie wpływać na skuteczność glikokortykosteroidów podczas zaostrzenia choroby. Witamina D jest niezbędna zarówno dla układu odpornościowego, jak i układu nerwowego, a oba te układy w SM działają niewłaściwie. Ponadto w badaniach klinicznych zaobserwowano zmniejszenie niektórych objawów choroby, widocznych w badaniach obrazowych, pod wpływem suplementacji witaminy D, choć nadal niejasny jest jej wpływ na parametry kliniczne32.
Dla osób ze stwardnieniem rozsianym istotne mogą być również witaminy z grupy B. Obserwuje się, że ich niedobór daje podobne objawy, co choroba (może prowadzić do demielinizacji). Właściwości tych witamin, czyli działanie przeciwzapalne i sprzyjające remielinizacji, są obiecujące, brak jest jednak dostatecznych badań klinicznych dla potwierdzenia ich skuteczności w tym schorzeniu33.
Najsilniejsze dowody przemawiają za stosowaniem jednej z witamin z tej grupy – biotyny, czyli witaminy B7. Na przykład w badaniu klinicznym z 2016 roku stwierdzono, że stosowanie przez rok 100 mg biotyny trzy razy dziennie doprowadziło do cofnięcia się stopnia niepełnosprawności u 12,6% pacjentów z postępującym SM, a także zmniejszyło odsetek pacjentów z postępującą niepełnosprawnością oraz poprawiło parametry kliniczne34.
Podsumowując: opieka nad osobami ze stwardnieniem rozsianym jest kwestią multidyscyplinarną, w której niezwykle ważną rolę odgrywa fizjoterapia. Może ona poprawić jakość życia pacjentów dzięki łagodzeniu konkretnych objawów choroby. Przegląd systematyczny piśmiennictwa Cochrane z 2007 roku ustalił, że nawet jeśli fizjoterapia nie zmniejsza rzeczywistego poziomu niepełnosprawności, to korzystnie wpływa na aktywność osób chorych i na ich ogólną zdolność do bycia czynnymi członkami społeczeństwa35. Nowsze, bo przeprowadzone w 2019 roku, duńskie badanie kliniczne z udziałem ponad 400 pacjentów z SM wykazało, że rehabilitacja multidyscyplinarna prowadzona w lecznictwie zamkniętym daje długo utrzymującą się (12 miesięcy po interwencji) poprawę związanej ze zdrowiem jakości życia36. Fizjoterapia daje osobom ze stwardnieniem rozsianym nadzieję na lepsze życie.
- Walton C. et al., Multiple Sclerosis Journal. 2020, Nov 11; 26(14): 1816-1821
- Guzik A., Kwolek A., Przegląd Medyczny Uniwersytetu Rzeszowskiego i Narodowego Insytutu Leków
- w Warszawie. 2015; 1: 55-62
- MS Symptoms | National Multiple Sclerosis Society (nationalmssociety.org)
- Leray E. et al., Rev Neurol (Paris). 2016 Jan; 172(1): 3-13
- Bansil S. et al., Acta Neurol Scand. 1999; 99: 91-94
- Types of MS | National Multiple Sclerosis Society (nationalmssociety.org)
- Losy J. i in., Polski Przegląd Neurologiczny. 2016; 12(2): 80-95
- Safarpour Y. et al., Curr Treat Options Neurol. 2017 Aug 17; 19(10): 33
- Rehabilitation | National Multiple Sclerosis Society (nationalmssociety.org)
- Kubsik-Gidlewska A.M. et al., Adv Clin Exp Med. 2017; 26(4): 709-715
- Ebrahimi M. et al., J Clin Physiother Res. 2020 Oct 3; 5(4): e24
- Attar Sayah A.E. et al., Quarterly of the Horizon of Medical Sciences. 2016; 22(1): 43-50
- Besios T. et al., Open Journal of Therapy and Rehabilitation. 2019; 7: 120-130
- Mackay A.M. et al., Int J MS Care. 2015 May-Jun; 17(3): 101-108
- Choobforoushzadeh A. et al., Appl Psychophysiol Biofeedback. 2015 Mar; 40(1): 1-8
- Campbell E. et al., Arch Phys Med Rehabil. 2016 Jan; 97(1): 141-51
- Döring A. et al., EPMA J. 2012; 3(1): 2
- Steiborn B., Łuczak-Piechowiak A., Polski Przegląd Nauk o Zdrowiu. 2006; 1: 95-103
- Flensner G., Lindencrona C., J Adv Nursg. 2002; 37: 541-550
- Sawant A. et al., Mult Scler Relat Disord. 2015 May; 4(3): 219-27
- Santos-Filho S.D., International Journal of Pathology Sciences. 2019 Jan; 2(1): 01-06
- Walhs T.L. et al., J Altern Complement Med. 2010 Dec; 16(12): 1343-9
- Straburzyńska-Lupa A., Straburzyński G. Physiotherapy. Wydawnictwo Lekarskie PZWL, Warszawa, 2007
- Woldańska-Okońska M., Czernicki J., Acta Bio-Opt Inform Med. 2002; 8: 5-9
- Afshari D. et al., Clin Neurol Neurosurg. 2016 Oct; 149: 171-4
- Czernicki J. et al., Kwart Ortop. 2006; 1: 13-17
- León Ruiz M. et al., Neurología (English Edition). 2020; https://doi.org/10.1016/j.nrleng.2020.05.004
- Silva T. et al., PLoS One. 2020; 15(4): e0230551
- Tuter D.S. et al., Open Heart. 2018; 5(2): e000981
- Bayer U. Et al., Alzheimers Dement (NY). 2017 Jan; 3(1): 114-122
- Ciechanowska K., Roeske A., Journal of Education, Health and Sport. 2018; 8(8): 408-418
- Miclea A. et al., Front Immunol. 2020 May 6; https://doi.org/10.3389/fimmu.2020.00781
- Nemazannikova N. et al., Medicinal Chemistry. 2018; 14(2): 170-180
- Tourbah A. et al., Multiple Sclerosis Journal. 2016; 22(13): 1719-1731
- Khan F. et al., Cochrane Database Syst Rev. 2007 Apr 18; (2): CD006036
- Boesen F. Ee al., Multiple Sclerosis. 2019 Nov; 26(14): 135245851988424