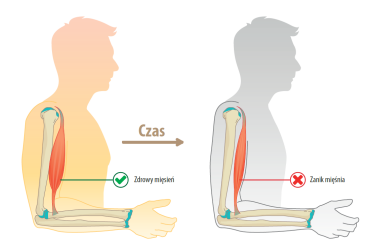
Najpowszechniejszym zaburzeniem wśród dzieci jest dystrofia mięśniowa Duchenne’a, a po niej – wrodzone dystrofie mięśniowe. Wśród dorosłych najczęstsze są dystrofie mięśniowe obręczy kończyn (LGMD – ang. limb girdle muscular dystrophies), dystrofia miotoniczna (DM) oraz mięśniowa dystrofia twarzowo-łopatkowo-ramieniowa (FSHMD – ang. facio-scapulo-humeral muscular dystrophy).
Częstość występowania dystrofii mięśniowych
Szacuje się, że mniej więcej 1 na 3500 osób na świecie cierpi na jakiś rodzaj zaburzenia neuromięśniowego. Współczynniki częstości występowania dystrofii mięśniowych różnią się w zależności od konkretnego typu.
- Dystrofia mięśniowa Duchenne’a (DMD) to najpowszechniejsza forma tego zaburzenia; jest ona zależna od płci, z wzorcem dziedziczenia 1 przypadek na 3500 żywych urodzeń płci męskiej.
- Dystrofia mięśniowa Beckera (która jest łagodną odmianą dystrofii mięśniowej Duchenne’a i dotyczy tego samego genu) jest drugą co do częstości występowania – 1 przypadek na 30 tys. żywych urodzeń płci męskiej.
- Dystrofia miotoniczna jest najpowszechniejszą dystrofią mięśniową pojawiającą się w życiu dorosłym o szacowanym występowaniu 1/8000.
Na podstawie tych liczb można określić, że co roku rodzi się niemal 3600 dzieci z dystrofią mięśniową Duchenne‘a. Przeciętna długość przeżycia pacjentów dotkniętych tą chorobą, wynosząca 20 lat, powoduje, że wśród nas jest wiele osób cierpiących z jej powodu i wymagających pomocy fizjoterapeutów.
Klasyfikacja dystrofii mięśniowych
Dystrofie mięśniowe można podzielić według różnych kryteriów – klinicznych, dziedziczenia genetycznego i defektów molekularnych.
- Kryteria kliniczne
- Każda dystrofia mięśniowa obejmuje konkretne grupy mięśni; pozwala to utworzyć wzór choroby mięśniowej, która może być klinicznie rozpoznana. Na przykład w dystrofii mięśniowej Duchenne’a oraz dystrofiach mięśniowych obręczy kończyn (LGMD) zaatakowane są głównie mięśnie kończyn, podczas gdy w FSHMD – mięśnie twarzy i barku. W dystrofii mięśniowej Duchenne’a mięśnie łydek, mięsień naramienny, mięsień ramienno-promieniowy i mięśnie języka są przerośnięte (ale słabe), podczas gdy część mostkowa mięśnia piersiowego większego oraz mięśnie przywodziciele ud wykazują poważną atrofię.
- Kryteria genetyczne
- Dystrofie mięśniowe charakteryzują się różnymi sposobami dziedziczenia. W dystrofii mięśniowej Duchenne’a oraz dystrofii mięśniowej Beckera (która stanowi łagodniejszą formę DMD i wiąże się z tym samym genem) dziedziczenie jest powiązane z chromosomem X. Choroba występuje głównie u chłopców i mężczyzn, a przekazywana jest w linii żeńskiej. Dzieje się tak, ponieważ gen dystrofiny znajduje się w chromosomie X. Do jej pełnej manifestacji zaburzeń dochodzi jedynie u przedstawicieli płci męskiej, ponieważ u nich występuje tylko jeden chromosom X. Kobiety i dziewczynki mają po dwa chromosomy X, dlatego nawet jeśli w jednym z nich znajduje się zmutowany gen, drugi normalnie funkcjonujący chromosom X zapobiega większym przejawom choroby. W 2/3 przypadków matka ma mutację w genie, tzn. jest nosicielką nieprawidłowego genu. Jednakże w około 1/3 przypadków do mutacji dochodzi spontanicznie. U synów kobiet-nosicielek istnieje 50-proc. prawdopodobieństwo zachorowania. W przypadku córek kobiet-nosicielek istnieje 50-proc. prawdopodobieństwo nosicielstwa i 50-proc. prawdopodobieństwo posiadania normalnego genu.
- Większość wrodzonych dystrofii mięśniowych charakteryzuje się autosomalnym recesywnym modelem dziedziczenia (autosomalny oznacza, że gen nie znajduje się w chromosomie płciowym, ale w jednym z pozostałych 22 chromosomów zwanych autosomami). Tutaj rodzice są nosicielami nieprawidłowego genu i chore dziecko dziedziczy nieprawidłowe geny po obojgu. Dlatego rodzice-nosiciele muszą się liczyć z 25-proc. prawdopodobieństwem, że ich dzieci będą chore, bez względu na płeć. Z drugiej strony dystrofia miotoniczna (DM) dziedziczona jest jako cecha autosomalna dominująca. Każda osoba ma dwie wersje danego genu, jedną po ojcu, drugą po matce. Cechy dominujące to takie, które prowadzą do choroby, nawet jeśli tylko jedna z wersji jest nieprawidłowa. Dlatego pacjenci z DM mają jeden nieprawidłowy gen, a prawdopodobieństwo, że ich dzieci odziedziczą ten nieprawidłowy gen i przez to także zachorują, wynosi 50 proc. W ten sposób chory gen przekazywany jest przyszłym pokoleniom w sposób wertykalny.
- Kryteria molekularne
- Zapewniają one najtrafniejszą diagnozę, ponieważ określa ona gen, który przenosi mutację. Badania genetyczne w tym kierunku należy przeprowadzać na DNA chorego dziecka (przeważnie pobieranego z jego krwi).
Dystrofia mięśniowa - diagnoza
Rozpoznanie dystrofii mięśniowej stawia się na podstawie wywiadu klinicznego, badania i wywiadu rodzinnego. Użytecznym kryterium przy określaniu konkretnego typu jest wiek zachorowania. Bardzo może pomóc informacja, która grupa mięśni jest dotknięta. Użyteczny jest wywiad rodzinny. Pokrewieństwo rodziców sugeruje autosomalną recesywną dystrofię mięśniową, taką jak LGMD, lub wrodzoną dystrofię mięśniową.
Wartości kinazy kreatynowej są często podwyższone, zwłaszcza w DMD i BMD. Do podwyższenia nie dochodzi w FSHMD ani w miotonicznej dystrofii mięśniowej.
Użyteczne są badania EMG, potwierdzają one, że mamy do czynienia z chorobą pierwotnie atakującą mięśnie. Miotonię łatwo jest rozpoznać w przypadku dystrofii miotonicznej. Biopsję mięśni przeprowadza się rzadziej, ponieważ przy powszechnej DMD przechodzi się od razu do badań molekularnych. Wykonuje się ją tylko wówczas, gdy w badaniach DNA nie wykryje się żadnej delecji. Biopsji mięśni zawsze powinno towarzyszyć barwienie przy użyciu konkretnych przeciwciał w celu zidentyfikowania typu dystrofii mięśniowej. Jest to szczególnie użyteczne w dystrofiach mięśniowych obręczy kończyn, gdyż wielu ich typów nie można rozróżnić na podstawie samego badania klinicznego.
Ostateczna odpowiedź pochodzi z badań molekularnych. Są one niezbędne z wielu powodów. Po pierwsze, pewna diagnoza jest konieczna dla doradztwa genetycznego i diagnostyki prenatalnej. Po drugie, nowoczesne terapie bazują na dokładnych zmianach w genach. Na przykład w DMD dobrze jest znać rozmiar delecji w różnych eksonach, ponieważ jako formę terapii opracowano pomijanie eksonów i prawdopodobnie niedługo zacznie ono być stosowane w klinicznej praktyce, przynajmniej pomijanie eksonu 51 i 45. Postępują także prace nad terapiami omijania kodonów nonsensownych, w przypadkach gdy to właśnie one stanowią mutację genu.
Leczenie dystrofii mięśniowej
Międzynarodowe grupy ekspertów oraz European Neuromuscular Centre wydają od czasu do czasu wytyczne odnośnie do postępowania. Istnieją doskonałe wytyczne dla DMD i LGMD.
Niektórzy lekarze niechętnie stosują sterydy, jednak autor tego artykułu rekomenduje, by stosować je w każdym przypadku DMD. Przy sterydach problemem staje się otyłość, ale doradzamy ścisłą kontrolę diety i unikanie nadmiernej podaży tłuszczów. Polecamy również jednoczesne stosowanie inhibitorów pompy protonowej, takich jak omeprazol czy lanzoprazol, lub podobnych leków w celu redukcji podrażnienia żołądka oraz suplementację wapnia i witaminy D w celu wzmocnienia kości.
Problemy z układem krążenia występujące w DMD i dystrofii mięśniowej Emery’ego-Dreifussa leczone są właściwie. Miotonia w dystrofii miotonicznej może być leczona takimi lekami jak karbamazepina czy fenytoina, ale brak jest farmaceutyków poprawiających stan mięśni.
Na całym świecie prowadzone są intensywne badania nad znalezieniem leków na dystrofie mięśniowe. Sukcesem było wprowadzenie pominięcia eksonu w DMD, dzięki czemu udaje się złagodzić chorobę. Podstawą tej technologii jest to, że w DMD powszechnie dochodzi do delecji eksonów, które przerywają transkrypcję DNA z genu w RNA i następnie w syntezę dystrofiny. Przez pominięcie przyległego eksonu przy użyciu specjalnie utworzonych oligonukleotydów przywraca się ramkę odczytu. Prowadzi to do poprawionej syntezy dystrofiny. Pomijanie eksonu 51 zostało już zatwierdzone do klinicznego stosowania.
Podobnie gdy mutacja jest kodonem nonsensownym, istnieją leki, dzięki którym można obejść ten "nonsens" i doprowadzić do syntezy białka. Zastosowanie jednego leku działającego na tej zasadzie (PTC) nie pozwoliło na osiągnięcie celów badania. Jednak naukowcy nie ustają w poszukiwaniach innych takich leków. Terapia genowa jest celem ostatecznym, ale w badaniach na zwierzętach miała ona ograniczoną skuteczność, no i nie ma jest jeszcze badań na ludziach.
Niektóre ośrodki na świecie przeprowadzają terapię komórkami macierzystymi, w której wstrzykuje się komórki macierzyste (czy komórki mezenchymalne) w mięsień w kilku miejscach. Autor artykułu nie spotkał jeszcze ani jednego dziecka, które doświadczyłoby poprawy. Dlatego nie poleca tych rodzajów terapii. Powinny one być dozwolone jedynie w ramach protokołów badawczych, dopóki nie udowodni się ich skuteczności.
Fizjoterapia a dystrofie mięśniowe
Fizjoterapia zapobiega przykurczom (stanom, w których skrócone mięśnie dokoła stawów powodują nieprawidłowe i czasem bolesne ich ustawienie). Może stać się niezbędne zastosowanie ortez (urządzeń ortopedycznych używanych do stabilizacji) lub korekcyjnej chirurgii ortopedycznej w celu poprawienia ruchów mięśni, a dzięki temu także jakości życia.
Zasady fizjoterapii przy dystrofii mięśniowej:
- Wykonywanie wzmacniających mięśnie ćwiczeń z obciążeniami. Silniejsze mięśnie mogą pomóc opóźnić nadejście osłabienia związanego z dystrofią.
- Ćwiczenia ruchowe i rozciągające. Gibkość może pomóc w łagodzeniu przykurczów stawów, sztywnienia mięśni wokół stawu, które dotyka większości osób cierpiących na dystrofie mięśniowe.
- Szyny lub ortezy na kończynach dolnych lub górnych. Szyny lub klamry pomagają w utrzymywaniu elastyczności ścięgien i mięśni oraz uniknięciu bolesnych przykurczów. Elementy te zastosowane w odpowiednim czasie mogą stać się potężnym sprzymierzeńcem dzieci, które mają problemy z utrzymywaniem równowagi czy samodzielnym chodzeniem. Nauka chodzenia z szyną wymaga praktyki, a tę najlepiej zdobyć podczas sesji z fizjoterapeutą.
- Hydroterapia. Wielu ekspertów zgadza się, że ćwiczenia w wodzie pomagają w napinaniu oraz wzmacnianiu mięśni i stawów bez obciążania tych części ciała, które już są osłabione lub słabną.
- Unikanie wad posturalnych, dbanie o właściwą postawę i podparcie dla kręgosłupa. Osoby cierpiące na dystrofię mięśniową mają także skłonność do skrzywień kręgosłupa, które z kolei mogą poważnie zaburzyć ich zdolność chodzenia, wstawania i samodzielnego wykonywania innych prostych czynności. Dzięki rozciąganiu i nauce przyjmowania właściwej postawy ciała znacząco zmniejszamy ryzyko problemów z kręgosłupem.
- Nauka oddychania. Nieodpowiednia postawa i przykurcze ciała mogą prowadzić do dodatkowego obciążenia płuc, przez co u osób z dystrofią mięśniową może dochodzić do problemów z oddychaniem. Staje się to szczególnie ważne podczas procesu starzenia się oraz gdy poruszanie się staje się trudniejsze. Warto pamiętać o głębokich oddechach (dziesięć razy rano i dziesięć razy wieczorem). Na późniejszych etapach choroby mogą być konieczne bardziej intensywne ćwiczenia oddechowe.
Dystrofie mięśniowe - rokowanie
Przy dystrofii mięśniowej perspektywy wyglądają różnie w zależności od jej typu i progresji zaburzenia. Niektóre przypadki mogą być łagodne i postępować bardzo wolno przy normalnej długości życia, podczas gdy w innych progresja słabości mięśni, funkcjonalnej niepełnosprawności i utraty chodzenia bywa znaczna. Spodziewana długość życia zależy od stopnia progresji oraz od stopnia zajęcia mięśni serca i układu oddechowego.
Diagnostyka prenatalna a dystrofie mięśniowe
Ponieważ zaburzenia są zdeterminowane genetycznie, istnieje ryzyko pojawienia się ich u kolejnych dzieci w danej rodzinie. Zależy to od typu dziedziczenia. Aby przeprowadzić diagnostykę prenatalną w kolejnych ciążach, niezbędne jest zidentyfikowanie defektu na poziomie molekularnym. Powinno się to robić, jeśli to możliwe, przed ciążą, czasem precyzyjne określenie defektu wymaga więcej czasu. Diagnostykę prenatalną najlepiej przeprowadzać w 11. tygodniu ciąży przy pomocy biopsji kosmówki.
Dystrofie mięśniowe - podsumowanie
W pracy z dziećmi z dystrofiami mięśniowymi i ich rodzicami zalecane jest podejście optymistyczne. Niedawny sukces technologii pomijania eksonów dobrze wróży co do przyszłych przełomów w zakresie skutecznego leczenia. Mięśnie powinno się utrzymywać w jak najsilniejszym i najzdrowszym stanie, ponieważ jeśli terapia stanie się dostępna, pomoże ona jedynie funkcjonującym mięśniom, nie będzie mogła ożywić włókien mięśniowych, które uległy degeneracji.