Ból dolnej części pleców - wprowadzenie
Ból dolnej części pleców to powszechny problem w krajach rozwiniętych, a jego występowanie w jakimś momencie życia stwierdza się u 84% populacji1. Ból dolnej części pleców skutkuje znaczącym poziomem niepełnosprawności i ograniczeniami codziennych czynności, między innymi niezdolnością do pracy37. W skali światowej ból dolnej części pleców powoduje najwyższą liczbę lat przeżytych z niepełnosprawnością według indeksu niepełnosprawności51. Około 85% przypadków klasyfikuje się jako ból wieloczynnikowy lub „niespecyficzny ból” dolnej części pleców (LBP – low back pain)49, a większość pacjentów pierwsze kroki kieruje ku placówkom opieki podstawowej14.
W wytycznych praktyki klinicznej zalecenia odnośnie do leczenia LBP oparte są na samozarządzaniu, fizjoterapii i terapii psychologicznej14. Ponadto nie zaleca się rutynowego stosowania badań obrazowych, funkcjonalnych i fizykalnych14. Z drugiej strony stwierdzono wiarygodne znaczące różnice między podgrupami pacjentów z ostrym i przewlekłym LBP oraz zdrowymi osobami, jeśli chodzi o fizyczne aspekty kręgosłupa lędźwiowego widoczne w badaniach obrazowych i fizykalnych (np. zakres ruchu kręgosłupa, funkcja i morfologia mięśni)33,20,38,16,52.
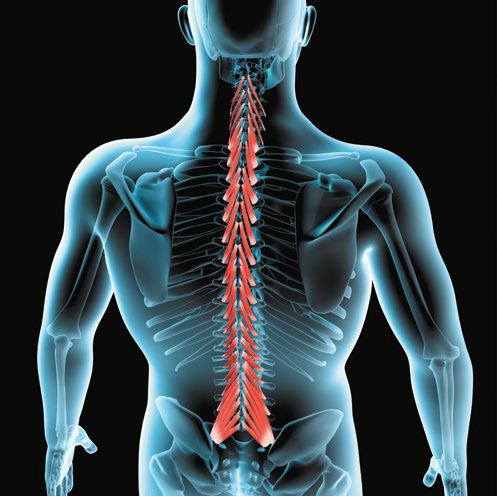
Mięsień wielodzielny lędźwi
Jednym z najczęściej badanych mięśni u pacjentów z LBP jest mięsień wielodzielny lędźwi (LM – lumbar multifidus). LM jest jednym z mięśni przyczyniających się do stabilności kręgosłupa lędźwiowego42,35,7. W pewnej podgrupie pacjentów LBP może być związany z dysfunkcją aktywnej stabilizacji kręgosłupa lędźwiowego, odpowiedzialną za przekształcenia się ostrego LBP w przewlekły, natomiast niejasne jest, jak można by zidentyfikować tę podgrupę47. Badania kliniczne wskazują, że u pacjentów z ostrym LBP stabilizacja jest skuteczniejsza od treningu funkcjonalnego24,6,41, szczególnie dlatego, że terapia stabilizacyjna zapobiega zmniejszeniu powierzchni przekroju LM (czyli atrofii mięśnia) po przedłużonym leżeniu w łóżku6. Tę redukcję średnicy LM obserwuje się również u pacjentów z przewlekłym LBP41,2,11, a jednak niejasnym pozostaje, czy jest to przyczyna, czy skutek przewlekłego LBP. Badania, które stwierdziły związki między dysfunkcją LM a LBP, przeprowadzono głównie w warunkach laboratoryjnych na niewielkich jednorodnych populacjach, co komplikuje możliwość uogólniania ich wyników i przekładania na praktykę kliniczną52,36,4.
W celu wypracowania lepszego podejścia niezbędna jest wiedza, które z tych parametrów mięśnia wielodzielnego lędźwi (funkcja i morfologia) mają znaczenie dla rutynowej opieki oraz czy mają one zastosowanie przy pacjentach z podostrym i/lub przewlekłym LBP. Dlatego też istnieje duża potrzeba badań sprawdzających występowanie zmian w funkcji i/lub morfologii LM w podgrupach pacjentów z ostrym, podostrym i przewlekłym LBP w realnych sytuacjach, o większych próbach badawczych. Dane z takich badań mogą przyczynić się do identyfikacji klinicznie istotnych podgrup, które potrzebują konkretnego leczenia, co zwiększyłoby skuteczność terapii LBP29,25.
Celem niniejszego badania jest porównanie cech klinicznych, związanych z funkcją dolnej części pleców i morfologią LM, między pacjentami z podostrym i przewlekłym LBP z dużej kohorty z praktyki klinicznej i osobami zdrowymi (grupa kontrolna).
Metody badania osób z bólem dolnej części pleców
Zastosowano projekt wieloośrodkowego kliniczno-kontrolnego badania przekrojowego. Uczestników rekrutowano w sieci Spine Network (zrzeszającej około 120 fizjoterapeutów) w niderlandzkim regionie Twente od marca 2017 do maja 2018 r. Do badania włączano pacjentów w wieku od 18 do 65 lat z LBP (niespecyficznym bólem dolnej części pleców). Kryteriami wykluczającymi były: istnienie ewentualnie poważnej patologii wymagającej skierowania do specjalisty, krzyżowo-lędźwiowy zespół korzeniowy, ciąża, wcześniejsza operacja pleców, obecna diagnoza psychiatryczna, niedostateczna znajomość języka holenderskiego lub indeks masy ciała (BMI) powyżej 3044. Pacjentów podzielono na grupy z podostrym LBP (trwającym krócej niż 3 miesiące) i z przewlekłym LBP (trwającym dłużej niż 3 miesiące)50,15. Do badania zrekrutowano także zdrowe osoby (grupa kontrolna) w wieku od 18 do 65 lat, bez LBP w wywiadzie (w ostatnich 6 miesiącach)53,17. Kryteria wykluczające dla tych osób były takie same jak dla pacjentów z LBP.
W badaniu przeprowadzono pomiary funkcji mięśnia LM (sEMG, czyli elektromiografia czynnościowa) i jego morfologii (USG) oraz testy czynnościowe dolnej części pleców przy pomocy kinematyki 3D. Badanie sEMG przeprowadzano, mierząc aktywność LM podczas testu Biering-Sorensena w celu oceny wytrzymałości izometrycznej jako miary czynności mięśnia LM12. Podczas testu uczestnicy leżeli na brzuchu z dolną częścią ciała przymocowaną do ławki. Uczestnik miał utrzymać pozycję poziomą bez wsparcia górnej części ciała przez 60 s. Wcześniej ustalono, że pacjenci z wyższym ryzykiem dolegliwości mogą wytrzymać ten test przez czas krótszy niż 58 s2. Dlatego test w niniejszym badaniu przeprowadzano maksymalnie przez 60 s. Wyliczano średnią częstotliwość dla każdego pacjenta dla ustalenia zmęczenia mięśnia oraz średnią kwadratową w celu ustalenia intensywności skurczów.
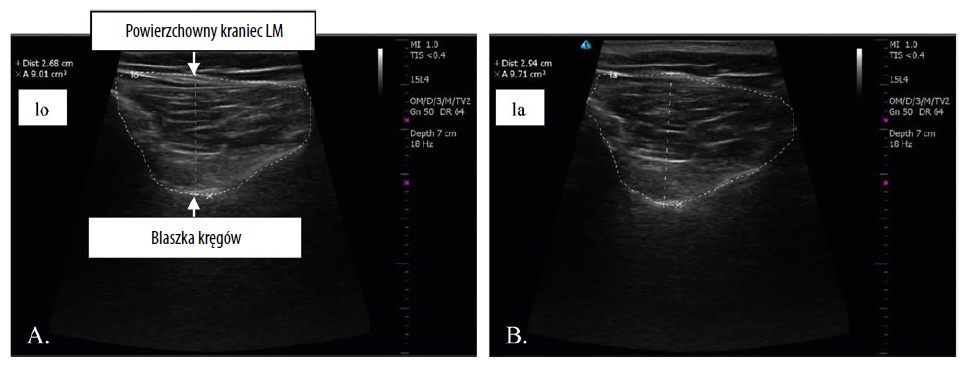
A. Lewy mięsień wielodzielny lędźwi w spoczynku (oznaczony „lo”). B. Lewy mięsień wielodzielny lędźwi w skurczu submaksymalnym (oznaczony „la”).
Grubość w centymetrach podana jest przy oznaczeniu „+Dist.” po lewej stronie.
Morfologię LM zbadano przy użyciu USG. Pozyskano osobne obrazy dla lewego i prawego LM w dwóch warunkach (w spoczynku i w skurczu submaksymalnym – w sumie po cztery obrazy u każdego uczestnika)34. Uczestnicy leżeli na brzuchu z poduszką pod brzuchem w celu zminimalizowania lordozy lędźwiowej. W celu uzyskania submaksymalnego skurczu LM uczestnicy wykonywali test uniesienia przeciwległej kończyny górnej34. Grubość LM (w cm) była mierzona w obszarze między blaszką kręgów a powierzchownym krańcem LM46,31 (ryc. 1A).
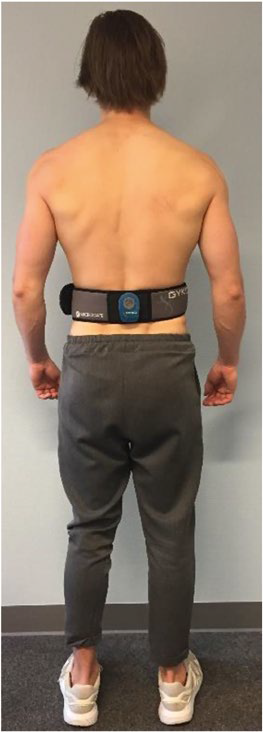
Do pomiaru zakresu ruchu (w stopniach) kręgosłupa lędźwiowego użyto urządzenia Microgate Gyko. Jest to inercyjne narzędzie pomiarowe, które przymocowywano do ciała uczestnika przy pomocy pasa elastycznego. Pas elastyczny umieszczano na nagim tułowiu wokół pleców i brzucha uczestnika, a środek urządzenia Gyko umiejscowiony był na plecach na połączeniu piersiowo-lędźwiowym (Th12-L1) (ryc. 2). Zakres ruchu mierzono podczas następujących testów: zgięcie i wyprost tułowia, boczne zgięcie w lewo i w prawo. Podczas tych testów uczestnika proszono o przyjęcie rozluźnionej wyprostowanej pozycji stojącej, ze stopami na szerokość barków, z kolanami w pozycji standardowej (10 stopni zgięcia) i ramionami opuszczonymi luźno do boków18. Uczestnicy wykonywali maksymalne zgięcie (bez zginania kolan) i wyprost tułowia (z biodrami w pozycji neutralnej). Potem wykonywano maksymalne zgięcie boczne w lewo i w prawo. Urządzenie Gyko posiada dobrą wiarygodność i prawidłowo dokonuje pomiarów zakresu ruchu18.
Wynikami drugorzędnymi badania były dane uczestników, indeks masy ciała, intensywność bólu mierzona przy pomocy skali numerycznej (NRS – numeric rating scale) oraz kwestionariusz Oswestry (Oswestry Disability Index – ODI)26,30. Skala NRS to 11-punktowa skala oceniania bólu, w której 0 oznacza brak bólu, a 10 oznacza najgorszy możliwy ból. Uczestników proszono o ocenienie średniego bólu, jakiego doświadczają danego dnia. ODI to kwestionariusz związany z tą konkretną chorobą przeznaczony dla pacjentów z LBP; daje on wyniki w zakresie od 0 do 100 punktów. Wyniki te dzielone są na pięć kategorii: 0-20% – minimalne ograniczenia; 21-40% – umiarkowane ograniczenia; 41-60% – oczywiste ograniczenia; 61-80% – ograniczenia większości czynności; 81-100% – pacjenci obłożnie chorzy.
Wyniki badań mięśnia wielodzielnego u osób z bólem dolnej części pleców
Uczestnicy badania
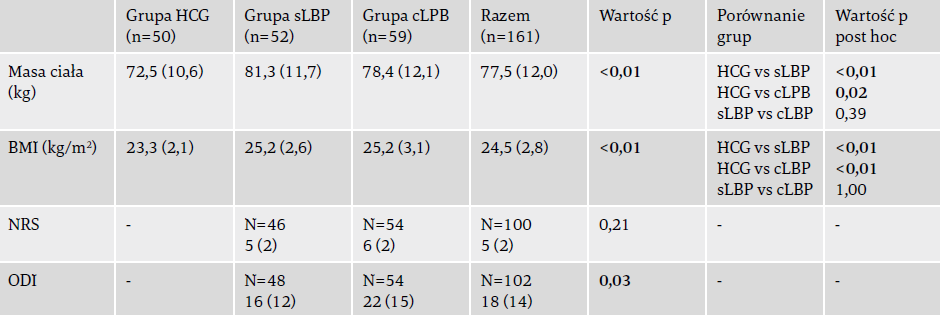
Badaniem objęto 161 uczestników, z czego 50 to osoby zdrowe (grupa kontrolna – healthy controls group HCG), u 59 występował przewlekły LBP (grupa cLBP), a u 52 podostry LBP (grupa sLBP). Ogólnie rzecz biorąc, w grupie kontrolnej występowała znacząco niższa masa ciała niż w obu grupach z LBP (72,5 kg przy 81,3 kg w grupie sLBP i 78,4 kg w grupie cLBP). Między obiema grupami z LBP nie istniały statystycznie znaczące różnice co do intensywności bólu, ale w grupie cLBP występował znacząco wyższy wynik niepełnosprawności niż w grupie sLBP (ODI w sLBP: 16; ODI w cLBP: 22). Statystycznie znaczące różnice między grupami stwierdzono odnośnie do wszystkich parametrów uczestników, oprócz wzrostu. Analiza związku potencjalnych czynników zakłócających i głównych miarwyniku wykazała niewielki wpływ płci, wieku i wzrostu na główne miary wyniku we wszystkich grupach.
z podostrym niespecyficznym bólem dolnej części pleców; cLBP – grupa pacjentów z przewlekłym niespecyficznym bólem dolnej
części pleców; NRS – numeryczna skala pomiaru bólu; ODI – kwestionariusz niepełnosprawności Oswestry. Wartości p znaczące
statystycznie zaznaczono tłustym drukiem.
Zakres ruchu tułowia i grubość LM
Zakres ruchu tułowia i grubość LM były znacząco większe we wszystkich kierunkach i warunkach w grupie kontrolnej niż u pacjentów z LBP, poza zakresem ruchu w bocznym zgięciu w prawo oraz grubością prawego LM w spoczynku. Największe znaczące różnice odnośnie do grubości LM stwierdzono między grupą kontrolną a grupą cLBP. Zaobserwowano, że grubość LM jest mniejsza w obu grupach z LBP niż w grupie kontrolnej oraz mniejsza w grupie cLBP niż w grupie sLBP. Jednak test post hoc ujawnił, że redukcja ta jest znacząca jedynie w porównaniu grupy kontrolnej z obiema grupami LBP. Dane na temat zakresu ruchu (w stopniach) i grubości LM (w cm) przedstawia tabela 2.
znaczące statystycznie zaznaczono tłustym drukiem.
Powierzchniowe EMG
Analizę wyników sEMG podczas testu Biering-Sorensena przeprowadzono dla 130 uczestników, ponieważ 21 z nich nie było w stanie wykonywać testu przez 60 s (ze względu na ból), a dla kolejnych 10 uczestników dane sEMG były niekompletne. Brakowało danych 1 z 50 uczestników z grupy kontrolnej, 13 z 52 uczestników z grupy sLBP oraz 17 z 59 uczestników z grupy cLBP. Nie wystąpiły znaczące różnice między grupami w momencie wyjściowym. Nie stwierdzono także znaczących różnic między grupami w wynikach średniej częstotliwości i średniej kwadratowej. Analiza statystyczna wskazuje, że dane te są bardzo niejednorodne.
Omówienie wyników badań mięśnia wielodzielnego u osób z bólem dolnej części pleców
Niniejsze badanie miało na celu porównanie danych klinicznych odnośnie do funkcji dolnej części pleców i morfologii LM u pacjentów z podostrym LBP, przewlekłym LBP oraz osób zdrowych.
Zakres ruchu u osób z bólem dolnej części pleców
U pacjentów z LBP zaobserwowano znacząco mniejszy zakres ruchu tułowia i mniejszą grubość mięśnia wielodzielnego lędźwi niż u osób zdrowych. Wystąpił także trend mniejszej grubości LM u pacjentów z przewlekłym LBP niż z podostrym LBP, choć nie był on znaczący statystycznie. U pacjentów z przewlekłym LBP wystąpiły większe ograniczenia funkcjonalne (wyższy wynik kwestionariusza ODI) niż u pacjentów z podostrym LBP. Jeśli zaś chodzi o dane sEMG, nie stwierdzono znaczących różnic między trzema grupami.
Ogólnie rzecz biorąc, w badaniu niniejszym w obu grupach LBP zaobserwowano mniejszy zakres ruchu różnych ruchów tułowia niż u osób zdrowych. A konkretnie pacjenci z LBP mieli zakres ruchu mniejszy o 15 stopni niż osoby zdrowe podczas zginania tułowia. Podczas prostowania tułowia i bocznego zgięcia tułowia u pacjentów z LBP zakres ruchu był o 5 stopni mniejszy niż u osób zdrowych. Mazzone i wsp. (2016) stwierdzili podobne wyniki u pacjentów z LBP, u których występowała redukcja ruchu lędźwi w porównaniu z osobami zdrowymi podczas wyprostu tułowia43. W wynikach niniejszego badania nie wystąpiły różnice intensywności bólu i ruchów tułowia między pacjentami z podostrym LBP i przewlekłym LBP.
Grubość mięśnia pacjentów z LBP
Wyniki pomiaru grubości LM wykazują, że osoby zdrowe mają znacząco grubszy mięsień wielodzielny lędźwi (o około 1 cm, czyli mniej więcej 30%) na poziomie L5-S1 niż pacjenci z LBP – z wyjątkiem grubości prawego LM w spoczynku.
Piśmiennictwo potwierdza, że pacjenci z LBP (większość literatury dotyczy pacjentów z przewlekłym LBP) cierpią na atrofię LM lub stwierdza się u nich mniejszą grubość LM w porównaniu z osobami zdrowymi w obu typach warunków (w spoczynku i w skurczu submaksymalnym)32,10,39,13. Wyniki niniejszego badania mógłby tłumaczyć fakt, że przy LBP dochodzi do zaprzestania używania LM w ciągu 12 tygodni, co z kolei prowadzi do zmniejszenia grubości tego mięśnia. W wynikach tych zaobserwowano największy spadek grubości LM w pierwszych 12 tygodniach występowania LBP (różnica między osobami zdrowymi a pacjentami z podostrym LBP). To zjawisko powstawania atrofii LM w początkowym okresie LBP stwierdzają także inne badania22,29. Po 12 tygodniach występowania LBP stwierdzono mniejszą grubość LM u pacjentów z przewlekłym LBP niż u pacjentów z podostrym LBP. Podobnie obserwowano w pracach wcześniejszych, w których stwierdzano, że narażona struktura mięśni dolnej części pleców może zwiększać ryzyko utrzymywania się LBP27. Nie jest jasne, czy stwierdzone w niniejszym badaniu różnice między pacjentami z LBP a osobami zdrowymi mają znaczenie kliniczne, ponieważ atrofia LM może być wynikiem szeregu innych czynników biologicznych i/lub psychospołecznych7,27,28.
W badaniu niniejszym zastosowano wyniki pomiarów elektromiografii czynnościowej (medianę częstotliwości i średnią kwadratową) jako wskaźniki odpowiednio zmęczenia mięśnia i poziomu aktywacji mięśnia45. Nie stwierdzono różnic między grupami, jeśli chodzi o zmęczenie mięśnia i jego aktywność podczas testu Biering-Sorensena. Być może można wytłumaczyć to faktem, że test ten wymaga skurczu statycznego, połączonego wysiłku prostowników dolnej części pleców, a jest mniej związany ze stabilnością kręgosłupa, w której LM odgrywa bardzo ważną rolę42. Aktywność LM mogła być kompensowana aktywacją otaczających mięśni w mniej dotkniętych bólem obszarach9.
Co ciekawe, pomiary sEMG nie wykazały różnic między osobami zdrowymi a pacjentami z LBP, ale stwierdzono statystycznie znaczące różnice między tymi grupami odnośnie do zakresu ruchu tułowia i grubości LM. Pozyskane tutaj dane elektromiograficzne wykazały duże odchylenia standardowe, wskazujące na dużą różnorodność między uczestnikami, co utrudniało wykazanie różnic. Na podstawie niniejszego badania przekrojowego nie można ustalić, czy zmniejszona funkcja i pogorszona morfologia są przyczyną, czy też skutkiem LBP. Zaobserwowano jednak w tych dużych kohortach trendy mniejszej grubości LM u pacjentów z sLBP niż u osób zdrowych oraz mniejszej grubości LM u pacjentów z przewlekłym LBP niż u pacjentów z bólem podostrym.
Co badania wniosą do pracy fizjoterapeuty?
Badanie niniejsze przeprowadzono w warunkach klinicznych, co oznacza, że większość testów przeprowadzali fizjoterapeuci w swoich miejscach pracy. Wszystkie testy były testami klinicznymi, jakich często używa się w praktyce fizjoterapeutycznej. Dlatego też projekt tego badania poprawia możliwość uogólniania jego wyników na inne praktyki kliniczne. W pracy fizjoterapeuty może być użyteczny na przykład pomiar zakresu ruchu tułowia przy pomocy urządzenia Gyko.
Żadne inne badanie nie podawało danych (z analizą statystyczną) porównujących grupy pacjentów z podostrym LBP, przewlekłym LBP i osoby zdrowe odnośnie do morfologii LM i funkcji dolnej części pleców w takim środowisku klinicznym i z taką liczbą uczestników. Wyniki te mogą stanowić pierwszy krok do opracowania nowych zasad predykcji klinicznej opartych na funkcji i morfologii, które byłyby mniej subiektywne niż inne algorytmy ustalania zasad.
Ograniczenia przeprowadzonych badań mięśnia wielodzielnego
Między grupami istniały znaczące różnice wielu zmiennych stanowiących cechy uczestników. Na przykład jeśli chodzi o współczynnik mężczyzn do kobiet, w grupie sLBP było więcej mężczyzn (62%) niż w grupie kontrolnej (38%) i grupie cLBP (41%). Osoby zdrowe miały znacząco niższą masę ciała niż pacjenci z LBP. Wstępna analiza wykazała, że wpływ zmiennych mylących, takich jak płeć, wiek i masa ciała, był ograniczony. A jednak grubość prawego LM w spoczynku u osób zdrowych była w pewien sposób skorelowana z masą ciała.
Osoby zdrowe miały znacząco niższą masę ciała, ale większą grubość LM we wszystkich warunkach niż pacjenci z LBP (z wyjątkiem prawego LM w spoczynku), dlatego można przyjąć, że ewentualna stronniczość prowadziłaby do niedoszacowania prawdziwych różnic między osobami zdrowymi a pacjentami. U osób zdrowych nie występował LBP w wywiadzie w ciągu ostatnich 6 miesięcy, co jest arbitralnym punktem odcięcia. Według niektórych danych naukowych nawet jeśli ból ustąpił 9-12 miesięcy przed rekrutacją do badania, w mięśniu nadal mogą występować zmiany morfologiczne23 . Słabością tego badania może być brak znajomości dokładnego czasu utrzymywania się LBP, a jedynie ustalenie, że jest to około 12 tygodni. Dlatego też trudno jest interpretować wyniki grupy sLBP (0-12 tygodni LBP). W przyszłych badaniach warto byłoby, w miarę możliwości, mierzyć dokładny czas utrzymywania się bólu w tygodniach w takich grupach pacjentów.
W niniejszym protokole test Biering-Sorensena miał maksymalny czas trwania 60 s, ze względów praktycznych w celu zminimalizowania obciążenia uczestników. Być może gdyby test ten był wykonywany w czasie tak długim, jaki jest do zniesienia dla poszczególnych uczestników, stwierdzono by więcej różnic między grupami (i/lub większe różnice) odnośnie do zmęczenia mięśnia i jego aktywności12. Z drugiej strony porównywanie danych sEMG z testów o różnych czasach trwania obarczone byłoby innymi ograniczeniami.
Cechy mięśnia wielodzielnego lędźwi u pacjentów z LBP i osób zdrowych
Zakres ruchu tułowia i grubość mięśnia wielodzielnego lędźwi są różne u pacjentów z LBP i osób zdrowych. Pomiar funkcji LM, wyrażonej jako wartości sEMG, nie wykazał różnic między tymi grupami. Nie stwierdzono znaczących różnic odnośnie do intensywności bólu między pacjentami z podostrym i przewlekłym LBP. U pacjentów z przewlekłym LBP występowała znacząco większa niepełnosprawność niż u pacjentów z podostrym LBP.
Źrodło: Musculoskeletal Science and Practice. 2021; 55: 102429 ©2021 The Authors Adaptacja: Katarzyna Bogiel Na podstawie licencji CC BY (http://creativecommons.org/licenses/by/4.0/)
- 1. Airaksinen, O., Brox, J.I., Cedraschi, C., et al., 2006. Chapter 4. European guidelines for the management of chronic nonspecific low back pain. Eur. Spine J. : official publication of the European Spine Society, the European Spinal Deformity Society, and the European Section of the Cervical Spine Research Society 15 (Suppl. 2), S192–S300.
- Alaranta, H., Luoto, S., Heli¨ovaara, M., Hurri, H., 1995. Static back endurance and the risk of low-back pain. Clin. Biomech. 10 (6), 323–324.
- Anders, C., Scholle, H.C., Wagner, H., Puta, C., Grassme, R., Petrovitch, A., 2005. Trunk muscle co-ordination during gait: relationship between muscle function and acute low back pain. Pathophysiology 12 (4), 243–247.
- Anders, C., Brose, G., Hofmann, G.O., Scholle, H.C., 2007. Gender specific activation patterns of trunk muscles during whole body tilt. Eur. J. Appl. Physiol. 101 (2), 195–205.
- Askamp J, van Putten MJ. Mobile EEG in Epilepsy. (1872-7697 (Electronic)).
- Belavy, D.L., Armbrecht, G., Gast, U., Richardson, C.A., Hides, J.A., Felsenberg, D., 2010. Countermeasures against lumbar spine deconditioning in prolonged bed rest: resistive exercise with and without whole body vibration. J. Appl. Physiol. 109 (6), 1801–1811.
- Beneck, G.J., Kulig, K., 2012. Multifidus atrophy is localized and bilateral in active persons with chronic unilateral low back pain. Arch. Phys. Med. Rehabil. 93 (2), 300–306.
- Bridges, A.J., Holler, K.A., 2007. How many is enough? Determining optimal sample sizes for normative studies in pediatric neuropsychology. Child Neuropsychol. : a journal on normal and abnormal development in childhood and adolescence 13 (6), 528–538.
- Le Cara, E.C., Marcus, R.L., Dempsey, A.R., Hoffman, M.D., Hebert, J.J., 2014. Morphology versus function: the relationship between lumbar multifidus intramuscular adipose tissue and muscle function among patients with low back pain. Arch. Phys. Med. Rehabil. 95 (10), 1846–1852.
- Danneels, L.A., Vanderstraeten, G.G., Cambier, D.C., Witvrouw, E.E., De Cuyper, H.J., 2000. CT imaging of trunk muscles in chronic low back pain patients and healthy control subjects. Eur. Spine J. 9 (4), 266–272.
- Danneels, L.A., Coorevits, P.L., Cools, A.M., et al., 2002. Differences in electromyographic activity in the multifidus muscle and the iliocostalis lumborum between healthy subjects and patients with sub-acute and chronic low back pain. Eur. Spine J. 11 (1), 13–19.
- Demoulin, C., Vanderthommen, M., Duysens, C., Crielaard, J.M., 2006. Spinal muscle evaluation using the Sorensen test: a critical appraisal of the literature. Joint Bone Spine 73 (1), 43–50.
- Djordjevic, O., Djordjevic, A., Konstantinovic, L., 2014. Interrater and intrarater reliability of transverse abdominal and lumbar multifidus muscle thickness in subjects with and without low back pain. J. Orthop. Sports Phys. Ther. 44 (12), 979–988.
- Foster Nadine, E.N., 2018. Prevention and treatment of low back pain: evidence, challenges, and promising directions. Lancet, The. 391 (10137), 2368–2383.
- Frank, J.W., Brooker, A.S., DeMaio, S.E., et al., 1996. Disability resulting from occupational low back pain. Part II: what do we know about secondary prevention? A review of the scientific evidence on prevention after disability begins. Spine 21 (24), 2918–2929.
- Goubert, D., Oosterwijck, J.V., Meeus, M., Danneels, L., 2016. Structural changes of lumbar muscles in non-specific low back pain: a systematic review. Pain Physician 19 (7), E985–E1000.
- Griffin, D.W., Harmon, D.C., Kennedy, N.M., 2012. Do patients with chronic low back pain have an altered level and/or pattern of physical activity compared to healthy individuals? A systematic review of the literature. Physiotherapy 98 (1), 13–23.
- Hamersma, D.T., Hofste, A., Rijken, N.H.M., Roe Of Rohe, M., Oosterveld, F.G.J., Soer, R., 2019. Reliability and Validity of the Microgate Gyko for Measuring Range of Motion of the Low Back. Musculoskeletal science & practice, p. 102091.
- Hebert, J., Koppenhaver, S., Fritz, J., Parent, E., 2008. Clinical prediction for success of interventions for managing low back pain. Clin. Sports Med. 27 (3), 463–479.
- Hebert, J.J., Koppenhaver, S.L., Teyhen, D.S., Walker, B.F., Fritz, J.M., 2015. The evaluation of lumbar multifidus muscle function via palpation: reliability and validity of a new clinical test. Spine J. 15 (6), 1196–1202.
- Hermens, H.J., Freriks, B., Disselhorst-Klug, C., Rau, G., 2000. Development of recommendations for SEMG sensors and sensor placement procedures. J. Electromyogr. Kinesiol. 10 (5), 361–374.
- Hides, J.A., Stokes, M.J., Saide, M., Jull, G.A., Cooper, D.H., 1994. Evidence of lumbar multifidus muscle wasting ipsilateral to symptoms in patients with acute/subacute low back pain. Spine 19 (2), 165–172.
- Hides, J.A., Richardson, C.A., Jull, G.A., 1996. Multifidus muscle recovery is not automatic after resolution of acute, first-episode low back pain. Spine 21 (23), 2763–2769.
- Hides, J., Stanton, W., McMahon, S., Sims, K., Richardson, C., 2008. Effect of stabilization training on multifidus muscle cross-sectional area among young elite cricketers with low back pain. J. Orthop. Sports Phys. Ther. 38 (3), 101–108.
- Hides, J.A., Walsh, J.C., Smith, M.M.F., Mendis, M.D., 2017. Self-managed exercises, fitness and strength training, and multifidus muscle size in elite footballers. J. Athl. Train. 52 (7), 649–655.
- Hjermstad, M.J., Fayers, Pm Fau, Haugen, D.F., Haugen, Df Fau, Caraceni, A., et al., 2011. Studies Comparing Numerical Rating Scales, Verbal Rating Scales, and Visual Analogue Scales for Assessment of Pain Intensity in Adults: a Systematic Literature Review (1873-6513 (Electronic)).
- Hodges, P.W., Danneels, L., 2019. Changes in structure and function of the back muscles in low back pain: different time points, observations, and mechanisms. J. Orthop. Sports Phys. Ther. 49 (6), 464–476.
- Hodges, P.W., Moseley, G.L., 2003. Pain and motor control of the lumbopelvic region: effect and possible mechanisms. J. Electromyogr. Kinesiol. 13 (4), 361–370.
- Hodges, P., Holm, A.K., Hansson, T., Holm, S., 2006. Rapid atrophy of the lumbar multifidus follows experimental disc or nerve root injury. Spine 31 (25), 2926–2933.
- van Hooff, M.L., Spruit, M Fau, Fairbank, J.C.T., Fairbank, Jc Fau, van Limbeek, J., van Limbeek, J Fau, Jacobs, W.C.H., Jacobs, W.C., 2015. The Oswestry Disability Index (Version 2.1a): Validation of a Dutch Language Version (1528-1159 (Electronic)).
- Hosseinifar, M., Akbari, A., Ghiasi, F., 2015. Intra-rater reliability of rehabilitative ultrasound imaging for multifidus muscles thickness and cross section area in healthy subjects. Global J. Health Sci. 7 (6), 354–361.
- Kader, D.F., Wardlaw, D., Smith, F.W., 2000. Correlation between the MRI changes in the lumbar multifidus muscles and leg pain. Clin. Radiol. 55 (2), 145–149.
- Kiesel, K.B., Uhl, T.L., Underwood, F.B., Rodd, D.W., Nitz, A.J., 2007a. Measurement of lumbar multifidus muscle contraction with rehabilitative ultrasound imaging. Man. Ther. 12 (2), 161–166.
- Kiesel, K.B., Uhl, T.L., Underwood, F.B., Rodd, D.W., Nitz, A.J., 2007b. Measurement of lumbar multifidus muscle contraction with rehabilitative ultrasound imaging. Man. Ther. 12 (2), 161–166.
- Kiesel, K.B., Uhl, T., Underwood, F.B., Nitz, A.J., 2008. Rehabilitative ultrasound measurement of select trunk muscle activation during induced pain. Man. Ther. 13 (2), 132–138.
- Kiesel, K.B., Butler, R.J., Duckworth, A., et al., 2012. Experimentally induced pain alters the EMG activity of the lumbar multifidus in asymptomatic subjects. Man. Ther. 17 (3), 236–240.
- Kuijer, W., Brouwer, S., Preuper, H.R.S., Groothoff, J.W., Geertzen, J.H.B., Dijkstra, P.U., 2006. Work status and chronic low back pain: exploring the international classification of functioning, disability and health. Disabil. Rehabil. 28 (6), 379–388.
- Larivière, C., Gagnon, D., Loisel, P., 2002. A biomechanical comparison of lifting techniques between subjects with and without chronic low back pain during freestyle lifting and lowering tasks. Clin. BioMech. 17 (2), 89–98.
- Lee, S.W., Chan, C.K.M., Lam, T.S., et al., 2006. Relationship between low back pain and lumbar multifidus size at different postures. Spine 31 (19), 2258–2262.
- De Luca, C.J., 1997. The use of surface electromyography in biomechanics. J. Appl. Biomech. 13 (2), 135–163.
- MacDonald, D.A., Lorimer Moseley, G., Hodges, P.W., 2006. The lumbar multifidus: does the evidence support clinical beliefs? Man. Ther. 11 (4), 254–263.
- MacDonald, D., Moseley, G.L., Hodges, P.W., 2009. Why do some patients keep hurting their back? Evidence of ongoing back muscle dysfunction during remission from recurrent back pain. Pain 142 (3), 183–188.
- Mazzone, B., Wood, R., Gombatto, S., 2016. Spine kinematics during prone extension in people with and without low back pain and among classification-specific low back pain subgroups. J. Orthop. Sports Phys. Ther. 46 (7), 571–579.
- Nordander, C., Willner, J., Hansson, G.A., et al., 2003. Influence of the subcutaneous fat layer, as measured by ultrasound, skinfold calipers and BMI, on the EMG amplitude. Eur. J. Appl. Physiol. 89 (6), 514–519.
- Plamondon, A., Trimble, K., Larivi`ere, C., Desjardins, P., 2004. Back muscle fatigue during intermittent prone back extension exercise. Scand. J. Med. Sci. Sports 14 (4), 221–230.
- Richardson, C., 1999. Therapeutic Exercise for Spinal Segmental Stabilization in Low Back Pain : Scientific Basis and Clinical Approach. Churchill Livingstone, Edinburgh; New York.
- Rosatelli Alessandro, L.A., 2008. Three-dimensional study of the musculotendinous architecture of lumbar multifidus and its functional implications. Clin. Anat. 21 (6), 539–546.
- Roy, S.H., De Luca, C.J., Casavant, D.A., 1989. Lumbar muscle fatigue and chronic lower back pain. Spine 14 (9), 992–1001.
- Steele, J., Bruce-Low, S., Smith, D., Jessop, D., Osborne, N., 2014. Lumbar kinematic variability during gait in chronic low back pain and associations with pain, disability and isolated lumbar extension strength. Clin. Biomech. 29 (10), 1131–1138.
- Steenstra, I.A., Munhall, C., Irvin, E., et al., 2017. Systematic review of prognostic factors for return to work in workers with sub acute and chronic low back pain. J. Occup. Rehabil. 27 (3), 369–381.
- Vos, T., Flaxman, A.D., Naghavi, M., et al., 2012. Years lived with disability (YLDs) for 1160 sequelae of 289 diseases and injuries 1990-2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 380 (9859), 2163–2196.
- Williams, J.M., Haq, I., Lee, R.Y., 2013. An investigation into the onset, pattern, and effects of pain relief on lumbar extensor electromyography in people with acute and chronic low back pain. J. Manip. Physiol. Ther. 36 (2), 91–100.
- Yodchaisarn, W., Puntumetakul, R., Emasithi, A., Boucaut, R., Chatchawan, U., 2018. Altered postural sway during quiet standing in women with clinical lumbar instability. J. Phys. Ther. Sci. 30 (8), 1099–1102.