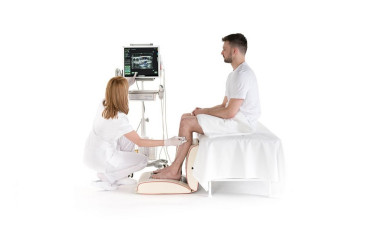
Jakie rodzaje niepełnosprawności mogą występować po udarze mózgu?
Rodzaje i stopnie niepełnosprawności po udarze zależą od tego, który obszar mózgu został uszkodzony.
Zasadniczo udar może powodować pięć rodzajów niepełnosprawności:
- paraliż lub problemy z kontrolowaniem ruchu;
- zaburzenia czucia, w tym ból;
- problemy z używaniem lub rozumieniem języka;
- problemy z myśleniem i pamięcią;
- zaburzenia emocjonalne.
Rola, jaką odgrywają fizjoterapeuci w rehabilitacji poudarowej
Fizjoterapeuci specjalizują się w terapii niepełnosprawności związanej z zaburzeniami motorycznymi i sensorycznymi.
Rehabilitacja pomaga osobom po udarze mózgu nauczyć się ponownie umiejętności utraconych w wyniku uszkodzenia części mózgu.
Na przykład umiejętności te mogą obejmować koordynowanie ruchów kończyn dolnych podczas chodzenia lub wykonywania kroków związanych z dowolną złożoną aktywnością.
Osoby niepełnosprawne zwykle unikają używania upośledzonych kończyn, co nazywane jest wyuczonym nieużywaniem. Jednak powtarzane, celowe aktywności upośledzonych kończyn sprzyjają plastyczności mózgu i pomagają zmniejszyć niepełnosprawność.
Rehabilitacja uczy nowych sposobów wykonywania zadań w celu zminimalizowania deficytów na płaszczyźnie struktury, funkcjonowania i partycypacji.
Eksperci zajmujący się rehabilitacją są zgodni co do tego, że najważniejszym elementem każdego programu rehabilitacji jest starannie ukierunkowana, dobrze zaplanowana, konsekwentna praktyka. Taka sama taktyka jest stosowana przez wszystkie osoby, które uczą się nowych umiejętności, takich jak gra na gitarze lub nowej dyscypliny sportowej lub gry ruchowej.
Dla niektórych pacjentów, którzy przeżyli znaczne załamanie zdrowia i sprawności, rehabilitacja będzie ciągłym procesem podtrzymywania i doskonalenia umiejętności i może obejmować pracę z różnymi specjalistami przez miesiące lub lata po ostrym incydencie choroby. Z czasem rehabilitacja może stać się częścią codzienności, angażującą zespół profesjonalistów i rodzinę.
Fizjoterapeuci wraz z innymi specjalistami odgrywają wiodącą rolę w opracowywaniu odpowiednich strategii i oferty terapeutycznej i treningowej, mającej na celu poradzenie sobie z przejściem pacjenta od bierności do aktywnego stylu życia.
Podczas fazy powrotu do zdrowia pojawia się wiele kwestii i problemów, które fizjoterapeuci muszą rozwiązać, aby przyspieszyć postęp powrotu do zdrowia i sprawności.
Problemy występujące podczas fazy powrotu do zdrowia po udarze:
- paraliż lub niedowład mięśni;
- nieprawidłowa koordynacja;
- apraksja (pacjenci tracą zdolność planowania poszczególnych etapów związanych z wykonaniem złożonego zadania i podjęcia odpowiednich kroków we właściwej kolejności, mają problemy z wykonaniem sekwencji instrukcji);
- obniżone napięcie mięśniowe;
- utrata czucia;
- upośledzenie mowy i języka;
- problemy z pamięcią i wnioskowaniem;
- trudności z połykaniem;
- traumy psychiczne (strach, lęk, frustracja, złość, smutek i poczucie desperacji, depresja kliniczna);
- problemy ze wzrokiem (postrzeganiem) i percepcją wzrokową.
Aby poradzić sobie z tymi problemami, fizjoterapeuci stosują różne podejścia podczas procesu rehabilitacji, które można zasadniczo podzielić na dwie kategorie w oparciu o warunki, w jakich funkcjonują.
Podejścia jakie wykorzystują fizjoterapeuci w walce z problemami u pacjentów po udarze mózgu:
- podejścia stosowane w warunkach klinicznych;
- podejścia stosowane w otoczeniu badawczym.
Podejścia stosowane w warunkach klinicznych - wczesna rehabilitacja
Terapia rehabilitacyjna rozpoczyna się w szpitalu na oddziale intensywnej terapii po ustabilizowaniu stanu zdrowia pacjenta, często w ciągu 24 do 48 godzin po udarze.
Pierwsze kroki obejmują wspomaganie zachowania zdolności do samodzielnego ruchu, ponieważ wielu pacjentów jest sparaliżowanych lub poważnie osłabionych.
W miarę możliwości stymuluje się zmianę pozycji pacjentów, zaangażowanie w bierne lub czynne ćwiczenia ruchowe w celu wzmocnienia kończyn, których funkcja została upośledzona z powodu udaru mózgu. Stopniowo pacjenci przechodzą od siedzenia i transferu pomiędzy łóżkiem a krzesłem, następnie do stania, utrzymywania własnego ciężaru i chodzenia, z pomocą lub bez niej.
Pielęgniarki rehabilitacyjne i terapeuci pomagają pacjentom wykonywać coraz bardziej złożone i wymagające zadania, takie jak kąpiel, ubieranie się i korzystanie z toalety, a także zachęcają pacjentów do korzystania z kończyn bezpośrednio zajętych podczas wykonywania tych zadań.
Rozpoczęcie nabywania umiejętności wykonywania tych podstawowych czynności w codziennym życiu stanowi pierwszy etap powrotu osoby po udarze do niezależności funkcjonalnej.
Tradycyjny program ćwiczeń terapeutycznych obejmuje również wzmacnianie, mobilizację, techniki kompensacyjne, trening wytrzymałościowy (np. trening aerobowy).
Tradycyjne podejścia do poprawy kontroli i koordynacji ruchowej podkreślają potrzebę powtarzania określonych ruchów w celu uczenia się, znaczenie percepcji dla kontroli ruchu oraz potrzebę opanowywania podstawowych ruchów i pozycji (Kirstens i in., 1991).
Podejścia stosowane w warunkach klinicznych - późna rehabilitacja
Metoda Bobath (Terapia neurorozwojowa Bobathów, 1990) u pacjentów po udarze mózgu
Metoda Bobath jest szeroko stosowana w rehabilitacji po udarach i w innych patologiach neurologicznych. Jest to koncepcja rozwiązywania problemów, która pozwala na różnorodność strategii wystarczająco elastycznych, aby dostosować je do mocnych i słabych stron konkretnego pacjenta, nie ograniczając się do zalecanego algorytmu ćwiczeń.
Tradycyjne podejście Bobath opierało się na przekonaniu, że ruchy dobrowolne są oparte na odruchach motorycznych i że terapia musi przebiegać zgodnie z normalną sekwencją rozwojową. Z biegiem lat podejście Bobath było modyfikowane, co wiązało się z pojawieniem się wielu zmian, które nadal są wdrażane.
Obecna koncepcja Bobath zakłada, że kontrola neuronalna nie jest prostą funkcją hierarchiczną, lecz jest bardziej złożona, ponieważ wiele systemów ciała uczestniczy w wykonywaniu ruchu, który jest zorganizowany wokół określonego zadania i ograniczony przez prawa fizyczne i środowisko.
Na podstawie tej zasady NDT jest na nowo definiowane jako podejście do rozwiązywania problemów w badaniu i terapii upośledzeń i ograniczeń funkcjonalnych osób z patologiami układu nerwowego, głównie dzieci z porażeniem mózgowym i dorosłych z udarem lub urazami czaszkowo-mózgowymi.
Ograniczenia metody Bobath
Obecnie nie ma dowodów na to, że interwencja wg koncepcji Bobath jest mniej lub bardziej skuteczna niż inne metody terapii (Konen i wsp., 2009; Luke i wsp., 2004; Paci, 2003).
Dlatego podejście NDT nadal wymaga dostarczenia dowodów w odniesieniu do jego skuteczności w porównaniu z innymi metodami terapeutycznymi.
Na założenia podejścia NDT składało się tradycyjne dziesięć zasad
- Pacjenci z porażeniem mózgowym lub udarem mózgu mają upośledzone wzorce kontroli postawy i koordynacji ruchów.
- Te upośledzenia układu są zmienne, a ogólna funkcja poprawia się, gdy problemy z koordynacją ruchową są rozwiązywane przez bezpośrednie zajęcie się zaburzeniami kontroli neuromotorycznej i postawy w kontekście konkretnego zadania.
- Upośledzenia sensomotoryczne wpływają na całą osobę.
- Wiedza o typowych adaptacyjnych zachowaniach motorycznych, ich rozwoju i zmianach w ciągu całego życia stanowi ramy oceny funkcji i planowania interwencji terapeutycznych.
- Podejście NDT koncentruje się na zmianie strategii ruchowych jako sposobu na osiągnięcie najlepszej wydajności energetycznej u danej osoby w kontekście zadań odpowiednich do jej wieku i uwzględniając antycypację jej przyszłych zadań funkcjonalnych.
- Ruch jest powiązany z przetwarzaniem sensorycznym na dwa różne sposoby: informacje zwrotne (feed back) i planowanie antycypacyjne (feed forward).
- Strategie interwencyjne obejmują aktywne zapoczątkowanie i uczestnictwo, w połączeniu z manualnym prowadzeniem terapeuty.
- Interwencja wykorzystuje analizę ruchu w celu zidentyfikowania deficytowych lub nietypowych elementów, które łączą ograniczenia funkcjonalne z uszkodzeniami układu nerwowego.
- Podczas każdej sesji terapeutycznej odbywa się ciągła ocena pacjenta.
- Celem interwencji NDT jest optymalizacja funkcji.
Dziewięć współczesnych zasad NDT
- NDT akceptuje, że ludzkie zachowanie/funkcje motoryczne wyłaniają się z ciągłych interakcji pomiędzy wieloma systemami wewnętrznymi jednostki.
- Ruch jest zorganizowany wokół celów behawioralnych.
- Wszystkie osoby mają kompetencje i posiadają mocne strony w różnych systemach.
- Cechą charakterystyczną sprawnej funkcji motorycznej człowieka jest zdolność do wybierania i dopasowywania różnych globalnych map neuronalnych z potencjalnie nieskończoną liczbą kombinacji ruchów dostosowanych do różnych czynników.
- NDT wykorzystuje model sprawności / niesprawności oparty na Międzynarodowej Klasyfikacji Funkcji do kategoryzacji stanu zdrowia i niepełnosprawności danej osoby.
- Terapeuci mogą najskuteczniej zaplanować interwencję, ustalając wyniki funkcjonalne we porozumieniu z pacjentem i opiekunami.
- Programy interwencyjne mają przynosić korzyści pacjentom przez cały okres ich życia.
- Nauka lub ponowne opanowywanie umiejętności motorycznych i optymalizacja ich wykonywania wymagają zarówno praktyki, jak i doświadczenia.
- Terapia jest najskuteczniejsza podczas odzyskiwania zdrowia lub fazy przejściowej.
Proprioceptywne torowanie nerwowo-mięśniowe (PNF) (Knott i Voss, 1968) w terapii po udarze mózgu
Podejście PNF wykorzystuje spiralne i diagonalne komponenty ruchu zamiast tradycyjnych ruchów w podstawowych płaszczyznach.
Celem takiego postępowania jest ułatwienia opanowywania i wykonywania wzorców ruchu, które mają bardziej funkcjonalne znaczenie niż tradycyjna technika wzmacniania mięśni poszczególnych grup.
Metoda wykorzystuje opór w celu facylitacji i "irradiacji" stosowanych bodźców na inne części ciała związane z pierwotnym ruchem.
Terapia wymuszonego nieużywania (CIMT) (Taub i wsp. 1968) w później rehabilitacji poudarowej
CIMT jest to podejście behawioralne składające się z różnych komponent, których źródłem jest podstawowa wiedza z zakresu neuronauk.
Terapia pacjentów po incydencie neurologicznym składa się z trzech elementów:
- powtarzalne, zorientowane na zadania treningowe upośledzonej kończyny lub funkcji odbywające się po kilka godzin dziennie przez 10 lub 15 kolejnych dni (w zależności od nasilenia początkowego deficytu);
- ograniczanie możliwości korzystania ze sprawniejszej kończyny;
- zastosowanie zestawu metod behawioralnych opracowanych w celu transferu osiągniętych wyników na inne płaszczyzny.
Ograniczenia CIMT:
- praktyczność zindywidualizowanego treningu;
- potrzeba walidacji osiąganych wyników;
- opłacalność ekonomiczna (rachunek kosztów);
- walidacja w klinikach i ośrodkach badawczych;
- potencjalne źródła błędu pod postacią wielkości efektu (magnitude of effect).
Kwestie otwarte w CIMT:
- trwałość efektu;
- rozkład treningu (intensywność i dawkowanie);
- najlepsze metody treningu (ćwiczenia modelujące czynności czy proste powtarzanie ćwiczeń);
- czynniki kulturowe przyczyniające się do współpracy pacjenta.
Metoda Brunnström (Movement Therapy) (Brunnström, 1970) w rehabilitacji po udarze mózgu
Metoda opiera się na koncepcji, według której uszkodzenie ośrodkowego układu nerwowego powoduje regresję do filogenetycznie starszych wzorców ruchowych.
W związku z tym pierwotne synergizmy, prymitywne odruchy i inne anomalie ruchowe są uważane za normalne procesy powrotu do zdrowia przed osiągnięciem dojrzałych wzorców ruchów.
Dlatego zgodnie z tą zasadą podejście Brunnström wykorzystuje prymitywne wzorce synergiczne w treningu, aby poprawić kontrolę motoryczną poprzez procesy facylitacji ośrodkowej.
Terapia obejmuje torowanie określonych synergii poprzez działanie na skórę oraz wykorzystanie bodźców proprioceptywnych.
Program ponownego uczenia motorycznego (Motor Relearning Program) (Carr i in., 1968) u pacjentów po udarze
Podejście to opiera się na teorii uczenia się motoryki i rozwijało się pod wpływem metody Bobathów. Celem jest, aby pacjent ponownie nauczył się, jak funkcjonalnie się poruszać i jak rozwiązywać problemy podczas próby wykonania nowych zadań.
Ponadto takie podejście uczy ogólnych strategii rozwiązywania problemów motorycznych, zamiast kłaść nacisk na powtarzane wykonywanie określonego ruchu w celu poprawy posiadanej już umiejętności.
Podejście sensomotoryczne (Rood Approach) (Noll Bender i Nelson, 1996) w rehabilitacji poudarowej
Podejście to opiera się na modyfikacji napięcia mięśniowego i dobrowolnej aktywności ruchowej przy wykorzystaniu skórnej stymulacji czuciowej.
W celu torowania napięcia mięśniowego stosuje się następujące techniki stymulacji skóry: szybkie rozciąganie, szybkie pocieranie lodem, szybkie szczotkowanie, opukiwanie ścięgien, wibracje i kompresja stawów w celu przyspieszenia skurczu mięśni proksymalnych.
Podobnie w celu inhibicji napięcia mięśniowego stosuje się powolne przedłużone rozciąganie, długie wychładzanie itp.
Nowsze podejścia w późniejszym etapie rehabilitacji
Trening chodu na bieżni u pacjentów poudarowych
Przywrócenie chodu jest głównym celem rehabilitacji neurologicznej poudarowej. Z tego względu odzyskiwaniu zdolności samodzielnego chodzenia poświęca się dużo miejsca w badaniach naukowych z zakresu fizjoterapii.
Od niedawna trening chodu na bieżni z częściowym odciążeniem zaczął cieszyć się rosnącym zainteresowaniem.
Wyposażenie umożliwiające przeprowadzanie takiego treningu zawiera w sobie układ podwieszający pozwalający regulować względną masę pacjenta, a tym samym ułatwia mu utrzymywanie równowagi i chodzenie w sposób kontrolowany. Automatyzm chodu stymulowany jest przez bieżnię.
Coraz więcej dowodów wskazuje, że trening na bieżni prowadzony u osób starszych z niedowładem połowiczym poprawia zdolności ruchowe podczas chodzenia po normalnym podłożu i ponownego uczenia się zdolności ruchowych, ponieważ zapewnia zorientowaną na zadanie praktykę chodzenia i aktywny, powtarzalny trening ruchowy.
Sugeruje się, że poprzez trening aktywowane zostają ruchy funkcjonalne wzorców motorycznych, wstępujące szlaki sensoryczne, a zatem centralne obwody neuronalne.
Osoby z niedowładem połowiczym często wykazują nieprawidłowe wzorce chodu, takie jak końsko-szpotawe ustawianie stopy (w nadmiernym zgięciu podeszwowym i inwersji) lub opadanie stopy (nadmierne zgięcie podeszwowe). Bardzo często podczas chodzenia paluch i zewnętrzny brzeg stopy ocierają się o ziemię, zwiększając w ten sposób ryzyko zwichnięcia i innych urazów stawów skokowych.
Trening chodu na bieżni z dodatkową stymulacją elektryczną
Aby zminimalizować te wzorce, Liberson i współpracownicy w 1961 r. po raz pierwszy zastosowali stymulację elektryczną w celu skorygowania opadania stopy w hemiplegii.
Funkcjonalna stymulacja elektryczna (FES), oparta na koncepcjach opisanych przez Libersona, wykorzystuje sygnały elektryczne do aktywacji nerwów obwodowych i kontroli ruchów funkcjonalnych.
Omawiana technika wykorzystuje aferentne informacje zwrotne podczas skurczu. Proces ten może zmaksymalizować ponowne uczenie się funkcji motorycznych przez pacjenta podczas aktywnego, opartego na powtórzeniach treningu ruchowego.
W praktyce klinicznej czas funkcjonalnej stymulacji elektrycznej (w minutach) można regulować zgodnie z informacjami zwrotnymi od pacjentów w zakresie od 20 do 45 minut.
Pacjentów należy poinstruować, aby zgłaszali terapeucie, kiedy odczuwają zmęczenie związane ze zgięciem grzbietowym ewersją stymulowanej kończyny dolnej. Gdy pojawia się zmęczenie, należy przerwać FES na 5 minut, a następnie powrócić do kolejnej aktywacji. W miarę poprawy kontroli wolicjonalnej można zmniejszyć amplitudę FES.
Opisano dwie główne zalety wykorzystania FES w połączeniu z treningiem na bieżni. Po pierwsze pacjenci często zgłaszali preferencje chodzenia po bieżni z odciążeniem, gdy trening uwzględniał funkcjonalną stymulację elektryczną. Pacjenci zgłaszają większy komfort takiego treningu, ponieważ jest im łatwiej właściwie ustawić stopę na podłożu.
Drugą zaletą FES jest zmniejszenie fizycznego udziału terapeuty w treningu. Dzięki temu może on zapewnić pomoc manualną w optymalizacji jakości, zamiast skupiać się na prostszych czynnościach, które może wykonać odpowiednie urządzenie.
Trening zorientowany na zadania w rehabilitacji po udarze mózgu
W literaturze przedmiotu nie ma jednoznacznej definicji podejścia zadaniowego. W podejściu zorientowanym na zadania ruch wyłania się jako interakcja między wieloma systemami mózgu i jest zorganizowany wokół celu, a granice jego wykonania stanowią m.in. ograniczenia środowiskowe (Shumway Cook i Woollacott, 2001).
Trening zorientowany na zadania obejmuje szeroki zakres interwencji, takich jak trening na bieżni, chodzenie, trening na standardowym podłożu, programy jazdy na rowerze, trening wytrzymałościowy i trening obwodowo-stacyjny, ćwiczenia w pozycji siedzącej i wykonywanie zadań w celu poprawy równowagi.
Trening zorientowany na zadania musi być powtarzalny i mieć istotne znaczenie dla jednostki.
Wiele interwencji w treningu zorientowanym na zadania, które okazały się skuteczne, można zastosować także w codziennej praktyce pielęgnacyjnej. Dotyczy to takich czynności, jak chodzenie, zmiana pozycji z siedzącej na stojącą z wykorzystaniem różnych krzeseł czy też ćwiczenia sięgania z pozycji siedzącej.
Dzięki wszechstronności i wplataniu zadań w czynności życia codziennego taki trening koncentruje się na zadaniach i na pacjencie, a nie na stałej obecności terapeuty i uzależnienia się od niego.
Aktywne stosowanie treningu zorientowanego na zadania w codziennej opiece pielęgniarskiej nad osobami po udarze mózgu prowadzi do poprawy wyników funkcjonalnych oraz ogólnej jakości życia w odniesieniu do kryteriów zdrowia.
Terapia wspomagana robotami (Krebs i in., 1998) u pacjentów po udarze mózgu
Terapia wspomagana robotami ułatwiająca rehabilitację po udarze zaczęła być wdrażana dopiero w latach 90.
Większość robotów opracowanych do rehabilitacji ma kilka trybów pracy, między innymi dostarcza pasywnego podparcia kończyny górnej o niskim współczynniku tarcia, przejmuje w dużej mierze wykonanie aktywnego ruchu w określonym zakresie i/lub zapewnia zapoczątkowanie wzorca ruchu, gdy pacjent nie może wykonać tego zadania samodzielnie. Pomaga też ukończyć ruch oraz oferuje odpowiedni poziom oporu przy wykonywaniu ruchu.
Dotychczas przebadano pięć rodzajów robotów:
- Assisted Rehabilitation and Measurement (ARM) – stworzony do poprawy funkcji sięgania w linii prostej (Reinkensmeyer i in., 2000).
- Mirror Image Movement Enabler (MIME) – umożliwia unilateralne lub bilateralne ruchy ramion/łokci (Lure i in., 2002; Kahn i in., 2006).
- Bi-Manu-Track – toruje bilateralny bierny i czynny ruch przedramienia (Prange i in., 2006).
- NeReBot – umożliwia ruch barku, łokcia i nadgarstka (Masiero i in., 2007).
- MIT-Manus/nMotion2 – pozwala pacjentowi na wykonywanie ruchu bez interferencji ze strony robota (chociaż robot może pomóc wykonać ruch, gdy dana osoba nie jest w stanie go zainicjować lub zakończyć) (Volpe i in., 1999; 2000).
Terapia wspomagana robotami może potencjalnie ułatwić poprawę kontroli motorycznej po udarze, jednak ciągle nie jest pewne, czy poprawia wyniki w większym stopniu niż konwencjonalna terapia.
Ograniczenia terapii po udarze wspomaganej robotami:
Roboty są bardzo kosztowne (koszt ten może spaść, jeśli staną się standardowym wyposażeniem w klinikach terapeutycznych).
Trzeba się również liczyć z możliwością występowania przestojów w przypadku wszelkich napraw lub modyfikacji komponentów wyposażenia, sprzętu komputerowego oraz oprogramowania, które nie jest rzadkością w przypadku maszyn opartych na zaawansowanej technologii.
Roboty mają trudności z zapewnieniem odpowiedniej terapii osobom ze spastyką. Także ograniczenie fizycznego kontaktu z drugim człowiekiem podczas sesji terapeutycznych może wpływać niekorzystnie na pacjenta.
Trening ruchów bilateralnych (Stewart i in., 2006) po udarze mózgu
Głównym powodem wdrażania bilateralnego treningu ramion jest to, że większość codziennie wykonywalnych czynności wymaga użycia obu ramion.
Na przykład powszednie aktywności, takie jak kąpiel, ubieranie się, spożywanie posiłków, korzystanie z toalety, a także wiele innych funkcji związanych z poruszaniem się, wstawaniem z łóżka lub krzesła oraz prowadzenie samochodu wymaga użycia obydwu kończyn górnych.
Obsługa różnorodnych urządzeń, zakupy i gotowanie również w dużym stopniu wymagają pracy obydwu ramion. Dlatego trening bilateralny może skutecznie poprawiać funkcję ramienia po udarze.
Zasada działania treningu bilateralnego
- W bilateralnym skoordynowanym ruchu kończyny górne łączą się ze sobą i działają prawie jak jedna całość, co odzwierciedla się w sprzężeniu między półkulami mózgowymi w tzw. dodatkowym obszarze motorycznym (supplementary motor area: SMA), w bocznej korze przedruchowej, obszarach przedruchowych i czuciowo-ruchowych, które mogą facylitować ruch w trenowanej kończynie.
- Podczas wykonywania ruchów bilateralnych dochodzi do zmniejszenia inhibicji wewnątrzkorowej, co może ułatwiać reorganizację uszkodzonej półkuli mózgu.
Ograniczenia treningu bilateralnego
Badania naukowe treningu bilateralnego wykazały, że pacjenci odbudowują zdolności motoryczne za jego pomocą, natomiast istnieją sprzeczne informacje, na ile ten rodzaj treningu jest bardziej skuteczny niż ćwiczenia unilateralne.
Także tworzenie protokołów rehabilitacyjnych zapewniających korzyści funkcjonalne oparte na trenowanych ruchach bilateralnych nie jest prostym zadaniem.
Mentalna terapia wyobrażeniowa (Page i in., 2000, 2007) w rehabilitacji poudarowej
Terapia ta wykorzystuje wizualne i kinestetyczne obrazy tworzone w umyśle z perspektywy pierwszoosobowej, w których pacjent ćwiczy w umyśle wykonywanie zadań bez aktywowania mięśni zaangażowanych w fizyczne wykonywanie danej czynności.
Niemniej jednak taki rodzaj treningu aktywuje wiele tych obszarów nerwowych, co rzeczywiste fizyczne wykonywanie określonych aktywności.
W badaniach naukowych z udziałem pacjentów po udarze połączono trening mentalny z ćwiczeniami codziennych zadań lub niefunkcjonalnych aktywności motorycznych i wykonywano to 3–5 razy w tygodniu. Wyniki wykazały pozytywny efekt dodania mentalnego treningu wyobrażeniowego do standardowej terapii.
Zatem trening mentalny wykonywany po udarze wydaje się obiecującym dodatkiem do rehabilitacji ruchowej. Mimo że niezbadana jest zdolność osób po udarze do tworzenia szczegółowych obrazów mentalnych wysokiej jakości, trening mentalny zdaje się pozytywnie wpływać na ogólny wynik terapeutyczny.
Terapia w rzeczywistości wirtualnej (Burdea i in., 1994) u pacjentów po udarze mózgu
Technologia rzeczywistości wirtualnej umożliwia stworzenie środowiska, w którym intensywność informacji zwrotnych i treningu może być systematycznie zmieniana i ulepszana w celu stworzenia najbardziej odpowiedniego, zindywidualizowanego otoczenia do uczenia się funkcji motorycznych.
Potencjalnymi korzyściami z treningu w środowisku rzeczywistości wirtualnej jest możliwość wydłużenia czasu, częstotliwości i intensywności terapii, którą można zapewnić pacjentom za pomocą półautomatycznych programów.
Ćwiczenia rehabilitacyjne w rzeczywistości powodują, że pacjent czuje się zanurzony w symulowanym świecie, co jest niezwykle ważne z punktu widzenia motywacji pacjenta.
Opublikowana w 2011 roku metaanaliza wyników wykorzystania rzeczywistości wirtualnej w rehabilitacji pacjentów poudarowych przyniosła pozytywne i bardzo obiecujące wyniki. Spośród 35 badań 12 zaklasyfikowano do metaanalizy.
W wyselekcjonowanych badaniach stosowano różnorodne wyposażenie zapewniające dostęp do rzeczywistości wirtualnej (np. rękawiczkę cybernetyczną – CyberGlove, metodę imersyjną i nieimersyjną, wirtualnego nauczyciela itd.).
Narzędzia wykorzystane do pomiaru skuteczności metody obejmowały m.in. skalę funkcji ramienia Fugla-Meyera, test motoryczny Wolfa – WMFT, test funkcji ręki T.F.R. Jebsena, pomiar niezależności funkcjonalnej (FIM), zmodyfikowaną skalę Ashworth i wiele innych.
W 11 spośród 12 badań stwierdzono istotną korzyść z zastosowania rzeczywistości wirtualnej u pacjentów po udarze mózgu. Co czyni tę metodę wysoce skuteczną i obiecującą.
Nie potwierdziły się obawy, że osoby trenowane w wykonywaniu zadania motorycznego w środowisku wirtualnym będą przejawiały poprawę jedynie w tym środowisku i ograniczoną do jednego zadania, natomiast efekty nauki nie będą skutecznie przenoszone na zadania w świecie rzeczywistym.
Wydaje się, że rzeczywistość wirtualna powinna stanowić istotny element rehabilitacji pacjentów neurologicznych.
Nieinwazyjna stymulacja kory mózgu u pacjentów po udarze mózgu
Wraz z rozwojem nieinwazyjnych technik stymulacji korowej stało się możliwe ocenianie i wpływanie na aktywność korową i zachowanie się ludzi.
Przezczaszkowa stymulacja magnetyczna (TMS) i przezczaszkowa stymulacja prądem stałym (TDCS) może przyczynić się do zrozumienia mechanizmów procesów rehabilitacyjnych i doprowadzić do opracowania nowych strategii terapeutycznych w neurorehabilitacji.
Badania wskazują na różnorodność mechanizmów oddziaływania nieinwazyjnej stymulacji mózgu osób po przebytym udarze na poprawę funkcji ruchowych. Najprawdopodobniej główne z nich mają związek z procesami neuroplastyczności wykorzystującymi zjawisko długotrwałego wzmocnienia synaptycznego (long-term potentation, LTP) oraz długotrwałego tłumienia synaptycznego (long-term depression).
Oddziaływanie na wybrane obszary mózgu może aktywować receptory pobudzające lub hamujące bezpośrednio w trakcie stosowania zabiegu, jak i przyczyniać się do utrzymywania się osiągniętego efektu przez dłuższy czas.
Zaprezentowane możliwości stają się źródłem kilku pytań: Czy wystarczająca jest jednorazowa stymulacja lub czy należy ją ponawiać? Kiedy zastosować stymulację pobudzającą długotrwałe wzmocnienie synaptyczne, a kiedy długotrwałe stłumienie synaptyczne i w związku z tym, czy należy stymulować ośrodki ruchowe półkuli uszkodzonej bezpośrednio przez udar, czy może półkuli po stronie przeciwnej?
Badanie opublikowane przez Hummela w 2005 w czasopiśmie "Brain" wykazało, że już jednorazowa przezczaszkowa stymulacja prądem stałym (TDCS) wpływała na osiągnięcia w Teście Funkcji Ręki Jebsena-Taylora (JTT) bezpośrednio w wyniku stymulacji w porównaniu z pacjentami z próby kontrolnej, u których urządzenie nie było włączone.
Z kolei grupa badawcza pod kierownictwem Emana M. Khedra stwierdziła pozytywny wpływ dziesięciodniowej serii zabiegów za pomocą magnetycznej stymulacji przezczaszkowej jako uzupełnienia klasycznej terapii. Bardzo interesujące są również doniesienia Naoyuki Takeuchi opublikowane w 2005 roku w czasopiśmie "Stroke".
Obecnie wiadomo, że pierwszorzędowa kora motoryczna po stronie przeciwnej względem uszkodzonej hamuje korę motoryczną bezpośrednio objętą udarem.
Naukowcy podjęli próbę stymulacji kontralateralnego pola motorycznego za pomocą impulsów zmniejszających jego aktywność celem sprawdzenia wpływu takiego oddziaływania na uszkodzone pole motoryczne.
Zgodnie z uzyskanymi wynikami przezczaszkowa stymulacja magnetyczna zmniejszała amplitudę ruchowych potencjałów wywołanych w kontralateralnym polu motorycznym i przyczyniała się do przyspieszenia chwytu ręką bezpośrednio zajętą, pomimo że uprzednio możliwości terapii za pomocą tradycyjnej terapii przestały przynosić poprawę.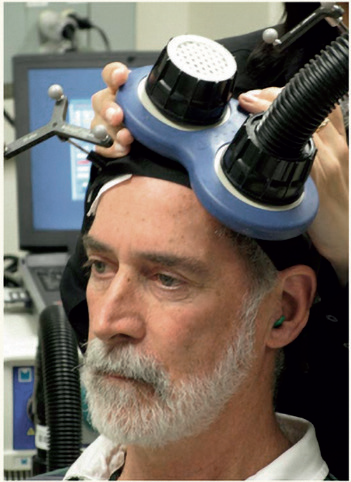
Rola modeli zwierzęcych w neurorehabilitacji
Modele zwierzęce były często pomijane lub traktowane z lekceważeniem. Tymczasem w laboratorium można wysnuć wiele bezcennych wniosków na podstawie analizy zwierzęcych modeli udaru mózgu.
Przykładowo, model ogniska niedokrwiennego u szczurów (endotelina-1 zastosowana do kory czuciowo-ruchowej kończyny przedniej i grzbietowo-bocznego obszaru prążkowia) wykorzystano do oceny wpływu wczesnej rehabilitacji ze wzbogaconym otoczeniem.
Połączenie wysiłków pacjenta (jego odpowiednia motywacja i zaangażowanie) z pracą całego zespołu terapeutycznego i wykorzystanie najnowszych zdobyczy nauki pozwalają na jak największe zmobilizowanie potencjału pacjenta w powrocie do samodzielności.
- Opara J: Fizjoterapia w udarach mózgu. Wydawnictwo Akademii Wychowania Fizycznego w Katowicach, Katowice 2011: 10–44.
- Rożnowska K, Ciborowska H, Członkowska A: Udar mózgu. Wydawnictwo Lekarskie PZWL, Warszawa 2006: 15–50.
- Błaszczyszyn M: Wyniki wczesnej rehabilitacji pacjentów po udarze mózgu – doniesienia wstępne. Zeszyty Metodyczno-Naukowe AWF w Katowicach 2006; 20: 177–189.
- Dimitrijević M.R.: Plastyczność układu nerwowego w procesie przywracania funkcji ruchowych u ludzi. Neurol. Neurochir. Pol. 1996, 30 (supl. 1), 9–16.
- Mauritz K.H., Hesse S., Platz T.: Late recovery of motor functions. Brain Plasticity, Advances in Neurology 1997, 73, 395–408.
- Johansson B.B.: Brain plasticity and stroke rehabilitation. Stroke 2000, 31, 223–230.
- Lennon S., Ashburn A.: The Bobath concept in stroke rehabilitation: a focus group study of the experienced physiotherapists’perspective. Disabil. Rehabil. 2000, 15, 665–674
- Kalra L., Eade J., Wittink M.: Stroke rehabilitation units: Randomized trials and mainstream practice. Cerebrovasc. Dis. 1996, 6, 266-271.
- Kwakkel G., Wagemaar R.C.: Effect of duration of upper-andlower-extremity rehabilitation sessions and walking speed onrecovery of interlimb coordination in hemiplegic gait. PhysTher. 2002, 5, 432–448.
- Laidler P.: Rehabilitacja po udarze mózgu. PZWL, Warszawa 1996. Europejskie Spotkanie w sprawie ustalenia wspólnego stanowiska dotyczącego postępowania w udarze mózgu, Helsingborg, Szwecja, 8–10 listopada 1995. Neurol. Neurochir. Pol. 1997