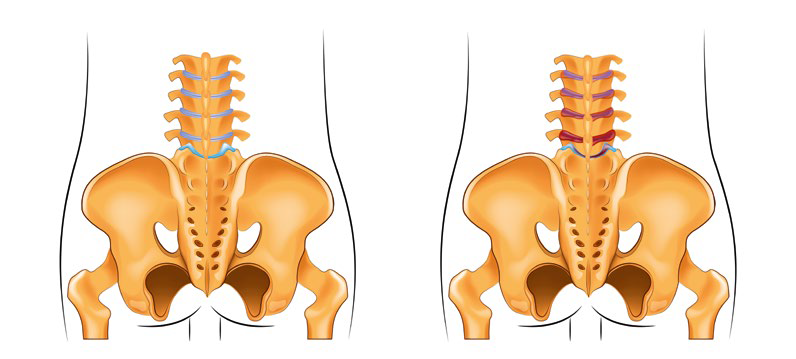
Spondyloartropatia osiowa (axSpA)
jest przewlekłą zapalną chorobą reumatyczną, charakteryzującą się zapalnym bólem pleców, strukturalnymi zmianami kręgosłupa i jego sztywnością. Upośledzona ruchomość i ból kręgosłupa prowadzą do ograniczeń w wykonywaniu codziennych czynności. W przebiegu axSpA stan zapalny występuje chronicznie przede wszystkim w szkielecie osiowym, ale może dotykać także innych obszarów kostnych (i przyjmować postać zapalenia stawu, przyczepu ścięgnistego lub palców) lub pozastawowych (np. w postaci zapalenia błony naczyniowej przedniej komory oka, zmian skórnych czy zapalenia jelita). Cechą charakterystyczną tej grupy chorób jest obecność bólu pleców o podłożu zapalnym z powodu występowania zapalenia przyczepu ścięgnistego, zwłaszcza na poziomie stawu krzyżowo-biodrowego i kręgosłupa, oraz ewentualne zajęcie struktur obwodowych, takich jak przyczep ścięgna Achillesa1.
Międzynarodowe Stowarzyszenie ds. Oceny Spondyloartropatii (ASAS) podało w 2009 r. kryteria diagnostyczne, pozwalające na rozpoznanie tej choroby u pacjentów z bólem pleców utrzymującym się co najmniej 3 miesiące, który pojawił się przed ukończeniem przez nich 45. roku życia. Diagnoza axSpA stawiana jest, gdy na badaniach obrazowych u takich osób widoczne jest zapalenie stawu krzyżowo-biodrowego (tzw. postać radiograficzna choroby) oraz występuje co najmniej jedna z następujących cech choroby:
- ból pleców o podłożu zapalnym,
- zapalenie stawu,
- zapalenie przyczepu ścięgnistego (pięta),
- zapalenie błony naczyniowej,
- zapalenie palców – bolesny obrzęk palców stóp i rąk, zwany także „palcami kiełbaskowatymi”,
- łuszczyca,
- choroba Leśniowskiego-Crohna lub wrzodziejące zapalenie jelita grubego,
- dobra odpowiedź na niesteroidowe leki przeciwzapalne,
- spondyloartropatia w wywiadzie rodzinnym,
- antygen HLA-B27 we krwi,
- podniesione CRP.
Bez widocznych zmian w badaniach obrazowych (postać nieradiograficzna choroby) można postawić to rozpoznanie na podstawie występowania antygenu HLA-B27 we krwi pacjenta plus dwóch innych cech charakterystycznych choroby (spośród wymienionych powyżej)2.
Postać radiograficzna jest po prostu bardziej zaawansowaną postacią spondyloartropatii. Charakteryzuje się ona powstawaniem nowych formacji kostnych i ankylozą (zesztywnieniem) stawu krzyżowo-biodrowego i kręgosłupa, co prowadzi do upośledzenia funkcjonowania, zmian posturalnych, deformacji i niepełnosprawności oraz znacznie obniżonej jakości życia.
Epidemiologia
Według przeglądu z 2018 r. szacuje się, że radiograficzna postać axSpA występuje u 9 do 30 na 10,000 osób. Progresja choroby z postaci nieradiograficznej do ankylozy jest powolna – w ciągu pięciu lat postać zaawansowana wystąpi u 5,1% pacjentów z postacią wczesną, a w ciągu dziesięciu lat u 19%. Postać radiograficzna wiąże się z nieco większym ryzykiem śmierci niż postać nieradiograficzna, natomiast ryzyko zdarzeń sercowo-naczyniowych jest mniej więcej takie samo w obu grupach pacjentów3. U pacjentów z axSpA mogą pojawiać się choroby współistniejące. W tej grupie występuje zwiększone ryzyko choroby sercowo-naczyniowej i osteoporozy, a także nadciśnienia i depresji.
Farmakoterapia
Wczesne podjęcie leczenia wiąże się z lepszą odpowiedzią kliniczną. Leczeniem pierwszego wyboru axSpA pozostają niesteroidowe leki przeciwzapalne – mają one udowodnioną skuteczność odnośnie do działania objawowego, choć nie ma pewności co do ich bezpieczeństwa przy długoterminowym stosowaniu ani wpływu na progresję choroby. W ostatnich dwóch dekadach doszło do dużych postępów w leczeniu spondyloartropatii osiowej dzięki wprowadzeniu leków biologicznych wycelowanych w TNF (czynnik martwicy nowotworów) lub interleukinę IL-17A, które ogólnie wydają się być podobnie skuteczne przy obu postaciach axSpA. Do biologicznych leków przeciwreumatycznych modyfikujących przebieg choroby (bDMARD) należą: etanercept, infliksymab, adalimumab, golimumab, certolizumab pegol oraz sekukinumab4.
Natomiast optymalne leczenie axSpA powinno łączyć podejście farmakologicznie z niefarkmakologicznym, czyli z takimi strategiami jak różne postaci terapii ćwiczeniowych, edukacja, odpowiedni styl życia i zmiana zachowania5.
Fizjoterapia i rehabilitacja
Te formy leczenia stanowią podstawę terapii przy axSpA, ze względu na lepszy profil bezpieczeństwa (mniejsze efekty uboczne) oraz na fakt, że część pacjentów nie reaguje zadowalająco na farmakoterapię.
Artykuł włoskich autorów z 2019 r. prezentuje przegląd obecnie dostępnych dowodów naukowych na temat rehabilitacji pacjentów z axSpA. Czytamy w nim, że ważną częścią postępowania przy tej chorobie okazały się interwencje fizjoterapeutyczne, które są skuteczniejsze, jeśli przeprowadza się je w formie nadzorowanych sesji grupowych w fizjoterapii ambulatoryjnej. Zaś najważniejszym elementem rehabilitacji są regularne ćwiczenia, które mają na celu redukcję obciążających objawów, takich jak ból i sztywność, oraz poprawę funkcjonowania pacjenta. Wykazano, że ćwiczenia u pacjentów z axSpA rzeczywiście zmniejszają aktywność choroby, ból i sztywność, a poprawiają funkcjonowanie fizyczne, rozszerzalność klatki piersiowej, mobilność kręgosłupa i funkcję krążeniowo- oddechową. Mają one również potencjał redukowania objawów depresyjnych. Ponadto badania wykazały, że nadzorowane ćwiczenia grupowe mają tę przewagę nad indywidualnymi programami ćwiczeń bez nadzoru, że te pierwsze przynoszą większą poprawę jakości życia, mobilności kręgosłupa i ogólnej oceny pacjenta.
Ważnym elementem programów rehabilitacji dla osób z axSpA są ćwiczenia wpływające na układ oddechowo- krążeniowy. Jak wykazują badania, intensywne ćwiczenia interwałowe na bieżni (cztery powtórzenia 4 min. biegania/ chodzenia przy tętnie na poziomie 90-95% tętna maksymalnego, na przemian z 3 min. aktywnego odpoczynku na poziomie 70% tętna maksymalnego, dwa razy w tygodniu) przynoszą znaczące zmniejszenie męczliwości, stresu emocjonalnego i poprawę zdolności do podejmowania aktywności. Natomiast w badaniu porównującym dodanie ćwiczeń aerobowych (pływania) do programu rozciągania i ćwiczeń mobilności okazało się, że taki dodatek zwiększa odległość pokonywaną przez pacjentów w 6-minutowym teście marszowym. W innych badaniach donoszono o takich korzyściach włączenia treningu aerobowego do programu rehabilitacji jak zwiększenie sprawności krążeniowo- oddechowej i poprawa wydolności fizycznej.
Ćwiczenia korzystnie wpływają na chorych zarówno przy wczesnej, nieradiograficznej postaci axSpA, jak i w postaci w postaci zaawansowanej (radiograficznej). W jednym z badań zastosowano połączenie takich metod, jak wzmacnianie i trakcja kręgosłupa, ćwiczenia kręgosłupa, korekcja postawy, elementy pilatesu, wzmacnianie mięśni i ćwiczenia w domu.
Okazało się, że ten intensywny program zmniejszył poziom kalprotektyny (markera stanu zapalnego, głównie w układzie pokarmowym) w osoczu zarówno pacjentów z radiologiczną, jak i nieradiologiczną postacią choroby. Ponadto u pacjentów z obu grup zaobserwowano lepszą mobilność i mniejszą aktywność choroby.
Mimo to, wciąż jest mało dowodów na skuteczność rehabilitacji we wczesnym stadium choroby, ze względu na małą ilość badań przeprowadzanych z udziałem tej grupy pacjentów oraz ze względu na czasem kontrowersyjne wyniki badań. Więcej jest danych na temat fizjoterapii w zaawansowanym stadium axSpA.
Według większości badań klinicznych ćwiczenia fizyczne mają korzystny wpływ na kontrolowanie aktywności choroby, ból, mobilność, funkcjonowanie i jakość życia.
Metaanaliza ośmiu badań RCT (randomizowanych badań kontrolowanych) porównujących grupę ćwiczącą z grupą kontrolną wykazała znaczącą poprawę odnośnie do aktywności choroby i funkcji fizycznej. Najsilniejszy efekt zaobserwowano w tych badaniach, w których dominowały raczej ćwiczenia aerobowe i wzmacniające niż klasyczne rozciąganie i ćwiczenia oddechowe. Wartość dodaną stanowiły także hydroterapia i edukacja.
Wykazano, że łączony program ćwiczeń (na zakres ruchu, wzmacniających i aerobowych) wydaje się dawać większe korzyści niż same ćwiczenia na zakres ruchu. Po pojawieniu się opcji leczenia biologicznego porównano efekty samej takiej terapii z leczeniem łączącym farmakoterapię biologiczną z rehabilitacją. Okazało się, że połączenie przynosi lepsze efekty. Należy nadmienić, że w większości badań rehabilitacji nie wdrażano, póki pacjent nie został ustabilizowany przy pomocy leku. Jednym z takich leków jest etanercept. W badaniu z jego zastosowaniem stwierdzono, że połączenie farmakoterapii z rehabilitacją jest skuteczniejsze niż sama farmakoterapia lub sama rehabilitacja – terapia kombinowana dawała większą poprawę funkcji, zmniejszenie niepełnosprawności i podniesienie jakości życia.
Połączenie leku biologicznego z rehabilitacją jest korzystne, ponieważ farmakoterapia zwiększa poziom aktywności pacjenta, łatwiej jest mu wykonywać ćwiczenia i rośnie jego motywacja do udziału w fizjoterapii. W ten sposób osiągany jest efekt synergii10.
Najnowsze zalecenia
W periodyku „Current Opinion in Rheumatology” w roku 2020 opublikowano przegląd wytycznych odnośnie do fizjoterapii w axSpA.
EULAR, czyli Europejska Liga Przeciwreumatyczna, zaleca osobom z axSpA aktywność fizyczną, która jest bezpieczną i integralną częścią opieki standardowej i powinna obejmować cztery obszary:
- ćwiczenia aerobowe (krążeniowo-oddechowe),
- giętkość, ć
- wiczenia oporowe (siłowe)
- oraz ćwiczenia neuromotoryczne.
Natomiast Francuskie Stowarzyszenie Reumatologiczne niedawno zaleciło, by cele leczenia obejmowały poprawianie jakości życia, zachowywanie lub przywracanie możliwości funkcjonalnych oraz uczestniczenie w aktywnościach społecznych. Rekomenduje ono także, by pacjenci ćwiczyli codziennie, według przekazywanych im zindywidualizowanych programów ćwiczeń domowych. Międzynarodowy konsensus opowiada się za tym, by program fizjoterapii obejmował ćwiczenia rozciągające, wzmacniające i korygujące postawę, głębokie oddychanie, prostowanie kręgosłupa, zakres ruchu kręgosłupa, ćwiczenia aerobowe oraz hydroterapię jako terapię pomocniczą.
Korzyści z ćwiczeń aerobowych zostały już omówione. Jeśli chodzi o trening giętkości, typowo polega on na prostowaniu kręgosłupa oraz rozciąganiu kończyn. Również programy ćwiczeń oparte na metodzie Pilatesa wykazywały znaczącą poprawę mobilności pacjentów. Jednak wyjątkowo potrzebny w tej populacji jest trening oporowy, ponieważ obserwuje się w niej znacząco niższą siłę mięśni i siłę funkcjonalną niż w populacji ogólnej. Według badań ćwiczenia siłowe są korzystne w chorobach reumatycznych, ponieważ sprzyjają prawidłowemu składowi masy ciała. Najkorzystniejszy wydaje się tutaj progresywny trening oporowy. Przy zalecaniu tego typu ćwiczeń należy jednak pamiętać, że w przebiegu axSpA bardzo często występuje zapalenie przyczepów ścięgnistych, nie należy więc ich nadmiernie przeciążać11.
Aktywność fizyczna – jak ją kontrolować?
W rekomendacjach ASAS i EULAR dotyczących postępowania z axSpA wszystkim pacjentom z tym schorzeniem zaleca się regularną aktywność fizyczną. Wcześniejsze badania wykazały, że regularna aktywność fizyczna poprawia zdrowie ogólne i status funkcjonalny u pacjentów z axSpA12-18. Widziana z perspektywy pacjenta aktywność fizyczna ma istotne znaczenie, ponieważ sprzyja świadomości ciała i niezależności19,20. Aktywność fizyczna definiowana jest jako wszelkie ruchy ciała przyczyniające się do zużywania energii21. W ujęciu ogólnym, pozytywne skutki zdrowotne regularnej aktywności fizycznej obejmują zmniejszanie ryzyka otyłości, cukrzycy typu 2, nadciśnienia, chorób układu krążenia, depresji, osteoporozy, raka jelita grubego i piersi22. Analogicznie, istnieje znany związek pomiędzy brakiem aktywności fizycznej, takim jak siedzenie lub leżenie, a złą jakością życia23.
Systematyczny przegląd literatury dotyczącej aktywności fizycznej u pacjentów z axSpA wykazał, że regularna aktywność fizyczna łagodzi ból i poprawia funkcjonowanie fizyczne oraz ruchomość kręgosłupa. Jednakże jej wpływ na aktywność choroby jest dyskusyjny, a meta-analiza jest skomplikowana ze względu na heterogeniczność badanych ćwiczeń fizycznych24.
Pacjenci z wyższą aktywnością choroby są według doniesień mniej aktywni fizycznie25,26. Cztery badania przeprowadzone z akcelerometrami sugerują, że poziom ogólnej aktywności fizycznej jest niższy u pacjentów z axSpA niż w zdrowej grupie kontrolnej27. Różnicę tę wyjaśniono obniżoną intensywnością aktywności fizycznej, ponieważ pacjenci z axSpA mają tendencję do mniejszego angażowania się w aktywność fizyczną o intensywności umiarkowanej i energicznej28.
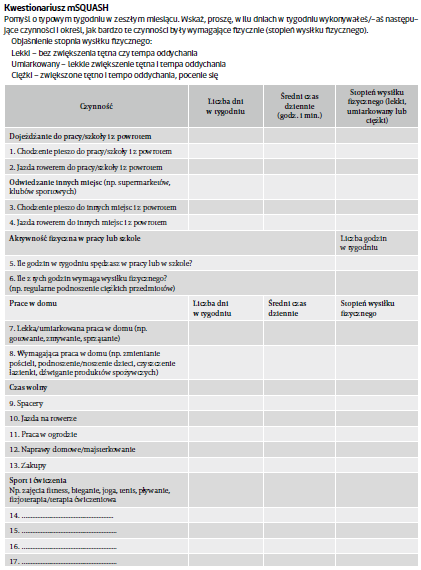
Aktywność fizyczną bada się przy pomocy różnych przyrządów. W celu oceny skuteczności tych przyrządów należy wziąć pod uwagę własności pomiarów, m.in. wykonalność, różnicowanie i prawdziwość29. Złotym standardem pomiaru całkowitego zużycia energii jest metoda podwójnie znakowanej wody (DLW – doubly labelled water). Jednakże metoda DLW jest droga, czasochłonna i odznacza się wysokim obciążeniem osoby badanej, co czyni ją mniej wykonalną. Jako alternatywę można wykorzystać akcelerometry i aplikacje monitorujące aktywność fizyczną. Istotną wadą tych metod jest brak specyfikacji typu aktywności fizycznej. Inną opcją są samodzielnie wypełniane kwestionariusze, które odznaczają się niskim kosztem, niskim obciążeniem pacjenta i łatwością stosowania w praktyce klinicznej. Poza tym można włączyć do nich samoleczenie pacjenta i informacje o konkretnym typie aktywności30. By można było w pełni czerpać korzyści z tych zalet, kwestionariusz powinien obejmować wszystkie dziedziny codziennej aktywności fizycznej (tzn. transport, pracę zawodową, prace domowe, czas wolny i sport), mierząc całkowity czas trwania, częstotliwość i intensywność tych czynności31.
Dobrym narzędziem jest kwestionariusz SQUASH, czyli krótki kwestionariusz do oceny poprawiającej zdrowie aktywności fizycznej. Garbo i wsp. dokonali modyfikacji tego kwestionariusza tak, by był on bardziej adekwatny dla pacjentów z axSpA. We współpracy z pracownikami służby zdrowia i pacjentami utworzyli oni kwestionariusz mSQUASH (ryc. 1). Okazał się on wrażliwy na zmiany, trafny, rzetelny i łatwo wykonalny. Autorzy zalecają jego stosowanie jako dobrego narzędzia dla wspierania samoleczenia pacjenta, zindywidualizowanych programów ćwiczeń i osiągania celów ćwiczeń.
Podsumowując, najważniejszym postępowaniem w leczeniu spondyloartropatii osiowej jest fizjoterapia połączona z farmakoterapią oraz zalecenie utrzymywania przez pacjentów aktywności fizycznej.
Wykorzystano fragmenty artykułu:
M.J.G. Garbo, D. Paap, F. Maas, A. Jetske Baron, L.C. van Overbeeke, M. Siderius, H. Bootsma, F. Wink, S. Arends, A. Spoorenberg, The mSQUASH; a valid, reliable and responsive questionnaire for daily physical activity in patients with axial spondyloarthritis, Seminars in Arthritis and Rheumatism. 2021; 51: 719-727, na podstawie licencji Creative Commons BY 4.0. zaawansowanej (radiograficznej). W jednym z badań zastosowano połączenie takich metod, jak wzmacnianie i trakcja kręgosłupa, ćwiczenia kręgosłupa, korekcja postawy, elementy pilatesu, wzmacnianie mięśni i ćwiczenia w domu.
- Sieper J, Poddubnyy D, Lancet. 2017; 390(10089): 73-84.
- Rudwaleit M. et al., Ann Rheum Dis. 2009 Jun; 68(6): 777-83.
- Wang R., Ward M.M., Curr Opin Rheumatol. 2018 Mar; 30(2): 137-143.
- So A., Inman R.D., Best Pract Res Clin Rheumatol. 2018 Jun; 32(3): 453-471.
- Fragoulis G.F., Siebert S. Rheumatology. 2020 Oct; 59 (Suppl. 4): iv79-iv89.
- Crotti C. et al., The Open Rheumatology Journal. 2018; 12(Suppl-1,M3): 214-225.
- Maresz K., Integr Med (Encinitas). 2015 Feb; 14(1): 34-39.
- Kucharz E.J. i wsp., Varia Medica 2018. tom 2, nr 4, strony 345-348.
- Kwiatkowska B., Maślińska M., Reumatologia. 2020; 58(1): 34-41.
- Perrotta F.M. et al., Rheumatol Ther. 2019 Dec; 6(4): 479-486.
- Martey C., Sengupta R., Curr Opin Rheumatol. 2020 Jul; 32(4): 365-370.
- Raychaudhuri S.P., Deodhar A., J Autoimmun 2014: 48-49: 128-33.
- Regel A. et al., RMD Open 2017; 3(1).
- Khan M.A. Ann Intern Med 2002; 136(12): 896-907.
- Braun J., Sieper J., Lancet 2007; 369(9570): 1379-90.
- Wanders A. et al., Ann Rheum Dis 2005; 64(7): 988-94.
- Boonen A. et al., Semin Arthritis Rheum 2015 Apr; 44(5): 556-62.
- Millner J.R. et al., Semin Arthriti Rheum 2016; 45: 411-27.
- Esbensen B.A., Ann Rheum Dis 2016; 75:21.
- Loeppenthin K. et al., Clin Rehabil 2014; 28(3): 289-99.
- Caspersen C.J. Et al., Public Health Rep 1985; 100(2): 126-31.
- Warburton D.E.R. et al., CMAJ 2006; 174(6): 801-9.
- Rohde G. et al., BMC Musculoskelet Disord 2017.
- Verhoeven F. et al., Int J Rheum Dis 2019.
- Fongen C. et al., Clin Rheumatol 2013 Aug 1; 18(1): 328.
- Brophy S. et al., Semin Arthritis Rheum 2013; 42: 619-26.
- O’Dwyer T. et al., Rheumatol Int 2015; 35:383-404.
- Swinnen T.W. Et al., PLoS One 2014; 9(2).
- Boers M. et al., J Rheumatol 1998; 25(2): 198-9.
- Sylvia L.G. et al., J Acad Nutr Diet 2014; 114(2): 199-208.
- Poppel M.N.M. van et al., S;port Med 2010; 40:565-600.