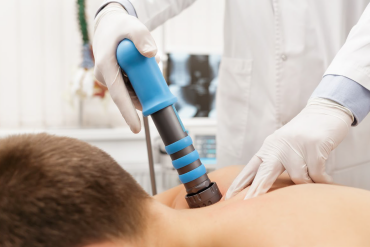
Ultradźwięki w medycynie pojawiły się po raz pierwszy w latach trzydziestych XX wieku, kiedy Theodore i Friederich Dussik podjęli pierwsze próby diagnozowania guzów mózgu z wykorzystaniem ultradźwięków. Badania USG zaczęły być tak naprawdę stosowane w diagnostyce dopiero w latach siedemdziesiątych, kiedy umożliwił to rozwój technologiczny1.
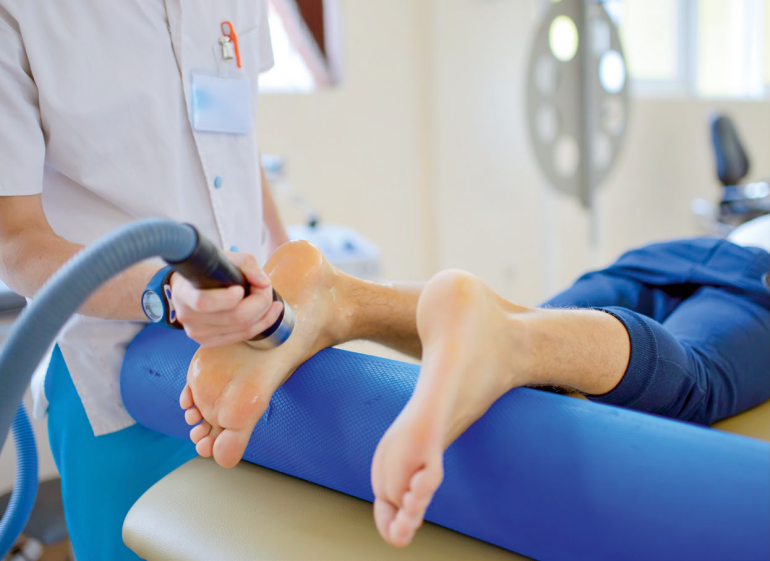
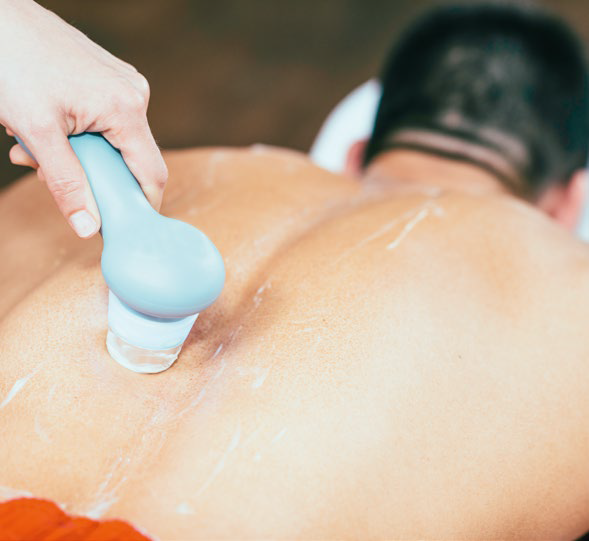
Odrębnym od diagnostycznego zastosowaniem ultradźwięków jest ich użycie w celach typowo leczniczych. Historia tej metody także sięga lat trzydziestych w Niemczech, kiedy to Raimar Pohlman wykazał terapeutyczny wpływ fal ultradźwiękowych na ludzkie tkanki i zaczął wprowadzać do praktyki medycznej fizjoterapię ultradźwiękami (pod nazwą „masaż ultradźwiękami”). Ogólnie w świecie naukowym zainteresowanie chemicznymi i medycznymi efektami działania ultradźwięków znacząco wzrosło w latach osiemdziesiątych, co doprowadziło do powstania terapii ultradźwiękami (TU) w latach dziewięćdziesiątych. Dziedzina ta rozwija się szybko i dynamicznie.
Mechanizm działania terapii ultradźwiękowej
Ultradźwięki to takie dźwięki, których częstotliwość przekracza 20000 Hz – są niesłyszalne dla ludzkiego ucha, ale postrzegane przez niektóre zwierzęta (np. psy i nietoperze). Jak wszystkie dźwięki, również ultradźwięki przenoszą energię. Podczas przechodzenia przez tkanki część z nich przedostaje się do głębszych struktur, część wraca odbita do urządzenia, część się rozprasza, a kolejna część zamienia się w ciepło.
Ma to znaczenie terapeutyczne, ponieważ dzięki ciepłu ultradźwięki podnoszą temperaturę tkanek, nasilają metabolizm, poprawiają miejscowe ukrwienie, zwiększają rozciągliwość włókien kolagenowych oraz zmniejszają lepkość płynów w tkankach. Co ważne, ultradźwięki są w stanie docierać i rozgrzewać tkanki znajdujące się głębiej, niż jest to możliwe przy innych metodach fizykoterapeutycznych.
Pozostałe mechanizmy działania terapii ultradźwiękami (niezwiązane z ciepłem) to m.in.:
- kawitacja, czyli gwałtowna zmiana stanu skupienia substancji z ciekłego na gazowy,
- aktywacja ciała gazowego,
- naprężenia mechaniczne,
- rezonans częstotliwości.
W terapii ultradźwiękami stosuje się dwa różne tryby:
- tryb ciągły, czyli ultradźwięki emitowane są bez przerw, oraz
- tryb pulsacyjny, w którym emisja ultradźwięków jest przerywana.
Innymi ważnymi parametrami TU są częstotliwość, natężenie i czas stosowania. Energia ultradźwięków pochłaniana jest dobrze przez te tkanki, które zawierają duże ilości białek (takie jak więzadła, ścięgna, powięzie, torebki stawowe i tkanki bliznowate), a w o wiele słabszym stopniu przez tkanki zawierające mało białka, a dużo wody (takie jak krew, tkanka tłuszczowa, chrząstka czy kość)2.
Jak piszą Saber i Saber, do głównych zastosowań medycznych TU należą:
- przyspieszanie procesu naprawczego uszkodzonych mięśni poprzez zmniejszenie odpowiedzi zapalnej i liczby komórek zapalnych oraz nasilenie proliferacji i różnicowania mięśniowych linii komórkowych, a także tworzenia tkanki łącznej, co na wczesnych etapach poprawia wytrzymałość mechaniczną,
- łagodzenie przewlekłych zespołów bólowych,
- poprawianie gojenia się ran,
- litotrypsja (kruszenie kamieni) w formie fali uderzeniowej,
- wywoływanie koagulacyjnej nekrozy guzów w tkance głębokiej i niszczenie proliferujących komórek nowotworowych i naczyń krwionośnych ożywiających guz (w onkologii)3.
Natomiast z punktu widzenia fizjoterapii najważniejsze właściwości TU to:
- zwiększanie rozciągliwości kolagenu,
- podwyższanie progu bólu,
- poprawa przepływu krwi,
- zmniejszanie obrzęków,
- redukcja nacieków i wysięków zapalnych,
- łagodzenie skurczów mięśni,
- zmniejszanie sztywności stawów4,5.
Zakres częstotliwości stosowanych w terapii ultradźwiękami dzieli się na wysoki (1-3 MHz) i niski (20-100 kHz). Ultradźwięki o wysokiej częstotliwości i niskiej lub umiarkowanej mocy stosowane są w fizjoterapii, rozbijaniu skrzepów (sonotromboliza), przezskórnym podawaniu leków (sonoforeza), poprawianiu wchłaniania leku przez komórki (sonoporacja) i aktywacji leków (terapia sonodynamiczna). Formą takich ultradźwięków jest także HIFU, czyli high-intensity focused ultrasound (ogniskowane ultradźwięki o dużych natężeniach). Znajdują one zastosowanie w minimalnie inwazyjnej terapii onkologicznej, litotrypsji, ginekologii plastycznej oraz podczas zabiegów kosmetycznych. Ultradźwięki niskiej mocy i wysokiej częstotliwości używane są także w technologii separacji, czyli np. do usuwania cząsteczek lipidów z krwiobiegu.
Ponadto ultradźwięki o częstotliwości 3 MHz stosowane są w leczeniu tkanek powierzchownych, a o częstotliwości 1 MHz – w leczeniu tkanek głębokich, ponieważ głębokość penetracji energii ultradźwięków jest odwrotnie proporcjonalna do ich częstotliwości.
Jeśli chodzi o ultradźwięki niskiej częstotliwości, są one stosowane głównie w stomatologii i chirurgii (do cięcia tkanek) oraz do syntezy mikrokapsułek z substancjami leczniczymi (o większej przyswajalności niż przy innej formie podania)3,6.
Jak widać, zakres zastosowania terapii ultradźwiękowej jest bardzo szeroki. Niniejszy artykuł skupia się jedynie na tych zastosowaniach tej metody, które mają znaczenie w fizjoterapii, takich jak rozgrzewanie tkanek (ścięgien, mięśni i innych) w celu poprawienia przepływu krwi, zmniejszenia bólu i przyspieszenia gojenia, oraz sonoforeza.
Ultradźwięki wspomagają gojenie się tkanek miękkich po urazach
Jednym z głównych zastosowań terapii ultradźwiękami jest wspomaganie gojenia się tkanek miękkich po urazach. Niedawne badanie wykazało, że terapia pulsacyjnymi ultradźwiękami o niskim natężeniu stymuluje fibroblasty (m.in. zwiększa ich żywotność oraz wpływa na wytwarzanie interleukiny 6, kolagenu, czynnika wzrostu śródbłonka naczyniowego oraz jednego z czynników wzrostu fibroblastów), co wskazuje, że taka terapia działa korzystnie w początkowych fazach gojenia się tkanek7.
Korzystny wpływ terapii ultradźwiękami na ścięgna wykazano już w 1989 r. w badaniu biomechanicznym, w którym ścięgna królików po zastosowaniu ultradźwięków regenerowały się lepiej i wykazywały większą wytrzymałość na rozciąganie i zdolność do absorbowania energii niż ścięgna nie poddane TU8. Podobne rezultaty uzyskano dwadzieścia lat później w badaniu na szczurach – ścięgna po TU były zdolne do przenoszenia znacząco większych obciążeń i były bardziej wytrzymałe na rozciąganie niż ścięgna poddane terapii pozorowanej9.
Ultradźwięki mają korzystny wpływ nie tylko na same ścięgna, ale także na ich połączenia z kością. W badaniu na zwierzętach z 2008 r. wykazano, że pulsacyjne ultradźwięki o niskim natężeniu (LIPUS – low intensity pulsed ultrasound) przyspieszają gojenie się połączenia kostno-- ścięgnistego dzięki wpływowi na czynnik wzrostu nabłonka naczyniowego i tworzenie się tkanki chrzęstnej10. Aby osiągnąć jeszcze lepsze wyniki, wskazane może być włączenie do leczenia elektrostymulacji funkcjonalnej. W badaniu na królikach w grupie z zastosowaniem obu tych postaci fizykoterapii osiągnięto większy przyrost tkanki kostnej i lepsze własności ścięgna niż w grupach z samymi ultradźwiękami (LIPUS) lub z samą elektrostymulacją funkcjonalną. Należy nadmienić, że w grupie łączonej na wczesnym etapie zastosowano ultradźwięki, a elektrostymulację wdrożono na późniejszym etapie11.
TU znajduje zastosowanie także przy urazach więzadeł. W amerykańskim badaniu na zwierzętach z 2005 r. zaobserwowano, że terapia ultradźwiękami o niskim natężeniu dzięki zwiększeniu proporcji kolagenu typu I poprawiła gojenie się uszkodzonych więzadeł pobocznych przyśrodkowych. Autorzy dochodzą do wniosku, że TU po urazie więzadła może przyspieszyć powrót do aktywności i zmniejszyć ryzyko ponownego urazu12. W 2016 r. przeprowadzono przegląd systematyczny piśmiennictwa na temat terapii ultradźwiękami o niskim natężeniu (LITUS – low intensity therapeutic ultrasound) dla poprawy gojenia się tkanek miękkich. Czytamy w nim, że TU w problemach mięśniowo-szkieletowych jest stosowana i badana już od siedmiu dekad.
Z badań na zwierzętach i na ludziach z ostatnich dwóch dekad wynika, że LITUS:
- ułatwia gojenie się ścięgien, zwiększając ich wytrzymałość na rozciąganie i poprawiając strukturę kolagenu,
- zwiększa proliferację komórek podczas mioregeneracji i poprawia biomechanikę tkanek (zwiększa zdolność do przenoszenia obciążeń, korzystnie wpływa na sztywność i absorpcję energii), jeśli chodzi o urazy mięśni szkieletowych i ścięgien,
- poprawia gojenie się połączeń kostno-ścięgnistych poprzez korzystny wpływ na funkcję tkanek. Ogólnie dowody naukowe przemawiają za stosowaniem LITUS podczas leczenia urazów tkanek miękkich – metoda ta poprawia wyniki po urazach mięśniowo-szkieletowych i podczas rekonwalescencji pooperacyjnej13.
Leczenie tendinopatii ultradźwiękami
TU korzystnie wpływa również na ścięgna, które nie uległy urazom, ale występują w nich zmiany o charakterze zapalnym lub zwyrodnieniowym. Na przykład w badaniu nad skutkami TU w wapniejącym zapaleniu ścięgien stożka rotatorów z udziałem 61 pacjentów po sześciu tygodniach terapii pulsacyjnymi ultradźwiękami (3-5 razy w tygodniu) zaobserwowano znaczące zmniejszenie bólu oraz poprawę funkcjonowania i jakości życia w porównaniu z placebo14.
Inne zastosowania ultradźwięków
Terapia ultradźwiękami jest skuteczną metodą leczenia problemów zdrowotnych, które zwykle nie kojarzą się z wizytami u fizjoterapeuty, takich jak np. zapalenie zatok. W Indiach przeprowadzono randomizowane badanie kliniczne porównujące TU z diatermią krótkofalową w leczeniu przewlekłej postaci tej choroby. W obu grupach wszystkim pacjentom zapewniono po pięć sesji fizjoterapii polegającej na – oprócz ultradźwięków lub diatermii – uwolnieniu podpotylicznym oraz technikach manualnego drenażu zatok. Drenaż zatoki czołowej fizjoterapeuta przeprowadzał, układając kciuk na zatoce, stosując nacisk bezpośredni i następnie opróżniając zatokę poprzez przesunięcie kciuka do tyłu, ale nie poza ucho. Drenaż zatoki szczękowej fizjoterapeuta przeprowadzał, układając kciuk na zatoce, stosując nacisk bezpośredni i następnie opróżniając zatokę poprzez przesunięcie kciuka do tyłu, do punktu tuż poniżej ucha. Obie procedury powtarzano po siedem razy. Po zakończeniu leczenia w obu grupach doszło do znaczącej poprawy odnośnie do intensywności bólu, tkliwości i jakości życia, natomiast zmiana ta była szybsza i większa w grupie z ultradźwiękami niż z diatermią15.
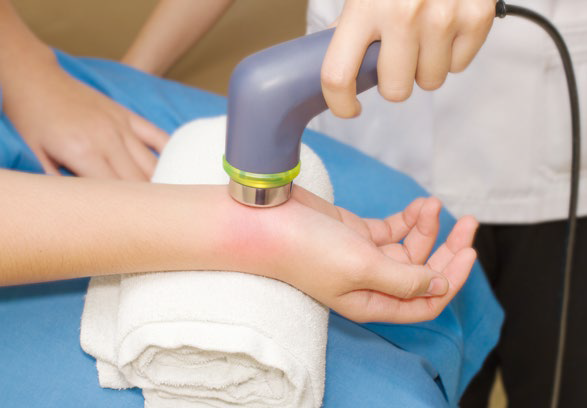
Ultradźwięki na łokieć tenisisty
W randomizowanym badaniu kontrolowanym porównano połączenie TU i ćwiczeń z iniekcjami kortykosteroidów w leczeniu zapalenia bocznego nadkłykcia kości ramiennej u 49 pacjentów. W grupie stosującej TU i ćwiczenia po 12 tygodniach terapii zaobserwowano znaczącą poprawę odnośnie do bólu (VAS, PRTEE), funkcjonowania i siły chwytu bez bólu w porównaniu z grupą z kortykosteroidami16. Podobnie korzystne efekty obserwowano w innych badaniach nad zastosowaniem TU przy tym problemie zdrowotnym, użytej bez innych metod lub w połączeniu z masażem lub innymi technikami fizjoterapeutycznymi17,18. Wydaje się oczywiste, że TU przyczynia się do uśmierzania bólu w przebiegu zapalenia nadkłykcia bocznego kości ramiennej.
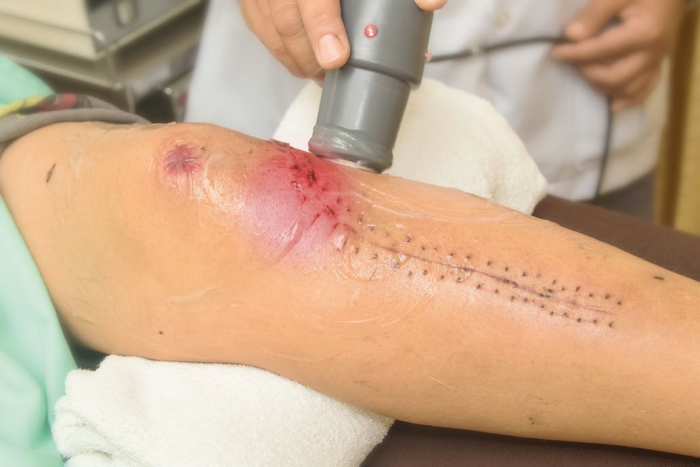
Treapia ultradźwiękami w leczeniu ran przewlekłych i blizn
W roku 2017 opublikowano przegląd dowodów naukowych odnośnie do ultradźwięków w leczeniu ran przewlekłych. Spośród jedenastu badań oryginalnych ujętych w przeglądzie aż dziewięć donosiło o znacząco dobroczynnym wpływie TU na takie rany przewlekłe jak owrzodzenia żylakowe, przewlekłe owrzodzenia podudzi (w tym z powodu krytycznego niedokrwienia kończyny), stopę cukrzycową i odleżyny. Wspomniane w tej pracy przeglądy literatury na temat TU w leczeniu ran przewlekłych obejmowały artykuły z lat 1998-2006.
W większości tych przeglądów stwierdzono korzystny wpływ TU na gojenie się przewlekłych ran. Ponadto w jednym odkryto dowody na dobroczynne działanie ultradźwięków zastosowanych na tkanki wokół rany, a w innym stwierdzono, że gojenie się ran przewlekłych poprawia się po 7-8 tygodniach stosowania ultradźwięków wysokiej częstotliwości.
Według metaanalizy Driver i wsp. z 2011 r. obejmującej osiem badań z udziałem 444 pacjentów, bezkontaktowe ultradźwięki niskiej częstotliwości (NCLFU – non-contact low frequency ultrasound) w przeciągu siedmiu tygodni zmniejszają obszar rany przewlekłej o ok. 85%. Ta metoda fizykoterapii po 6 tygodniach doprowadziła do zagojenia się 32,7% ran, a po 12 tygodniach – do zagojenia się 41,7% ran. Średni czas leczenia przy pomocy NCLFU wyniósł 8,2 tygodnia. Autorzy konkludują, że metoda ta przyspiesza gojenie się ran przewlekłych.
Ogólnie rzecz biorąc, najlepiej przebadane jest stosowanie TU przy owrzodzeniach żylakowych i owrzodzeniach podudzi, natomiast dane odnośnie do odleżyn i stopy cukrzycowej są skąpe i często niskiej jakości, dlatego niemożliwe jest wyciąganie stanowczych wniosków19.
Mięśnie i powięzi - terapia ultradźwiękami
W niedawnym badaniu randomizowanym wykazano, że TU o niskim natężeniu przynosi znaczące zmniejszenie bólu u pacjentów z bólem mięśniowo-powięziowym karku i barku związanym z górną częścią mięśnia czworobocznego grzbietu. Jego autorzy sugerują, że TU można stosować w leczeniu bólu związanego z punktami spustowymi występującymi w górnej części tego mięśnia, co często się zdarza u pacjentów z ostrym bólem karku20. Natomiast w badaniu nad TU o wysokim natężeniu w leczeniu zapalenia powięzi podeszwowej uzyskano znaczące obniżenie poziomu bólu, zmniejszenie rozmiaru cyst wypełnionych płynem oraz poprawę funkcji stopy. Nie zaobserwowano żadnych efektów ubocznych terapii21. W innym badaniu z udziałem 60 pacjentów z przewlekłym zapaleniem powięzi podeszwowej po zastosowaniu TU doszło do znaczącego zmniejszenia bólu, poprawy funkcji i zmniejszenia grubości powięzi podeszwowej (co uwidoczniło obrazowanie przy pomocy rezonansu magnetycznego)22.
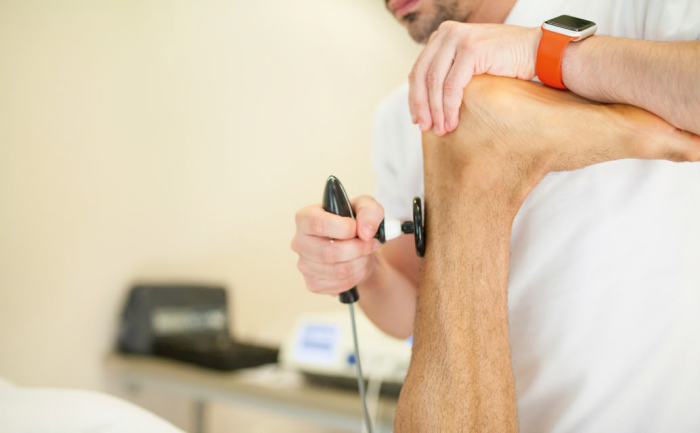
Ultradźwięki pomocne w leczeniu bólu stawów
Ultradźwięki znajdują szerokie zastosowanie w leczeniu bólu stawów, zarówno pochodzenia artretycznego, jak i innego. Przy włączeniu TU do większego planu terapeutycznego obserwowano znaczące zmniejszenie przewlekłego bólu takich stawów jak kolanowy, barkowy czy biodrowy24.
Już w roku 2008 w przeglądzie krytycznym wykazano, że TU skutecznie uśmierza ból, poprawia funkcję i sprzyja naprawie chrząstki u osób z chorobą zwyrodnieniową stawu kolanowego. Autor doszedł do wniosku, że jest to metoda skuteczna i bezpieczna25. Bardziej współczesny przegląd badań eksperymentalnych z 2017 r. donosił, że pulsacyjne ultradźwięki o niskim natężeniu mają korzystny wpływ na komórki chrząstki stawowej u osób z chorobą zwyrodnieniową, zwłaszcza na chondrocyty stawu kolanowego26. W opublikowanym rok później przeglądzie systematycznym i metaanalizie wpływu pulsacyjnych ultradźwięków o niskim natężeniu czytamy, że randomizowane badania kontrolowane wysokiej jakości wykazują, iż LIPUS wpływa korzystnie na ból i odzyskiwanie sprawności funkcjonalnej stawu kolanowego przy chorobie zwyrodnieniowej tego stawu, nie powodując niekorzystnych efektów ubocznych27. W innym przeglądzie systematycznym porównano ultradźwięki pulsacyjne z ciągłymi w leczeniu choroby zwyrodnieniowej kolana. Okazało się, że choć ultradźwięki ciągłe przynoszą ulgę w bólu, to ultradźwięki pulsacyjne dają dodatkowo poprawę funkcji stawu. Jednocześnie stwierdzono, że obie te metody leczenia są bezpieczne28. W porównaniu TU z przezskórną elektrostymulacją (TENS) odnośnie do bólu i funkcjonowania 40 pacjentów z bolesną chorobą zwyrodnieniową stawu kolanowego obie formy fizykoterapii okazały się równie skuteczne29. W przeglądzie Cochrane z 2002 r. stwierdzono, że zastosowanie samej TU skutecznie zmniejsza ból stawu, poranną sztywność i opuchliznę stawu oraz poprawia siłę chwytu i zgięcie grzbietowe nadgarstka u pacjentów z reumatoidalnym zapaleniem stawów30. Nie zaleca się natomiast stosowania TU przy ostrym skręceniu stawu skokowego – brytyjskie wytyczne NICE (National Institute for Health and Care Excellence) stwierdzają, że niewiele jest badań na ten temat, potencjalne efekty leczenia są ogólnie niewielkie i prawdopodobnie mają one ograniczone znaczenie kliniczne, szczególnie gdy weźmiemy po uwagę zwykle krótki okres rekonwalescencji po urazie tego typu.
Ultradźwięki zwiększają zakres ruchu
W japońskim badaniu na zdrowych ochotnikach sprawdzono wpływ terapii ultradźwiękami na zakres ruchu i temperaturę ciała. Interwencję przeprowadzano na górnych włóknach prawego mięśnia czworobocznego, na wysokości segmentu C7. Okazało się, że przez 20 minut po interwencji bierny i czynny zakres ruchu odcinka szyjnego kręgosłupa był większy niż w grupie kontrolnej (bez interwencji). Jednocześnie zaobserwowano zwiększoną temperaturę na powierzchni ciała, która po 20 minutach wróciła do normalnego poziomu. Autorzy wiążą efekt zwiększenia zakresu ruchu ze zmniejszeniem przez ultradźwięki czułości mechanoreceptorów w mięśniach szkieletowych oraz ze zwiększeniem rozciągliwości mięśni dzięki efektowi termicznemu, wpływającemu na lepkosprężystość tkanek23.
Zogniskowane ultradźwięki a ChZ stawu kolanowego
W 2016 r. opublikowano podwójnie zaślepione badanie randomizowane z grupą kontrolną nad zastosowaniem zogniskowanych ultradźwięków pulsacyjnych o niskim natężeniu (FLIPUS – focused low-intensity pulsed ultrasound) u 106 pacjentów z chorobą zwyrodnieniową stawu kolanowego. Grupa terapeutyczna poddawana była terapii FLIPUS i otrzymywała diklofenak, a w grupie kontrolnej również podawano diklofenak, ale przeprowadzano pozorowaną terapię FLIPUS. Po 10 dniach leczenia okazało się, że w grupie terapeutycznej znacząco poprawiły się wyniki odnośnie do bólu, szybkości chodzenia, funkcjonowania, niepełnosprawności i jakości życia bezpośrednio po terapii, oraz odnośnie do bólu i niepełnosprawności podczas wizyt kontrolnych (po 4 i 12 tygodniach po leczeniu). Nie odnotowano żadnych efektów ubocznych związanych z metodą FLIPUS podczas ani po interwencji, autorzy badania piszą więc, że jest to skuteczna i bezpieczna metoda uśmierzająca ból oraz poprawiająca funkcjonowanie i jakość życia u pacjentów z tą chorobą31.
Leczenie złamań kości za pomocą ultradźwięków
Zastosowanie TU w leczeniu złamań jest tematem kontrowersyjnym – po uzyskaniu obiecujących wyników w pierwszym badaniu z 1994 r. stwierdzono jednak, że mogły być one nieadekwatne ze względu na utratę z badania aż jednej trzeciej uczestników. Poza tym korzyści obserwowane w badaniach na liniach komórkowych nie odnajdywały potwierdzenia w późniejszych badaniach na ludziach. A jednak w roku 2017 odkryto, że pulsacyjne ultradźwięki o niskim natężeniu mogą być bardzo pomocne w leczeniu złamań bez zrostu. W badaniu autorstwa Leightona i wsp. sprawdzono tę metodę w leczeniu 1441 złamań bez zrostu, zdefiniowanych jako złamanie bez zrostu widocznego na badaniu rtg co najmniej trzy miesiące po urazie. Stwierdzono, że ultradźwięki mogą stanowić alternatywę dla operacji przy aseptycznych złamaniach bez zrostu, doprowadzając do ich zrostu w ponad 80% przypadków. Metoda ta sprawdzała się lepiej przy hipertroficznych brakach zrostu niż przy biologicznie nieaktywnych atroficznych brakach zrostu. Lepszemu wynikowi leczenia sprzyjało upłynięcie co najmniej sześciu miesięcy od ostatniej operacji przed zastosowaniem TU32.
Sonoforeza - masaż ultradźwiękami
Podczas zabiegów sonoforezy (inaczej fonoforezy) używa się ultradźwięków w celu przezskórnego wprowadzenia leku do organizmu. Głównym – ale nie jedynym – mechanizmem zwiększającym przepuszczalność skóry jest kawitacja33. Na modelach zwierzęcych wykazano, że na bezpieczną i skuteczną sonoforezę pozwala zastosowanie ultradźwięków o częstotliwości od 1 do 3 MHz i natężeniu od 0,1 do 2 W/cm2(34).
W fizjoterapii sonoforeza najczęściej stosowana jest do leczenia stanu zapalnego w tkankach miękkich organizmu, takich jak mięśnie, ścięgna czy więzadła, czyli w leczeniu takich problemów jak zapalenie ścięgna, zapalenie kaletki maziowej, zapalenie torebki stawowej (np. bark zamrożony) czy zapalenie stawu. Do najczęściej stosowanych podczas sonoforezy substancji leczniczych należą steroidy (np. hydrokortyzon, deksametazon), niesteroidowe leki przeciwzapalne (np. diklofenak, ibuprofen, salicylany) i inne leki przeciwbólowe (np. lidokaina).
Skuteczność sonoforezy może obrazować randomizowane badanie kontrolowane z 2019 r. z udziałem 60 pacjentów z co najmniej jednym punktem spustowym w obrębie mięśnia czworobocznego grzbietu. Pacjentów tych podzielono na trzy grupy, w których zastosowano leczenie uciskiem, suche igłowanie lub sonoforezę (betametazon). We wszystkich grupach zaobserwowano poprawę, czyli znaczące zmniejszenie bólu, zwiększenie aktywnego zakresu ruchu kręgosłupa szyjnego i obniżenie progów bólu, natomiast wyniki uzyskane w grupach z sonoforezą i z suchym igłowaniem (taki sam poziom skuteczności) były lepsze od rezultatów w grupie leczonej uciskiem (terapia mięśniowo-powięziowa)35.
Chińscy naukowcy przeprowadzili niedawno przegląd badań nad zastosowaniem ultradźwięków w leczeniu choroby zwyrodnieniowej stawu kolanowego. Wynika z niego, że sonoforeza znacząco obniża ból związany z tą jednostką chorobową. Natomiast dla osiągnięcia lepszego efektu – poprawy funkcjonowania fizycznego i zwiększenia aktywnego zakresu ruchu – należy dodać do leczenia zwykłą terapię ultradźwiękami, która jest skuteczna także w tych obszarach36. Odmienne rezultaty uzyskano w tureckim randomizowanym badaniu kontrolowanym z udziałem 60 pacjentów z ostrym bólem dolnej części pleców. W grupie 1. leczenie polegało na podawaniu przy pomocy sonoforezy diklofenaku i tiokolchikozydu w formie żelu, a w grupie 2. na samych ultradźwiękach z użyciem żelu, który nie zawierał żadnych substancji farmakologicznych. Okazało się, że obie formy leczenia przyniosły obniżenie poziomu bólu, natomiast w grupie z sonoforezą w tygodniu drugim eksperymentu odnotowano większą poprawę sprawności pacjentów, tak że w tygodniu szóstym widoczne były pewne różnice między grupami na korzyść sonoforezy. Autorzy formułują wniosek, że leczenie pacjentów z ostrym bólem dolnej części pleców przy pomocy sonoforezy okazało się skuteczniejsze od konwencjonalnej terapii ultradźwiękami w perspektywie krótkoterminowej37.
Stoi to w zgodzie z ustaleniami dwóch przeglądów badań nad TU w bólu pleców. W jednym z nich stwierdzono, że same ultradźwięki (bez sonoforezy) nie były przy tej dolegliwości skuteczniejsze od placebo, a w drugim – że dawały jedynie efekt krótkoterminowy38,39. Wygląda na to, że przy bólu pleców lepszym wyborem jest sonoforeza.
Jak widać, ultradźwięki terapeutyczne są bardzo przydatne przy całym szeregu problemów zdrowotnych leczonych przy pomocy fizjoterapii. Ta metoda fizykoterapii może pomóc wielu pacjentom o różnorodnych dolegliwościach.
- Newman P.G., Rozycki G.S., Surgical Clinics of North America, 1998 Apr; 78(2): 179-195.
- Ayier R., Noori S.A., Chang K.V. Et al., Pain Med. 2020; 21: 1437-1448.
- Saber A.A., Saber A., J Surg. 2017; 5: 61-69.
- Robertson V.J. et al., Arch Phys Med Rehabil. 2005; 86(4): 819-825.
- Bissell J.H., J Hand Surg Am. 1999; 24(3): 435-448.
- Mason T.J., Ultrasonics Sonochemistry. 2011; 18: 847-852.
- De Oliveira Perrucini P.D. et al., Am J Phys Med Rehabil. 2020; 99: 19-25.
- Enwemeka C.S., Am J Phys Med Rehabil. 1989 Dec; 68(6): 283-7.
- Jeremias S.L. Jr et al. J Orthop Sports Phys Ther. 2011; 41: 526-531.
- Lu H. et al., Ultrasound Med Biol. 2008; 34:1248-1260.
- Hu J., et al., J Orthop Res. 2014 Feb; 32(2): 204-9.
- Sparrow K.J. et al., Am J Sports Med. 2005 Jul; 33(7): 1048-56.
- Best T.M. et al., Inter Med Rev (Wash D C). 2016 Dec; 2(11): 271.
- Page M.J. et al., Cochrane Database Syst Rev. 2016 Jun 10; 106(6): CD012225.
- Kalekar S., Gurudut P., Indian J Physiother Occup Ther. 2019; 1(1): 29-36.
- Murtezani A. et al., Ortop Traumatol Rehabil. 2015; 17(4): 351-357..
- Dingemanse R. et al., Br J Sports Med. 2014; 48: 957-965.
- Smidt N. et al., Ann Med. 2003; 35: 51-62.
- Conner-Kerr T., Oesterle M.E., Chronic Wound Care Manag Res. 2017 May 29; 2017(4): 89-98.
- Petterson S. et al., J Pain Res. 2020; 13: 1277-1287.
- Heigh E. et al., J Foot Ankle Surg. 2019; 58: 519-527.
- Ulusoy A. et al., J Foot Ankle Surg. 2017; 56: 762-767.
- Morishita K. et al., J Phys Ther Sci. 2014 May; 26(5): 711-715.
- Desmeules F. et al., Phys Ther Sport. 2015; 16: 276-284.
- Srbely J.Z., J Can Chiropr Assoc. 2008; 52: 30-37.
- Rothenberg J.B. et al., PMR. 2017; 9: 1268-1277.
- Zhou X.Y. et al., Biomed Res Int. 2018; 2018: 7469197.
- Zeng C. et al., Osteoarthritis Cartilage. 2014 Aug; 22(8): 1090-9.
- Kim E.D. et al., Pain Res Manag. 2019; 2019: 7964897.
- Casimiro L. et al., Cochrane Database Syst Rev. 2002 (3): CD003787.
- Jia L. et al., Scientific Reports. 2016; 6: article number: 35453.
- Nicholson J.A. et al., Bone and Joint Research. 2019 Jul 12; doi: 10.1302/2046-3758.87.BJR-2018-0215.R2
- Park D. et al., PLOS One. 2016, Jun 20; doi: 10.1371/journal.pone.0157707
- Rao R., Nanda S., J Pharm Pharmacol. 2009 Jun; 61(6): 689-705.
- Tabatabaiee A. et al., J Back Musculoskelet Rehabil. 2019; 32(4): 587-594.
- Wu Y. et al., Clin Rehabil. 2019; 33: 1863-1875.
- Altan L. et al., Ultrasonics. 2019 Jan; 91: 201-205.
- Noori S.A. Et al., Pain Med. 2020; 21: 1482-1493.
- Ebadi S. et al., Cochrane Database Syst Rev. 2014; (3): CD009169.