Nieinwazyjna stymulacja mózgu (NSM) obejmuje całą serię metod, których używa się do wywołania przepływu prądu elektrycznego do mózgu oraz w mózgu w celach diagnostycznych lub terapeutycznych. Podczas gdy NSM stosuje się głównie do badania zachowania i fizjologii mózgu, w ostatnich latach naukowcy sprawdzają możliwość korzystania z NSM jako ewentualnej formy terapii przy szerokim wachlarzu rozpoznań klinicznych, a także do leczenia ubytków ruchowych będących wynikiem problemów neurologicznych takich jak udar, porażenie mózgowe czy uszkodzenie rdzenia kręgowego.
Rodzaje nieinwazyjnej stymulacji mózgu
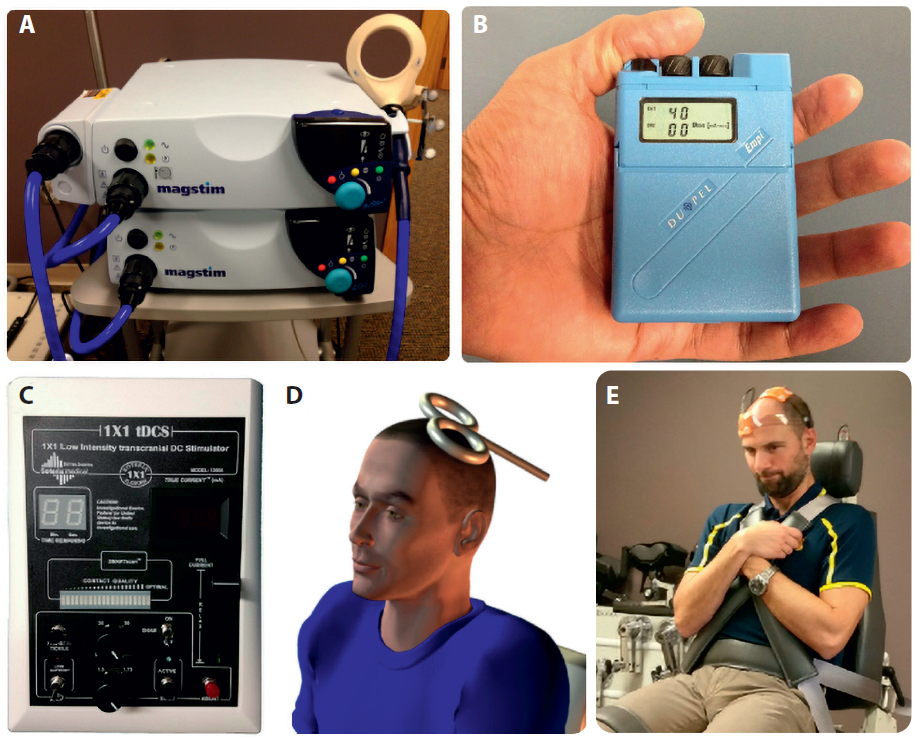
Techniki NSM dzielą się zasadniczo na dwa rodzaje, każdy z odrębnym mechanizmem działania. Przezczaszkowa stymulacja magnetyczna (ang. transcranial magnetic stimulation – TMS) indukuje słabe prądy elektryczne w mózgu przy użyciu zwoju magnetycznego umieszczonego nad skórą głowy w tym rejonie mózgu, który ma być stymulowany (ryc. 1A, D).
Drugi rodzaj metod NSM to grupa technik stymulacji elektrycznej znanych jako przezczaszkowa stymulacja prądowa (ang. transcranial current stimulation – tCS). Istnieją różne metody tCS, jednak najlepiej przebadaną i najczęściej stosowaną jest przezczaszkowa stymulacja stałoprądowa (ang. transcranial direct current stimulation – tDCS) (ryc. 1B, C, E). Metoda tDCS zmienia pobudliwość mózgu przy pomocy słabego (0,5–2 mA) prądu elektrycznego przekazywanego do gąbek namoczonych w roztworze soli umieszczonych nad stymulowanym miejscem.
Inna zyskująca na popularności metoda tCS to przezczaszkowa stymulacja prądem zmiennym (ang. transcranial alternating current stimulation – tACS); ze względu na ograniczoną liczbę badań nad tą metodą mniej wiadomo na temat jej klinicznej skuteczności.
Ryc. 1. Schematy TMS i tDCS.
Zasady działania stymulacji mózgu
TMS może być przeprowadzana w formie stymulacji pojedynczym impulsem, impulsami sparowanymi lub impulsami powtarzanymi (ang. repetitive transcranial magnetic stimulation – rTMS). Metody pojedynczych impulsów oraz impulsów sparowanych stosowane są zwykle do badania fizjologii i plastyczności kory mózgowej.
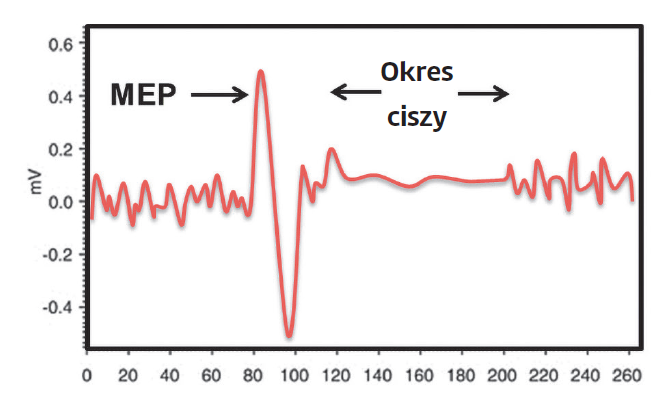
Podczas stymulacji ruchowego obszaru mózgu powyżej pewnego progu dochodzi do powstawania neuroelektrycznych sygnałów zwanych ruchowymi potencjałami wywołanymi (ang. motor evoked potentials – MEP), które można monitorować przy pomocy elektromiografii (EMG) powierzchniowej (rys. 2). MEP-y mogą być generowane podczas spoczynku mięśni albo podczas ich skurczu. Zwykle większe MEP-y uzyskuje się łatwo, gdy badany wykonuje w tle niewielki skurcz (około 5–10% maksymalnego). Jeśli ruchowy potencjał zostanie wywołany podczas skurczu w tle, dochodzi do przerwania zależnego od woli skurczu mięśni, co można z łatwością śledzić i badać przy użyciu EMG. Zjawisko to nazywane jest okresem ciszy (ryc. 2); uważa się, że dochodzi do niego przy udziale receptorów kwasu gamma-aminomasłowego (GABA). Na amplitudę i opóźnienie ruchowych potencjałów wywołanych oraz na czas trwania okresów ciszy wpływają stany patologiczne. Dlatego ruchowe potencjały wywołane mogą służyć jako pożyteczne kliniczne narzędzie do diagnozowania i oceny pewnych zaburzeń ośrodkowego układu nerwowego, takich jak stwardnienie rozsiane, a także do prognozowania odzyskiwania sprawności ruchowej po udarze.
Ryc. 2. Schemat ruchowych potencjałów wywołanych generowanych podczas przezczaszkowej stymulacji magnetycznej
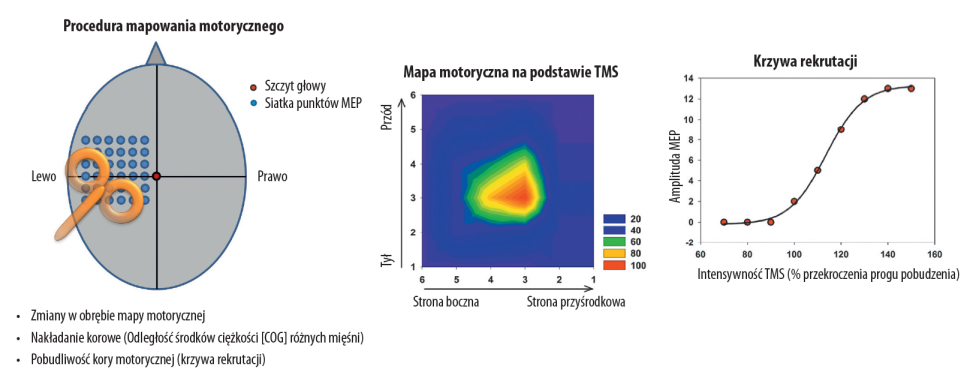
Ruchowe mapy mózgu można także generować, stymulując kilka punktów otaczających "hotspot" mięśnia (region mózgowej kory ruchowej kontrolujący ten mięsień) (ryc. 3). Gdy cewka umieszczona jest bezpośrednio nad hotspotem mięśnia, amplituda MEP powinna być większa w porównaniu z pomiarem przeprowadzonym przy zwoju umieszczonym daleko od tego hotspotu. Mapy takie mogą być przydatne podczas badania zmian neuroplastycznych w mózgu, do których doszło w wyniku urazu lub zabiegu (np. powiększenie lub skurczenie się obszaru mapy). Pobudliwość mózgu można badać przy użyciu pojedynczej odpowiedzi MEP uzyskanej z hotspota lub dzięki analizie krzywych bodziec–reakcja (tzn. krzywych rekrutacji) ruchowych potencjałów wywołanych (ryc. 3). Zwykle krzywe bodziec–reakcja mają przebieg sigmoidalny i charakteryzują się większym nachyleniem przy większej pobudliwości kory mózgowej.
Przy przezczaszkowej stymulacji magnetycznej impulsami sparowanymi do tego samego lub różnych obszarów mózgu wysyłane są dwa impulsy oddzielone pewnym interwałem czasowym. Metody impulsów sparowanych używa się głównie do badania wewnątrzkorowego i międzypółkulowego hamowania (lub facylitacji), co jest niezwykle pomocne w zrozumieniu zmian patofizjologicznych zachodzących w układach kory mózgowej po urazie lub uszkodzeniu układu nerwowego. Pomagają one także w ustalaniu mechanizmów biorących udział w regeneracji systemu nerwowego po fizjoterapii lub leczeniu farmakologicznym.
Ryc. 3. Schemat mapowania ruchowego i krzywa rekrutacji ruchowych potencjałów wywołanych.
Do czego można wykorzystać NSM?
Powtarzalna TMS (rTMS) stosowana jest często do przeprowadzenia neuromodulacji i uzyskania neuroplastyczności i może skutkować wydłużonymi zmianami pobudliwości, niezanikającymi od razu po stymulacji. Zwykle kierunek neuromodulacji zależy od częstotliwości zastosowanej podczas stymulacji, a konkretnie rTMS o wysokiej częstotliwości zwiększa pobudliwość kory mózgowej, a rTMS o niskiej częstotliwości pobudliwość tę zmniejsza.
Jednakże stymulacja przy zastosowaniu wyładowań theta (odmiana rTMS o wysokiej częstotliwości) może wywołać zarówno redukcję, jak i facylitację pobudliwości kory mózgowej w zależności od czasu trwania wyładowania – stymulacja przerywanymi wyładowaniami theta zwiększa pobudliwość kory, a ciągła stymulacja wyładowaniami theta pobudliwość tę zmniejsza.
Metoda tDCS stanowi przede wszystkim technikę neuromodulacji, którą stosuje się przy użyciu stymulatora o akumulatorowym napędzie z elektrodami umieszczanymi na skórze głowy (ryc. 4). W odróżnieniu od TMS tDCS nie wyzwala potencjału czynnościowego. Przepływ prądu wpływa na pobudliwość neuronów poprzez zmianę spoczynkowego potencjału błonowego neuronów i pozostawia po sobie skutki (czyli przedłużoną zmianę pobudliwości neuronów). Uważa się, że skutki te powstają dzięki modulacji synaps glutaminergicznych i GABAergicznych.
Metodę tDCS można stosować do otrzymywania efektu pobudzającego lub hamującego, w zależności od polaryzacji stymulacji. Konkretnie stymulacja anodowa daje efekt depolaryzacyjny, który zwiększa pobudliwość neuronów; stymulacja katodowa zaś daje efekt hiperpolaryzacyjny, który zmniejsza pobudliwość neuronów.
Istnieją różne sposoby montażu elektrod (tzn. ich umiejscowienia) przy tDCS i obecnie brak jest pełnej zgody co do najlepszej konfiguracji dla optymalnego odzyskiwania sprawności ruchowej po urazie neurologicznym. Metoda tDCS ma pewną ważną przewagę nad innymi metodami nieinwazyjnej stymulacji mózgu. Jest to mianowicie technologia niskokosztowa, przenośna i może być łączona z innymi formami leczenia (np. z treningiem motorycznym). Co więcej, w literaturze nie ma zgłoszeń poważnych efektów ubocznych – znajdują się jedynie doniesienia o zwykłych efektach ubocznych związanych ze stymulacją prądem stałym, takich jak mrowienie, swędzenie czy pieczenie.
Metoda tDCS to obiecująca niefarmakologiczna forma terapii, dzięki poręczności i niskim kosztom stosowania. Wykazała ona korzystny wpływ na wiele problemów zdrowotnych, w tym na niedobory motoryczne, przewlekły ból, depresję i inne zaburzenia neuropsychiatryczne, zaburzenia mowy i spadek funkcji poznawczych.
Metody NSM pierwotnie używano w zaburzeniach neuropsychiatrycznych i neurologicznych, lecz zakres jej zastosowania się poszerza. Jak już wspomniano, różne badania wykazały terapeutyczną skuteczność NSM w zaburzeniach depresyjnych, zwłaszcza u tych pacjentów, którzy nie reagowali dobrze na konwencjonalną terapię farmakologiczną. Amerykańska Agencja Żywności i Leków dopuściła rTMS do stosowania w leczeniu depresji. W wielu badaniach wykazano także, że zarówno tDCS, jak i rTMS to obiecujące metody leczenia przewlekłego bólu i fibromialgii.
W ostatnich latach przeprowadzono pewną liczbę badań oceniających wykonalność i skuteczność NSM w modulowaniu pobudliwości kory mózgowej oraz w ułatwianiu nauki poruszania się i odzyskiwania sprawności po udarze lub porażeniu mózgowym. Większość wyników sugeruje, że zarówno TMS, jak i tDCS to bezpieczne i skuteczne sposoby modulowania pobudliwości kory mózgowej, nasilania adaptacji i nauki ruchowej oraz wpływania na konsolidację pamięci motorycznej u zdrowych osób dorosłych, jak również u pacjentów neurologicznych. Co ważne, u osób z zaburzeniami neurologicznymi modulacjom takim często towarzyszy poprawa sprawności ruchowej i wyników klinicznych.
W większości badań oceniano odzyskiwanie sprawności ruchowej i poprawę funkcjonowania kończyn górnych, natomiast w kilku przyjrzano się także potencjalnej roli NSM w poprawianiu funkcji chodzenia po udarze czy porażeniu mózgowym. Wyniki tych badań także wskazują, że NSM, połączona z treningiem mobilności/chodzenia to bezpieczna i wykonalna metoda poprawiania funkcji chodzenia.
Badania wydają się być znacząco niejednorodne, jako że niedawny raport z Bazy Danych Przeglądów Systematycznych Cochrane’a nie poparł korzystania z powtarzalnej TMS w leczeniu dysfunkcji motorycznych po udarze.
Ryc. 4. Zastosowanie tDCS.
NSM - jak dawkować stymulację?
Stopień neuromodulacji i związana z nim plastyczność behawioralna czy funkcjonalna zależą od dawkowania stymulacji. Ogólnie biorąc, większa intensywność stymulacji lub dłuższy jej czas trwania będzie skutkować większą neuromodulacją.
Zwiększone dawkowanie bodźca zwiększy także potencjalne ryzyko niepożądanych efektów ubocznych, łącznie z drgawkami, bólem głowy i oparzeniami. W związku z tym ustalono zasady bezpieczeństwa przy stosowaniu TMS i tDCS w warunkach badawczych i klinicznych. Obie te metody uważane są za bezpieczne z rzadkim występowaniem poważnych niepożądanych efektów ubocznych, gdy przestrzegane są zasady bezpieczeństwa ustalone dla tych procedur. Dlatego przed zastosowaniem TMS/tDCS niezbędne jest odpowiednie szkolenie i zapoznanie się z wytycznymi odnośnie do bezpieczeństwa, etyki i stosowania tych metod.
Należy także odnotować, że techniki NSM nie zostały zatwierdzone przez Agencję Żywności i Leków i są uważane za będące w trakcie badań (z wyjątkiem terapii depresji). Wraz z rozwojem wiedzy naukowej na temat NSM potencjalne zastosowania tej metody się poszerzą, a organy zatwierdzające prawdopodobnie dopuszczą jej użycie w leczeniu dużej liczby innych problemów zdrowotnych.