Mianem przewlekłego określa się ból, który trwa dłużej niż normalny okres rekonwalescencji, lub ból towarzyszący przewlekłemu problemowi zdrowotnemu. Patologia bólu przewlekłego jest ogromnie zróżnicowana; w jej etiologii należy uwzględnić m.in.: występujący w wywiadzie uraz, infekcje, zaburzenia czy choroby, łącznie z zapaleniem stawów i nowotworami.
Elektryczna stymulacja obszarów ośrodkowego układu nerwowego przy pomocy wszczepionych chirurgicznie stymulatorów okazała się przynosić ulgę w bólu. By uniknąć ryzyka i efektów ubocznych operacji, obecnie opracowywane są nieinwazyjne metody dające możliwość elektrycznego stymulowania motorycznej kory mózgowej poprzez czaszkę.
Idea, zgodnie z którą polaryzacja mózgu może modulować neuroplastyczność, doprowadziła do zastosowania przezczaszkowej stymulacji stałoprądowej (ang. transcranial direct current stimulation – tDCS), przezczaszkowej stymulacji magnetycznej (ang. transcranial magnetic stimulation – TMS) oraz przezczaszkowej stymulacji prądem zmiennym (ang. transcranial alternating current stimulation – tACS) jako dodatku do protokołów terapeutycznych.
Przezczaszkowa stymulacja stałoprądowa (tDCS)
To nowa metoda stymulacji mózgu mająca potencjał zmieniania plastyczności kory mózgowej i torowania mózgu w celu wzmacniania procesów uczenia się. Badania wykazały, że tDCS różnych obszarów kory mózgowej skutkuje modyfikacjami funkcji percepcyjnych, kognitywnych i behawioralnych oraz zaburzeń mózgu. Jony dodatnie przyciągane są przez elektrodę ujemną (katodę), podczas gdy jony ujemne przyciągane są przez elektrodę dodatnią (anodę). Ta polaryzacja zmienia potencjały błonowe, a tym samym – pobudliwość tkanki nerwowej. Wykazano, że wykorzystanie anody jako elektrody aktywnej (anodowe tDCS) zwiększa pobudliwość kory mózgowej, podczas gdy wykorzystanie katody (katodowe tDCS) pobudliwość tę zmniejsza.
Upraszczając, tDCS nie powoduje wyładowania neuronów spoczynkowych (pod postacią ich nadmiernie wygórowanego pobudzenia), a raczej – działając na poziomie potencjałów błonowych – moduluje stopień spontanicznej aktywności elektrycznej neuronów. Przypuszcza się, że sposób działania tDCS oparty jest na procesach długotrwałego wzmacniania synaptycznego (ang. long term potentiation – LTP) i długotrwałego hamowania synaptycznego (ang. long term depression – LTD) jako przejawów neuroplastyczności. długotrwałe wzmacnianie to wzajemne sprzęganie neuronów w celu łatwiejszego przekroczenia progu pobudzenia, natomiast długoterminowe hamowanie to zjawisko inhibicji zachodzące pomiędzy dwoma neuronami.
Efekty te osiąga się głównie poprzez zmianę zdolności przewodnictwa synaptycznego. W tDCS mamy do czynienia ze zmianą zdolności przewodnictwa synaps poprzez modyfikacje wewnątrzkomórkowych poziomów cyklicznego adenozynomonofosforanu i wapnia. Ponadto zarówno LTP, LTD, jak i efekty tDCS są zależne od syntezy białek.
Choć dokładne mechanizmy są niejasne, uważa się, że zmiany pobudliwości kory mózgowej po zastosowaniu tDCS odzwierciedlają zmiany w funkcji synaps, przypominające zmiany neuroplastyczne.
Zastosowanie kliniczne: tDCS może być stosowana na dwa sposoby
- do zmieniania stanu stałego kory mózgowej poprzez zwiększanie lub zmniejszanie jej pobudliwości;
- do torowania kory mózgowej (zjawisko primingu) celem zwiększenia jej podatności na inne zabiegi terapeutyczne.
Pojęcie torowania (ang. priming) mózgu w celu wzmocnienia uczenia się jest szczególnie interesujące dla fizjoterapeutów, ponieważ wyniki ich pracy można poprawić, łącząc tDCS z tradycyjnymi terapiami, takimi jak reedukacja funkcji motorycznych, obwodowa stymulacja elektryczna (np. przezskórna elektryczna stymulacja nerwów TENS, funkcjonalna stymulacja elektryczna FES) czy leczenie farmakologiczne. tDCS stosuje się w stanach patologicznych w celu redukcji bólu i poprawy funkcji motorycznych.
Stymulacja kory mózgowej — rozmieszczenie elektrod
Rozmieszczenie elektrod zależy od tego, jaki obszar mózgu jest celem stymulacji oraz czy pożądanym efektem ma być zwiększenie czy zmniejszenie pobudliwości kory mózgowej.
Przy pomocy tDCS można stymulować wiele obszarów mózgu, łącznie z pierwszorzędową korą ruchową, pierwszorzędową korą czuciową, korą przedczołową i wzrokową. W każdym przypadku czynną elektrodę umieszcza się nad docelowym obszarem mózgu, a elektrodę odniesienia (bierną) nad miejscem nieaktywnym, takim jak biegun czołowy kory mózgowej.
Aby uniknąć uszkodzeń tkanki mózgowej, gęstość prądu stosowanego podczas tDCS nie powinna przekraczać 25 mA/cm2, a łączna zastosowana gęstość powierzchniowa ładunku nie powinna być większa niż 216 C/cm2. Współczesne protokoły tDCS wykorzystują prądy stałe pomiędzy 0,2 a 2 mA, dające maksymalną gęstość prądu rzędu 28,5 mA/cm2 i gęstość powierzchniową ładunku równią 0,022 C/cm2 przy użyciu standardowej elektrody.
Przy tych poziomach nie dochodzi do wytwarzania ciepła pod elektrodami, a markery uszkodzeń neuronów po zastosowaniu tDCS pozostają niezmienione.
Pięciominutowa sesja zmienia pobudliwość kory mózgowej, co utrzymuje się przez nie dłużej niż 5 minut. Jednakże tDCS zastosowana przez 13 minut wywołuje zmiany, które trwają jeszcze przez 90 minut po zakończeniu stymulacji.
Liczne badania potwierdzają, że przezczaszkowa stymulacja o niskiej intensywności jest bezpieczna dla ludzi i wiąże się jedynie z rzadkimi i stosunkowo nieznacznymi efektami ubocznymi (Poreisz, Boros, Antal & Paulus, 2007). tDCS nie podnosi poziomu molekularnych markerów uszkodzeń neuronów w osoczu, takich jak neuroswoista enolaza (Nitsche & Paulus, 2001) czy asparaginian N-acetylu (Rango i in., 2008). Ponadto ani rezonans magnetyczny z kontrastem, ani badania EEG nie wykazały żadnych patologicznych zmian związanych z zastosowaniem tDCS (Iyezr i in., 2005; Nitsche, Niehaus i in., 2004). Co więcej, nie zaobserwowano u ludzi żadnych przypadków ataków epileptycznych wywołanych przez tDCS (Poreisz i in., 2007).
Powtarzalna przezczaszkowa stymulacja magnetyczna (ang. repetitive transcranial magnetic stimulation – rTMS)
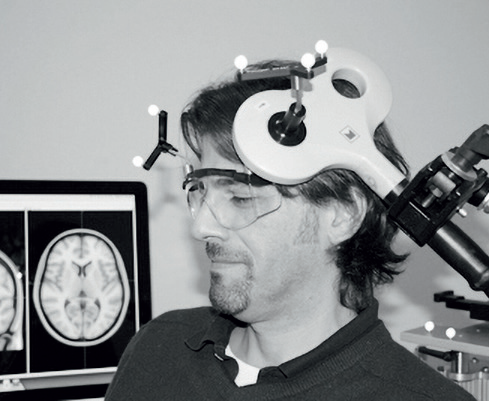
Metoda rTMS indukuje prądy elektryczne w korze mózgowej. Efekt zależy od częstotliwości impulsów, przy czym wysoka częstotliwość (≥5 Hz) rTMS nad M1 skutkuje pobudzeniem kory mózgowej i zmniejszeniem bólu. Typowa cewka ma charakter ogniskowy, z około jednocentymetrowym głównym obszarem stymulacji. Pozwala to na bardzo precyzyjną stymulację, ale jednocześnie wymaga dokładnej nawigacji.
(ok. 2 tygodni) po szeregu sesji
Raportów na temat długoterminowego leczenia przy pomocy rTMS jest niewiele. Wykazano, że redukcja bólu po pojedynczej sesji rTMS prognozuje pozytywną reakcję na stymulację zewnątrzoponową, podczas gdy brak reakcji na rTMS nie przedstawia wartości jako kryterium wykluczenia operacji.
Przezczaszkowa stymulacja szumów tła (ang. transcranial random noise stimulation – tRNS)
Nowatorska metoda tRNS polega na zastosowaniu prądu zmiennego o przypadkowo zmieniającej się częstotliwości, co w wyniku daje falę "białego szumu". Wykazano, że 10 minut przezczaszkowej stymulacji o natężeniu 1 mA przy przypadkowo zmieniającym się szumie o częstotliwości 100–640 Hz skutkuje zwiększoną pobudliwością M1 u osób zdrowych, trwającą dłużej niż 1 godzinę.
Zakłada się, że neurony zostają aktywowane bez względu na kierunek przepływu prądu. Domniemany mechanizm polega na tym, że zmieniające się pole elektryczne powoduje powtarzające się otwieranie i zamykanie kanałów sodowych bramkowanych napięciem, co skutkuje wielokrotnymi napływami jonów i przesunięciem potencjału błonowego w kierunku potencjału czynnościowego.
Bezpieczeństwo tRNS oszacowano przy pomocy pomiarów neuroswoistej enolazy (NSE, czuły marker uszkodzeń neuronów, którego poziom zwiększa się w epilepsji) oraz elektroencefalografii (EEG).
Nie stwierdzono żadnego wpływu ani na NSE, ani na EEG. tRNS nadaje się do badań zaślepionych, jako że zwykle stymulacji tej się nie zauważa, a próg odczucia przezskórnego jest przy tRNS wyższy niż przy tDCS.
W badaniu dyskryminacji wzrokowej tRNS zastosowana nad korą wzrokową poprawiła zdolność widzenia w porównaniu z tDCS i symulowaną stymulacją (placebo).
Przewlekły ból jest jedną z głównych przyczyn niepełnosprawności, odpowiednie radzenie sobie z nim będzie pociągać za sobą lepsze rokowanie i wyższy współczynnik sukcesu terapeutycznego. Stwierdzono związek między przewlekłością problemu a zmianami wywoływanymi przez ból, tak więc przeprowadzona w porę interwencja zapobiega pogorszeniu się problemu.