Wiele towarzystw naukowych zaleca rehabilitację naczyniową pierwszego rzutu (poziom A) pacjentom z chromaniem przestankowym (stopień 2. według klasyfikacji Leriche’a i Fontaine’a)1,2, co stanowi dla nich codzienne wyzwanie.
Dzieje się tak z wielu powodów: trudno jest zakwalifikować chorego do programu ćwiczeń czy włączyć specjalistę leczącego arteriopatię do postępowania terapeutycznego, które ze względu na wieloczynnikowy charakter choroby musi być wielodyscyplinarne. Należy też wiedzieć, jak dostosować protokół do stopnia zaburzenia i jego wpływu na inne obszary organizmu3.
Rehabilitacja w zakresie możliwości chodzenia pozostaje podstawową metodą leczenia arteriopatii kończyn dolnych. Pacjentowi można zaproponować różne protokoły. Wszystkich chorych z niedokrwistością wysiłkową powinno się systematycznie kierować do ośrodków rehabilitacyjnych w celu poprawy chodu – podobnie jak to się dzieje w przypadku rehabilitacji kardiologicznej4.
Choroby naczyń obwodowych - epidemiologia
Choroba obturacyjna tętnic obwodowych (peripheral arterial obstructive disease, PAOD) to częsta choroba ogólnoustrojowa, zwłaszcza w stopniu 1. i 2. według klasyfikacji Leriche’a i Fontaine’a. Pacjent ma zapalenie wielu tętnic, które może wpływać na inne lokalizacje, w tym serce i mózg. Według międzynarodowego rejestru REACH połowa chorych z PAOD miała zaatakowany przynajmniej jeden inny obszar tętniczy w porównaniu z 1/3 osób z zaburzeniami w obrębie naczyń mózgowych i 1/4 tych z chorobą wieńcową5,6.
Faktycznie kwestionariusz chromania stosowano w badaniach europejskich i amerykańskich, w których stwierdzono, że częstość występowania chromania przestankowego wynosi 1% w grupie osób przed 50. rokiem życia i tylko 6% wśród pacjentów po 65. roku życia. Częstość występowania PAOD wzrosła znacznie – o prawie 25% – w latach 2000–2010: na początku tego okresu wynosiła ok. 5% w populacji poniżej 50. roku życia, a w 2010 r. osiągnęła poziom ok. 20% zarówno wśród mężczyzn, jak i kobiet po 80. roku życia (w krajach o wysokim dochodzie)6,7.
Główne czynniki ryzyka naczyniowego, sprzyjające rozwojowi PAOD, to palenie tytoniu i cukrzyca. Pierwszy z nich podwaja lub potraja prawdopodobieństwo zachorowania, a drugi podwaja lub zwiększa je czterokrotnie – przy jednoczesnym wzroście ryzyka związanego z czasem trwania cukrzycy. Wysokie ciśnienie tętnicze i wysoki poziom lipoproteiny o niskiej gęstości (ang. low-density lipoprotein, LDL) również są związane z PAOD, ale w mniejszym stopniu6.
Choroby naczyń obwodowych - patofizjologia
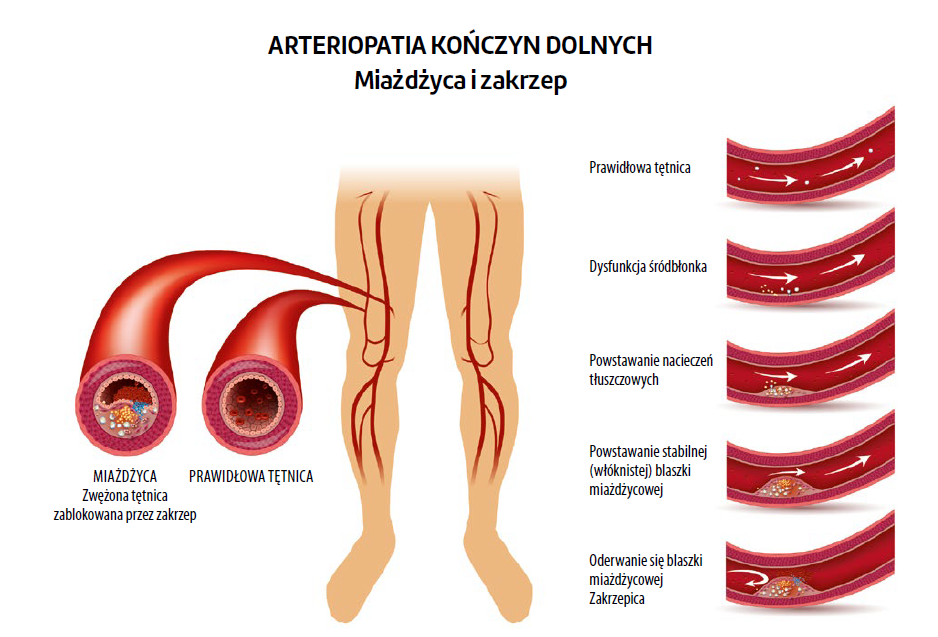
Wraz z wiekiem i procesem starzenia postępuje twardnienie ścian tętnic – ta nieunikniona ewolucja ma charakter chorobotwórczy. Miażdżyca przekształca drzewo tętnicze w sztywną "rurę", coraz mniej zdolną do zmiany swego kalibru i regulacji przepływu krwi. Peryferyjne obszary organizmu są coraz gorzej odżywiane8- 11, a proces ten przyspieszają jeszcze inne czynniki ryzyka sercowo-naczyniowego (cukrzyca, nadciśnienie tętnicze, otyłość, palenie tytoniu, płeć męska, wiek pomenopauzalny u kobiet itp.). Dlatego też dochodzi do powstawania blaszki miażdżycowej, która blokuje światło tętnic, wywołując symptomy kliniczne chromania przestankowego10,11.
Mechanizmy poprawy dystansu chodzenia
- Zmiany metaboliczne: PAOD powoduje dysfunkcję mitochondriów przez gromadzenie się pośrednich metabolitów (acylokarnityna). Regularny trening chodu zmniejsza stężenie acylokarnityny i poprawia funkcję mitochondriów.
- Stymulacja angiogenezy: Wysiłek fizyczny powoduje wzrost poziomu VEGF i HIF-1 (czynników wywołanych niedotlenieniem), które sprzyjają angiogenezie. • Poprawa w zakresie czynników biomechanicznych Wykazano, że u wytrenowanego pacjenta dojdzie do korzystnego zmniejszenia zużycia tlenu przez mięśnie dzięki wsparciu ruchu i wzorca chodu.
- Czynniki krwotoczne: Ćwiczenia poprawiają lepkość krwi i plastyczność czerwonych krwinek.
- Czynniki zapalne: Klasycznie podwyższony w przebiegu PAOD poziom markerów pejoratywnej ewolucji układu sercowo- -naczyniowego zmniejsza się po trzech miesiącach rehabilitacji.
- Czynniki śródbłonkowe: Kilka badań wykazało po rehabilitacji poprawę funkcji śródbłonka – znaczenie tego faktu podkreślono ze względu na rolę w poprawie dystansu chodzenia u pacjentów ćwiczących wyłącznie kończyny górne.
- Poprawa progu bólu: Jak ustalono w badaniu Gardnera, pozwala to na lepsze przestrzeganie przez pacjenta zaleceń terapeutycznych.
- Zarządzanie czynnikami ryzyka: Ćwiczenia poprawiają profil ciśnienia tętniczego, obniżają poziom cholesterolu LDL, regulują cukrzycę i wspomagają stabilizację masy ciała.
- Łagodzenie zaburzeń nastroju: Wraz ze wzrostem czynności życia codziennego złagodzeniu ulegały objawy zespołu depresji reaktywnej i następowała poprawa funkcji poznawczych12.
Techniki rehabilitacji chodu
Rehabilitację naczyniową u chorych z chromaniem przestankowym – niedokrwieniem wysiłkowym – zaleca obecnie w pierwszej linii leczenia (poziom A) wiele towarzystw naukowych. Powodów jest wiele. Po pierwsze, znaczący jest wpływ na jakość życia przez poprawę samooceny, wynikającą z polepszenia możliwości funkcjonalnych. Po drugie, zmniejsza się ryzyko powikłań i obniża śmiertelność – dzięki udziałowi w programie edukacji terapeutycznej13,14. Program taki jest niezbędny, aby pacjent przestrzegał długoterminowo zasad dotyczących higieny i diety, z uwzględnieniem zaprzestania palenia tytoniu, adherencji terapeutycznej (statyny, leki przeciwpłytkowe, inhibitory konwertazy angiotensyny), odpowiednio dostosowanej i regularnej aktywności fizycznej oraz oczywiście edukacji żywieniowej. Czas trwania, częstotliwość i intensywność ruchu powinny być zalecane według określonych wytycznych. Ostatecznie uzyskuje się wydłużenie dystansu chodzenia – średnio o 150% – które można by wytłumaczyć poprawą ekstrakcji i obwodowego wykorzystania tlenu14-16.
Główne mechanizmy zaangażowane w poprawę dystansu chodzenia obejmują adaptacje sercowo-oddechowe, krążeniowe, biochemiczne (działanie czynników wzrostu, takich jak VEGF i FGF-2) i mięśniowo-szkieletowe. Dobrze zsyntetyzowali to w niedawnym badaniu Brenner i wsp17.
Rehabilitację można prowadzić w ośrodku rehabilitacyjnym wyspecjalizowanym w patologiach naczyniowych w warunkach pełnej hospitalizacji, ambulatoryjnie, jak również w domu pacjenta. Niektórzy autorzy wykazali zasadniczo identyczną skuteczność, jeśli chodzi o dystans marszu u chorych rehabilitowanych w placówkach i pod nadzorem w domach18,19. Wszystkim pacjentom z PAOD należy zaproponować regularne spacery19.
Wskazaniami do rehabilitacji chodu obecnie są20:
- niedokrwienie wysiłkowe, szczególnie w przypadku zmian udowych, ale również u pacjentów ze zmianami biodrowymi lub dystalnymi – jeśli wyniki są mniej zadowalające
- niedokrwienie spoczynkowe u pacjenta z przeciwwskazaniem do zabiegu chirurgicznego – w takim przypadku preferowane jest prowadzenie rehabilitacji w specjalistycznym ośrodku
- po zabiegu chirurgicznym lub procedurach wewnątrznaczyniowych, a nawet po amputacji – tę orientację terapeutyczną należy rozważać w porozumieniu z chirurgiem naczyniowym.
Konieczna jest wstępna ocena, która musi mieć charakter kompleksowy i obejmować dokładne oględziny oraz badanie kliniczne z palpacją tętna obwodowego i osłuchiwaniem dróg naczyniowych22.
Ewaluacja tętnic kończyn dolnych (echokardiografia dopplerowska, indukowane pluripotencjalne komórki macierzyste) i – jeśli to możliwe – mikrokrążenia (TcPO2) pozwala wykryć inne lokalizacje choroby miażdżycowej, takie jak choroba niedokrwienna serca, zwężenie tętnicy szyjnej lub tętniak aorty brzusznej. Ocenę uzupełnia systematyczne poszukiwanie upośledzenia układu mięśniowo- szkieletowego, które może wymagać adaptacji programu rehabilitacji22.
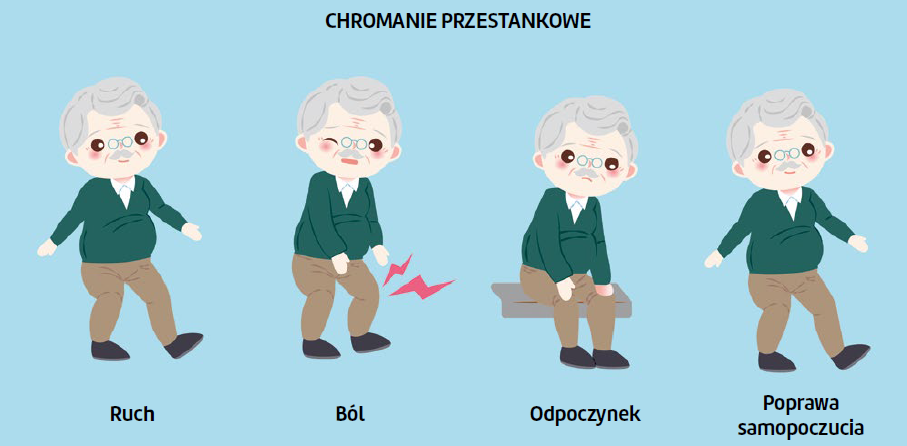
Od wielu lat towarzystwa naukowe opowiadają się za "protokołem Gardnera"19, czyli chodzeniem przez 30-60 minut, co najmniej trzy razy w tygodniu, przez okres od trzech do sześciu miesięcy. Ewentualne chromanie powinno wystąpić przed upływem 10 minut. W tym protokole pacjent powinien kontynuować chodzenie po pojawieniu się pierwszych objawów dyskomfortu – aż do wystąpienia tzw. umiarkowanego bólu, ocenianego na 7/10 według wizualnej skali analogowej (visual analogue scale, VAS). W tym momencie należy koniecznie się zatrzymać. Przed wznowieniem spaceru pacjent powinien odpoczywać co najmniej przez 5 minut19. Proponowany protokół należy oczywiście dostosować do charakterystyki danego pacjenta i wszelkich chorób współistniejących. Rehabilitacja chodu z bólem pojawiającym się na każdym odcinku spaceru prowadzi do lepszych wyników, ale może zniechęcać osłabionych chorych, którzy nie chcą cierpieć. Gardner wykazał, że przy równoważnym czasie pracy mniejsza intensywność wysiłku (40% vs. 80%) umożliwia uzyskanie identycznych wyników23.
Metoda interwałów treningowych polega na naprzemiennych partiach treningu o wysokiej intensywności i aktywnych okresach odpoczynku z submaksymalnym wysiłkiem. Stosuje się ją w kardiologii z dobrymi wynikami. W 2011 r. Villemur i wsp. we wstępnym badaniu przetestowali ten protokół u pacjentów z niedokrwieniem wysiłkowym. Wykazali podwojenie dystansu chodzenia w ciągu dwóch tygodni. Wyniki te wymagają jednak potwierdzenia24.
Wymagany czas trwania wsparcia nie jest określony ze względu na liczne zmienne czynniki, czyli utrzymujące się i pogłębiające nieprawidłowości. Konsensus zaleca jednak wstępny program nadzorowanych ćwiczeń24, obejmujący co najmniej dwie26 do trzech27 30-60-minutowych sesji tygodniowo. Ich długość jest zwykle dostosowana do możliwości pacjenta. 30-minutowe sesje odbywają się dwa razy dziennie, a 60-minutowe – raz dziennie28. Program realizowany jest przez jeden29, trzy28,30-32, cztery33, sześć33-35 lub dwanaście27 do piętnastu miesięcy26. Wiele ograniczeń lub adaptacji wynika z wieloogniskowego charakteru choroby, towarzyszących jej niepełnosprawności30,36 i szczególnych okoliczności (amputacja, hemiplegia, otyłość)28,37,38. Różnorodność programów rehabilitacyjnych jest znaczna.
Program rehabilitacji naczyniowej składa się z co najmniej trzech cotygodniowych godzinnych sesji przez okres od trzech do sześciu miesięcy w specjalistycznym ośrodku, w domu pacjenta (pod nadzorem) lub w gabinecie fizjoterapeutycznym39. W każdym przypadku musi mieć dwie komplementarne osie: poprawę kondycji poprzez wysiłek oraz edukację terapeutyczną pacjenta.
Istnieją dwie fazy przygotowania do aktywności: ewaluacyjna oraz następująca po niej faza ponownego wprowadzenia. Celem ewaluacji jest ilościowe określenie ograniczeń w chodzeniu pacjenta i ukierunkowanie procedur leczniczych mających na celu przywracanie sprawności przez ocenę tolerancji wysiłku i wykrycie nietolerancji wieńcowej lub innych przeciwwskazań39,40. Można zastosować kilka metod oceny zdolności do aktywności fizycznej, które wymieniono poniżej.
Metody oceny zdolności do aktywności fizycznej:
- Pomiar odległości chodzenia po płaskim terenie do czasu pojawienia się skurczu – słabo wystandaryzowany test o niskim stopniu powtarzalności39, umożliwia jednak poszukiwanie zaburzeń chodu, które można zaobserwować w przebiegu ciężkiego chromania i które w razie potrzeby będą wymagały korekty.
- Sześciominutowy test marszowy: standaryzowany i walidowany w ocenie przewlekłych niepełnosprawności. Bada wytrzymałość z dobrą powtarzalnością40.
- Testy na bieżni, w celu monitorowania postępów pacjenta w warunkach standaryzowanych i dzięki temu powtarzalnych co do prędkości i nachylenia. Najczęściej są to próby ze stopniowym wzrostem intensywności41. Można je przeprowadzać z obciążeniem stałym (niezmienna prędkość i nachylenie) lub progresywnym42.
- Test ergometryczny na rowerku: może być przydatny w przypadku otyłości lub zaburzeń chodu związanych z upośledzeniami ortopedycznymi lub neurologicznymi. Jest on interesujący z punktu widzenia pulmonologii i kardiologii, ale nie sprawdza ułomności związanej z chorobą tętnic.
- Elektrokardiograficzna próba wysiłkowa kończyny górnej to dobra alternatywa, gdy kończyny dolne są niesprawne; czułość jest zbliżona do testu na bieżni43.
Druga faza przywracania sprawności jest spersonalizowana, dostosowana do każdego przypadku i uwzględnia wyniki uzyskane przez pacjenta podczas oceny. Wprowadzony protokół może ewoluować w zależności od ewolucji choroby tętnic. Ważne jest wyznaczenie odpowiednich i realistycznych celów, tak by nie zniechęcać pacjentów40. Istnieją dwa główne rodzaje technik, które są często kojarzone: trening ogólny i regeneracja analityczna.
Trening ogólny polega na wykonywaniu różnych związanych z chodzeniem ćwiczeń – na bieżni lub cykloergometrze – w celu zaangażowania kończyn dolnych i górnych, a tym samym maksymalnej objętości mięśni. Ergometryczna regeneracja, obejmująca kończyny górne i tułów, może być przydatna, gdy nogi są niesprawne. Ma pozytywne działanie ogólnoustrojowe i poprawia dotlenienie tkanek na poziomie kończyn dolnych44.
Regeneracja analityczna (segmentowa) kończyn dolnych to zestaw technik ukierunkowanych na budowę masy mięśniowej przez skurcz mięśni w wyniku postępującego oporu oraz zwiększonego przepływu krwi w sieci tętnic. Metoda ta jest zalecana rzadziej, ponieważ jej ogólnoustrojowy wpływ jest mniej istotny w porównaniu z treningiem ogólnym45. Dynamiczne skurcze mięśni z częstotliwością 20-50 na minutę, przy narastającym obciążeniu i zgodnie z tolerancją kliniczną, osiąga się dzięki unikaniu występowania przykurczów.
Inne techniki rehabilitacji mogą być stosowane w zależności od sytuacji. Są to m.in.: fizjoterapia oddechowa w przypadku towarzyszącej przewlekłej obturacyjnej choroby płuc (POChP), drenaż limfatyczny w przypadku obrzęku, mobilizacja w przypadku retrakcji i sztywności, rehabilitacja postawy i ćwiczenia propriocepcji w przypadku zaburzeń równowagi, tzw. masaże refleksyjne stymulujące mikrokrążenie – interesujące w przypadku zaburzeń troficznych lub bardzo ograniczonego chromania, a także spacery w środowisku wodnym – gdy perymetr chodzenia jest bardzo ograniczony44,45.
Elementem rehabilitacji naczyniowej może być trening na wioślarzu.
Ważne zasady programu rehabilitacyjnego dla pacjentów z chorobami naczyń obwodowych:
- Elastyczność: Ćwiczenia rozluźniające lub rozciągające są niezbędnym warunkiem wstępnym pracy mięśniowej i wytrzymałościowej. Poprawiają również elastyczność.
- Aktywne ćwiczenia analityczne: Segmentowe budowanie mięśni poprawia ich wytrzymałość i wydolność funkcjonalną. Siła skurczów jest ustalana na 20-50% siły maksymalnej, oszacowanej wcześniej, tak by pozostawać na poziomie pracy aerobowej.
- Rehabilitacja chodzenia: Ćwiczenia chodzenia wykonuje się codziennie, ustalając ich zakres na podstawie wstępnej oceny granicy możliwości. Odległość do przebycia ustala się na poziomie 80% maksymalnej wydolności, a czas odpoczynku – na poziomie 80% czasu, który upływa do ustąpienia bólu.
- Warunki pracy: Sesje trwają od 30 do 45 minut. Intensywność rehabilitacji zawsze opiera się na podstawie tętna treningowego i progu duszności. Sesje obejmują rozgrzewkę, 30-minutową fazę wytrzymałościową przy tętnie docelowym, a następnie aktywną regenerację. Faza wytrzymałościowa może przebiegać przy stałym obciążeniu lub być prowadzona w formie naprzemiennych segmentów o mniejszej intensywności i szczytów aktywności. Trening może odbywać się na różnych ergometrach (rowerku, ergometrze ręcznym, bieżni, stepperze, wioślarzu). Może mieć również formę spaceru, jazdy na rowerze na świeżym powietrzu bądź pływania.
- Fizjoterapia oddechowa: Przez cały okres rehabilitacji pacjentów, często nałogowych palaczy, interesująca jest praca nad kontrolą wentylacji. Umożliwia ona świadome oddychanie brzuszno- -przeponowe, a tym samym poprawia przyjmowanie O2.
- Edukacja terapeutyczna pacjenta: Edukacja terapeutyczna jest integralną częścią programu opieki. Powinna umożliwić utrzymanie wyników osiągniętych w czasie jego trwania. Główne poruszane tematy to: leczenie, dyslipidemia, nadwaga, kontrola ciśnienia tętniczego, cukrzyca, tytoń, aktywność fizyczna i pielęgnacja stóp44,45.
Efekty protokołów rehabilitacyjnych w chorobach naczyń obwodowych
Metaanaliza Gardnera pokazuje 180-proc. wzrost odległości pokonywanej do czasu wystąpienia bólu w stosunku do wyniku z pierwszych dwóch miesięcy (Watson i in.16 ). W przeglądzie Cochrane z 2008 r., który obejmował 22 randomizowane badania, odnotowano, że dystans ten poprawiono za pomocą rehabilitacji bardziej niż dzięki standardowej terapii medycznej – o 200%, bez powikłań sercowo-naczyniowych – i utrzymano taki stan przez ponad dwa lata46.
W ośrodkach rehabilitacyjnych, przy większym nakładzie pracy, dystans chromania można zwiększyć od czterech do pięciu razy. Terapia najlepiej działa na zmiany udowe, ale biodrowe i dystalne również można znacznie zmniejszyć. Osłabienie pośladków jest bardziej umiarkowane.
Fokkenrood46 w przeglądzie Cochrane z 2013 r. wykazał lepsze wyniki u pacjentów poddanych rehabilitacji w ośrodkach w porównaniu z tymi rehabilitowanymi w domu. Nastąpił u nich przyrost pokonywanej odległości o 160 m, a wynik ten utrzymano przez rok. Nadzór pozytywnie wpływa na przestrzeganie zaleceń i intensywność ćwiczeń. Jest on bardzo polecany przez towarzystwa medyczne ze względu na korzystny stosunek kosztów do efektywności47.
W ostatnim badaniu ERASE porównano wzrost maksymalnej odległości pokonywanej pieszo u pacjentów z chromaniem przestankowym, związanym z urazem tętnicy biodrowej lub udowej, leczonym wyłącznie wewnątrznaczyniowo lub w połączeniu z rehabilitacją chodu według protokołu Gardnera. Ten drugi algorytm zaowocował po roku lepszym wynikiem. Maksymalną odległość marszu zwiększono 5,7-krotnie. W grupie stosującej tylko rehabilitację chodu maksymalny pokonywany pieszo dystans również znacznie się poprawił47. Przegląd Cochrane z 2013 r. wykazał lepsze wyniki u pacjentów poddawanych rehabilitacji w zorganizowanym ośrodku – w porównaniu z tymi, którzy ćwiczyli w domu i samodzielnie zgłaszali raporty z ćwiczeń. W placówce dodatkowy przyrost odległości wyniósł 160 m, a wynik ten utrzymał się przez rok48.
Rehabilitacja pacjentów z chorobą tętnic obwodowych - wnioski
Rehabilitacja naczyniowa jest leczeniem pierwszego rzutu niedokrwienia wysiłkowego u pacjentów z PAOD. Pozwala znacznie zwiększyć maksymalną odległość pokonywaną pieszo, zwłaszcza w przypadku urazów uda. Umożliwia również poprawę równowagi między czynnikami ryzyka, funkcjami poznawczymi i czynnościami życia codziennego.
W przypadku długotrwałych zmian udowych jest równie skuteczna jak leczenie wewnątrznaczyniowe. Najlepiej prowadzić ją pod nadzorem, ale można zalecić ją również jako leczenie ambulatoryjne pod minimalną kontrolą. Terapia taka musi być dostosowana do pacjenta i wielodyscyplinarna. Odpowiada ona na potrzebę oczywistą, ale niezaspokojoną z powodu braku odpowiednich rozwiązań systemowych – wciąż jest źle zalecana i słabo znana osobom decyzyjnym w tym zakresie (kardiolodzy, chirurdzy naczyniowi, lekarze rodzinni). Skierowanie na rehabilitację naczyniową powinno zostać włączone do schematu postępowania z chorobami sercowo-naczyniowymi.
Głównym czynnikiem ryzyka choroby tętnic obwodowych jest, obok cukrzycy, palenie papierosów.
Źródło: Annals of Medicine and Surgery 70 (2021) 102864. ©2021, The Authors Na podstawie licencji Creative Commons 4.0 BY (http://creativecommons.org/licenses/by/4.0/) Adaptacja: Katarzyna Bogiel
- Hirsch A.T., Haskal Z.J., Hertzer N.R. et al., ACC/AHA 2005 Practice Guidelines for the Management of Patients with Peripheral Arterial Disease.
- European Stroke Organisation 1, M. Tendera, V. Aboyans et al., ESC Guidelines on the Diagnosis and Treatment of Peripheral Artery Diseases, 2011.
- Theys S., Rondeux C., Ferrandez J.-C., Bouchet J.-Y., Readaptation dans l’arteriopathie des membres inferieurs, 2009.
- Garrigues D., Ferrari B., Ferrando N.P., Guiraut T., Readaptation vasculaire de l’arteriopathie obliterante des membres inferieurs en, 2018.
- Beebe H.G., Dawson D.L., Cutler B.S., Herd J.A., Strandness Jr. D.E., Bortey E.B. et al., A new pharmacological treatment for intermittent claudication: results of a randomized, multicenter trial, Arch. Intern. Med. (1999).
- Fowkes F.G., Rudan D., Rudan I., Aboyans V., Denenberg J.O., McDermott M.M. et al., Comparison of global estimates of prevalence and risk factors for peripheral artery disease in 2000 and 2010: a systematic review and analysis, Lancet (2013).
- Aboyans V., Ho E., Denenberg J.O., Ho L.A., Natarajan L., Criqui M.H., The association between elevated ankle systolic pressures and peripheral occlusive arterial disease in diabetic and nondiabetic subjects, J. Vasc. Surg. (2008).
- White C.J., White J., White R.A., ACC/AHA: Am Col Card/Am HeartAss 2005 guidelines for the management of patients with peripheral disease, J. Am. Coll. Cardiol. (2006).
- TASC, Trans-Atlantic inter-Society Consensus) II. Inter-Society consensus for the management of peripheral arterial disease, J. Vasc. Surg. (2007).
- TASC I (Trans-Atlantic inter-Society Consensus), Management of peripheral arterial disease, Int. Angiol. (2000).
Gibellini R., Fanello M., Ferrari Bardile A., Salerno M., Aloi T., Exercise training in intermittent claudication, Int. Angiol. (2000). - Hamburg N.M., Balady G.J., Exercise rehabilitation in peripheral artery disease : functional impact and mechanisms of benefits, Circulation (2011).
- Liles D.R., Kallen M.A., Petersen L.A., Bush R.L., Quality of life and peripheral arterial disease, J. Surg. Res. (2006).
- Waldstein S.R., Elias M.F., Introduction to the special section on health and cognitive function, Health Psychol. (2003).
- Activite physique, Contexte et effets sur la sante. Expertise Collective, Inserm, Paris, 2008.
- Watson L., Ellis B., Leng G.C., Exercise for intermittent claudication, Cochrane Database Syst. Rev. (2008).
- Brenner I., Perry M., Brown C.A., Exercise interventions for patients with peripheral arterial disease: a review of the literature, Phys Sportsmed (2012).
- Spronk S., Bosch J.L., den Hoed P.T., Veen H.F., Pattynama P.M., Hunink M.G., Cost-effectiveness of endovascular revascularization compared to supervised hospitalbased exercise training in patients with intermittent claudication: a randomized controlled trial, J. Vasc. Surg. (2008).
- Gardner A.W., Katzel L.I., Sorkin J.D., Bradham D.D., Hochberg M.C., Flinn W.R. et al., Exercise rehabilitation improves functional outcomes and peripheral circulation in patients with intermittent claudication: a randomized controlled trial, J Am Geriatr So c (2001).
- Haute Autorite de Sante, Arteriopathie obliterante des membres inferieurs, Actualisation septembre (2010).
- Tew G.A., Moss J., Crank H., Mitchell P.A., Nawaz S., Endurance exercise training in patients with small abdominal aortic aneurysm: a randomized controlled pilot study, Arch. Phys. Med. Rehabil. (2012).
- Holanda A., Aubourg M., Dubus-Bausiere V., Eveno D., Abraham P., Reeducation des patients ayant une arteriopathie obliterante des membres inferieurs avec une claudication, 2013.
- Gardner A.W., Montgomery P.S., Flinn W.R., Katzel L.I., The effect of exercise intensity on the response to exercise rehabilitation in patients with intermittent claudication, J. Vasc. Surg. (2005).
- Villemur B., Marquer A., Gailledrat E., Benetreau C., Bucci B., Evra V. et al., New rehabilitation program for intermittent claudication: interval training with active recovery: pilot study, Ann Phys Rehabil Med (2011).
- Rondeux C., Dereume J.P., Azama M., Famaey J.P., Goldstein M., Le reentraînement physique ambulatoire de l’arteritique: une methode et ses resultats, Kinesither Scient (1978).
- HAS (HauteAutorite de Sante, Prise en charge de l’arteriopathie chronique obliterante atherosclereuse des membres inferieurs (indications medicamenteuses de revascularisation et de reeducation), J. Mal. Vasc. (2006).
- Quere I., L’education therapeutique des patients atteints d’arteriopathie des membres inferieurs, J. Mal. Vasc. (2008).
- Franco A., Shoop W., Valette A., Readaptation des arteriopathies peripheriques au stade II, J. Mal. Vasc. (1980).
- Lundgren F., Dahllof A.G., Schersten T., Bylund-Fellenius A.C, Muscle enzyme adaptation in patients with peripheral arterial insufficiency: spontaneous adaptation, effect of different treatments and consequences on walking performance, Clin Sci (1989).
- Chomard D., Readaptation de l’arteriopathie des membres inferieurs, EMC (Elsevier Masson SAS, Paris), Cardiologie, 2003, 11-752-A-10.
- Chomard D., Fourreau N., Les tests en readaptation arterielle: etude sur 28 patients, Ann. Readapt. Med. Phys (2001).
- Theys S., Clerin M., Schoevaerdts J.C., Reflexions sur la kinesitherapie analytique des affections arterielles des membres inferieurs, Med. Hyg. (1982).
- Theys S., Du vol sanguin a l’hemometacinesie, Ann. Kinesither. (2000).
- Vayssairat M., Les explorations vasculaires non invasives du pied diabetique, J. Mal. Vasc. (2008).
- Cormier J.M., Fiessinger J.N., Capron L., Atherosclerose obliterante des membres inferieurs, EMC (Elsevier Masson SAS, Paris), Cardiologie, 1984, 11-316-A-10.
- Hiatt W.R., Regensteiner J.G., Hargarten M.E., Wolfel E.E., Brass E.P., Benefit of exercise conditioning for patients with peripheral arterial disease, Circulation (1990).
- Schoop W., Praktische Angiologie, Georg Thieme Verlag, Stuttgart 1975.
- Williams L.R., Ekers M.A., Collins P.S., Lee J.F., Vascular rehabilitation: benefits of a structured exercise/ risk modification program, J. Vasc. Surg. (1991).
- Hiatt W.R., Nawaz D., Regensteiner J.G., Hossack K.F., The evaluation of exercise performance in patients with peripheralvascular disease, J Cardiopulm Rehabil (1988).
- Teixeira da Cunha-Filho I., Gomes Pereira D.A., Borges de Carvalho A.M., Campedeli L., Soares M., de Sousa Freitas J., The reliability of walking tests in people with claudication, Am. J. Phys. Med. Rehabil. (2007).
- Nicolaï S.P., Viechtbauer W., Kruidenier L.M., Candel M.J., Prins M.H., Teijink J. A., Reliability of treadmill testing in peripheral arterial disease: a meta-regression analysis, J. Vasc. Surg. (2009).
- Labs K.H., Nehler M.R., Roessner M., Jager K.A., Hiatt W.R., Reliability of treadmill testing in peripheral arterial disease: a comparison of a constant load wit a graded load treadmill protocol, Vasc. Med. (1999).
- Schwade J., Blomqvist C.G., Shapiro W., A comparison of the response to arm and leg work in patients with ischemic heart disease, Am. Heart J. (1977).
- Tew G., Nawaz S., Zwierska I., Saxton J.M., Limspecific and cross-transfer effects of armcrank exercise training in patients with symptomatic peripheral arterial disease, Clin Sci (2009).
- McDermott M.M., Ades P., Guralnik J.M., Dyer A., Ferrucci L., Liu K. et al., Treadmill exercise andresistance training in patients with peripheral arterial disease with and without intermittent claudication: a randomized controlled trial, J. Am. Med. Assoc. (2009).
- Fokkenrood H.J., Bendermacher B.L., Lauret G.J. et al., Supervised exercise therapy versus non-supervised exercise therapy for intermittent claudication, Cochrane Database Syst. Rev. (2013).
- Fakhry F., Spronk S., van der Laan L., Wever J.J., Teijink J.A., Hoffmann W.H. et al., Endovascularrevascularization and supervised exercise for peripheral artery disease and intermittent claudication: a randomized clinical trial, J. Am. Med. Assoc. (2015).
- Fokkenrood H.J., Bendermacher B.L., Lauret G.J., Willigendael E.M., Prins M.H., Teijink J.A., Supervised exercise therapy versus non-supervised exercise therapy for intermittent claudication, Cochrane Database Syst. Rev. (2013).